Федеральное Государственное Учреждение Здравоохранения цмсч №165 Федерального Медико-Биологического Агентства справочное методическое пособие
| Вид материала | Методическое пособие |
| Неотон (фосфокреатин). Милдронат Диаминовалериановая кислота Следует обратить особое внимание |
- Работа выполнена в фгу «Государственный научный центр лазерной медицины» Федерального, 275.62kb.
- Утверждено, 220.09kb.
- «Научно-исследовательский институт детских инфекций Федерального медико-биологического, 263.32kb.
- Комплексный подход к диагностике и хирургическому лечению заболеваний щитовидной железы, 1223.26kb.
- «Оценка эффективности и безопасности структурно-резонансной терапии у неврологических, 1777.93kb.
- «Санкт-Петербургский институт усовершенствования врачей-экспертов Федерального медико-биологического, 361.07kb.
- Федеральное медико-биологическое агентство, 6378.43kb.
- На правах рукописи, 423.43kb.
- Государственное образовательное учреждение высшего профессионального образования московский, 1119.17kb.
- Государственное образовательное учреждение высшего профессионального образования московский, 1335.69kb.
Кофермент А состоит из аденозин-3,-фосфат-5,-пирофосфата, соединенного сложноэфирной связью с пантотеновой кислотой (витамин), которая в свою очередь соединяется амидной связью с -меркаптоэтиламином. С атомом серы дополнительную тиоэфирную связь образует ацетильная группа. Итоговое вещество называется ацетил-СоА, который является предшественником в синтезе жирных кислот и стероидов из углеводов; осуществляет с помощью ПВДГК ---пируватдегидрогеназного комплекса (состоящего из трех апоферментов и пяти коферментов — тиаминпирофосфат, липоевая кислота, FAD, NAD и кофермент А) связь между процессом образования пирувата в цитозоле, циклом лимонной кислоты и окислением жирных кислот (образует водорастворимые тиоэфиры с жирными кислотами) в матриксе митохондрий; служит ацетилирующим агентом в разнообразных синтетических процессах; кроме того, может утилизироваться в синтезе ацетоуксусной кислоты. При этом каждый фрагмент ПВДГК важен для регуляции многих видов метаболизма, облегчает функционирование разных органов и систем в различных патологических и стрессовых ситуациях—неспецифически.
Это относится и к тиолепте (альфа- липоевая кислота; тиоктовая кислота)--- без всякого обоснования относимой к антирадикальным и антигипоксантам, пригодной для специального лечения, например, невропатий.
Идебенон (нобен; убинон; убихинон)--- ко-фермент Q (переносчик восстановительного эквивалента в дыхательной цепи митохондрий).
Карнитин ( карнитен; элькар).Наряду с белками и углеводами основными источниками энергии являются жиры. Образование энергии из жиров зависит от согласованной работы множества ферментов и переносчиков. Конечной и одной из важнейших стадий этого процесса является окисление жирных кислот и синтез АТФ в ссылка скрыта. Уровень синтеза ссылка скрыта зависит от поступления ссылка скрыта внутрь митохондрий. Ключевым участником этого процесса является L-карнитин, который транспортирует длинноцепочечные жирные кислоты в митохондрии через внутреннюю мембрану последних , в которых происходит их β-окисление до ссылка скрыта с последующей его утилизацией. В более древних органеллах – оксисомах, пероксисомах, карнитин обеспечивает и челночный механизм по доставке ацетил-КоА в ссылка скрыта для пластических целей. Из молодых органелл – митохондрий, ссылка скрыта которых в обратном направлении непроницаема для карнитина, транспорт ацетил-КоА в цитоплазму осуществляется с помощью цитрата, а поступающий в митохондрии карнитин декарбоксилируется до β-метилхолина с последующим удалением.
L-Карнитин играет также важную роль в сохранении стабильного уровня ссылка скрыта, который необходим для активирования карбоксилсодержащих метаболитов. Тем самым l-карнитин включается в промежуточный обмен в целом, регулируя соотношение ацил-CoA/CoASH и поддерживая необходимый уровень свободного CoASH в клетке. CoASH необходим для ссылка скрыта, для ссылка скрыта некоторых аминокислот, для дезинтоксикации органических кислот и ссылка скрыта, для функционирования ссылка скрыта и, следовательно, для работы цикла трикарбоновых кислот. L-Карнитин способствует удалению короткоцепочечных жирных кислот из митохондрии, освобождая внутримитохондриальный CoA, стабилизация уровня которого и функциональная взаимосвязь между пулами СoA и левокарнитина являются жизненно важными для оптимизации энергетического метаболизма.
Цитотоксические органические кислоты, как и ксенобиотики, биотрансформируются превращением в производные ацил-CoA, которые удаляются из дальнейшего катаболического процесса.Анаболический эффект L-карнитина был установлен экспериментально, а также опытом длительного применения в медицинской и спортивно-медицинской практике без объяснения механизма действия. Возможно, анаболические функции L-карнитина осуществляются путем участия в метаболизме ссылка скрыта за счет поддержания оптимального соотношения ацил- CoA/CoASH. Анаболическое действие L-карнитина обусловлено как повышением секреции и ферментативной активности желудочного и кишечного соков, в связи с чем повышается усвояемость пищи, в частности белка, так и увеличением производительности при физических нагрузках.
L-карнитин оказывает защитное действие при ссылка скрыта, что обусловлено ингибированием синтеза церамидов (мощные промоторы клеточного апоптоза) и активности каспаз (ключевые медиаторы апоптоза).
Неотон (фосфокреатин).
Милдронат --- Аналог гамма-бутиробетаина, подавляет гамма-бутиробетаингидроксиназу, снижает синтез карнитина и транспорт длинноцепочечных жирных кислот через оболочки клеток, препятствует накоплению в клетках активированных форм неокисленных жирных кислот - производных ацилкарнитина и ацилкоэнзима А. В условиях ишемии восстанавливает равновесие процессов доставки кислорода и его потребления в клетках, предупреждает нарушение транспорта АТФ; одновременно с этим активирует гликолиз, который протекает без дополнительного потребления кислорода. В результате снижения концентрации карнитина усиленно синтезируется гамма-бутиробетаин, обладающий вазодилатирующими свойствами. Механизм действия определяет многообразие его фармакологических эффектов по функции многих органов.
Биотредин ( L- треонин 0,1г, пиридоксина гидрохлорид 0,005 г). L-треонин в присутствии пиридоксина (витамина В6) распадается на аминокислоту глицин и ацетальдегид (уксусную кислоту), которые стимулируют процессы торможения и одновременно окислительно-восстановительные реакции, процессы дыхания и синтеза АТФ в клетках.
Когитум – ацетиламиноянтарная кислота.
Тонибрал (диметиламиноэтанол).
Лимонтар (янтарная кислота 0,2+ лимонная кислота 0,05).
Диаминовалериановая кислота (орнитин) — ссылка скрыта, играет важную роль в биосинтезе ссылка скрыта. При отщеплении от молекулы диаминовалериановой кислоты оксида углерода при гниении трупов образуется ссылка скрыта — одна из нескольких составляющих, так называемого, ссылка скрыта.При приёме внутрь стимулирует реакцию образования мочевины из аммиака в орнитиновом цикле мочевинообразования. Входит в состав распространённого медицинского препарата Гепа-мерц .
Цитруллин--- ссылка скрыта, которая не входит в состав строительных ссылка скрыта, однако имеет большое число физиологических эффектов, цитруллин участвует в метаболизме мочевины, он является промежуточным метаболитом в утилизации токсичного вещества - аммиака. Из цитруллина может образовываться ссылка скрыта - основной донатор азота, который улучшает кровоток в мышцах; укрепляет иммунную функцию и увеличивает энергетический потенциал организма. Цитруллин встречается в специализированных энзимах, входит в состав кожи, волос и оболочки нервов.
Мильгамма. Комбинированный препарат: ссылка скрыта - жирорастворимая форма тиамина.Тиамин - витамин B1 - регулирует углеводный и белковый обмен в клетке, участвует в процессах жирового обмена, обладает антиоксидантной активностью, регулирует проведение нервного импульса, влияя на передачу возбуждения, способствует развитию анальгетического эффекта.ссылка скрыта - витамин B6 - является кофактором для многих ферментов, действующих в клетках нервной ткани; участвует в декарбоксилировании, в дез- и переаминировании аминокислот, препятствует накоплению аммиака, участвует в синтезе нейромедиаторов (допамин, норадреналин, адреналин, гистамин и GABA).
Триметазидин Цитопротекторный эффект обусловлен повышением энергетического потенциала, активацией окислительного ссылка скрыта и рационализацией потребления ссылка скрыта (усиление аэробного ссылка скрыта и блокада окисления ссылка скрыта).
Тиотриазолин (морфолиний-метил-триазолил-тиоацетат) усиливает действие анаэробного гликолиза, ускоряет процессы окисления в ссылка скрыта с сохранением внутриклеточных запасов ссылка скрыта.
Цитофлавин (инозин= рибоксин +янтарная кислота +рибофлавин +никотинамид в разных соотношениях для орального и парентерального приема). Никотинамид - Витаминное средство (витамин В3, витамин РР). По строению близок к никотиновой кислоте. Представляет собой важный компонент кодегидрогеназы I (НАД) и II (НАДФ), участвующих в окислительно-восстановительных процессах в клетке. Участвует в метаболизме жиров, протеинов, аминокислот, пуринов, тканевом дыхании, гликогенолизе. Не оказывает выраженного сосудорасширяющего действия, при его применении не наблюдается покраснения кожных покровов и ощущения "прилива" крови к голове. Оказывает противопеллагрическое действие. Янтарная кислота. Важнейший участник цикла трикарбоновых кислот, или цикла Кребса. Цикл Кребса — центральное звено метаболизма, основной способ получения энергии при окислении органических субстратов, место пересечения многих метаболических путей. Добавление сукцината извне активирует цикл Кребса в соответствии с принципом Ле-Шателье (добавление в равновесную систему исходных продуктов), что позволяет ускорить процесс вывода недоокисленных продуктов обмена. Пиридоксин. Из трех структурных форм — пиридоксин, пиридоксамин и пиридоксальфосфат — в качестве кофермента работает последняя: пере(=транс)аминирование и декарбоксилирование аминокислот; обмен метионина; синтез и распад цистатионина (роль фолата); обмен триптофана (кинуренин; антраниловая кислота; участие в синтезе никотиновой кислоты); синтез аминолевулиновой кислоты из глицина и сукцинил-КоА; переход глутаминовой кислоты в гамма-аминомасляную кислоту. Рибоксин. (Инозин)— это ссылка скрыта, состоящий из ссылка скрыта, связанного с остатком ссылка скрыта (рибофуранозы) посредством ссылка скрыта.Инозин является компонентом ссылка скрыта и необходим для ссылка скрыта в случае ссылка скрыта.Является производным ссылка скрыта. Инозин можно рассматривать в качестве предшественника ссылка скрыта. Дополнительное введение рибоксина (см. схему метаболизма) по обратной связи дает преимущества анаэробному гликолизу, что в свою очередь, повышает концентрацию 2,3-ДФГ и способствует более полной отдаче кислорода в ишемизированных тканях эритроцитами.
Таким образом, цитофлавин является основой «метаболического прикрытия» , включающего также аспаркам, магнерот, эссенциале, компливит (поливитамины и микроэлементы), тиолепта, гептрал, мексидол, карнитин, убинон.
Все эти метаболиты неспецифичны для любой ткани. В то же время это не означает бесполезности использования метаболитов. Они оказывают дозозависимый эффект на функциональные резервы организма при различных стрессах: синдром хронической усталости, ишемия и реоксигенация миокарда и мозга, тяжелая физическая перегрузка (в том числе в спорте больших достижений), изменение метаболизма при интоксикации (лекарственные, бытовые, профессиональные; лучевые нагрузки) и различных заболеваниях (бронхо-легочной системы, печени, сердца, мозга).
Легко понять различие между коррекцией функции и структуры на примере влияния на фармакокинетику антиаритмика этмозина ингибитором микросомального окисления циметидином: Под влиянием циметидина Сmax и АUС этмозина увеличиваются у больных ХИБС настолько, что приближаются к показателям у больных тяжелым циррозом печени. Однако уловить ухудшение в состоянии печени под влиянием циметидина удалось только с помощью радиоизотопной гепатографии, а все остальные клинико-инструментальные и лабораторные показатели были в норме.
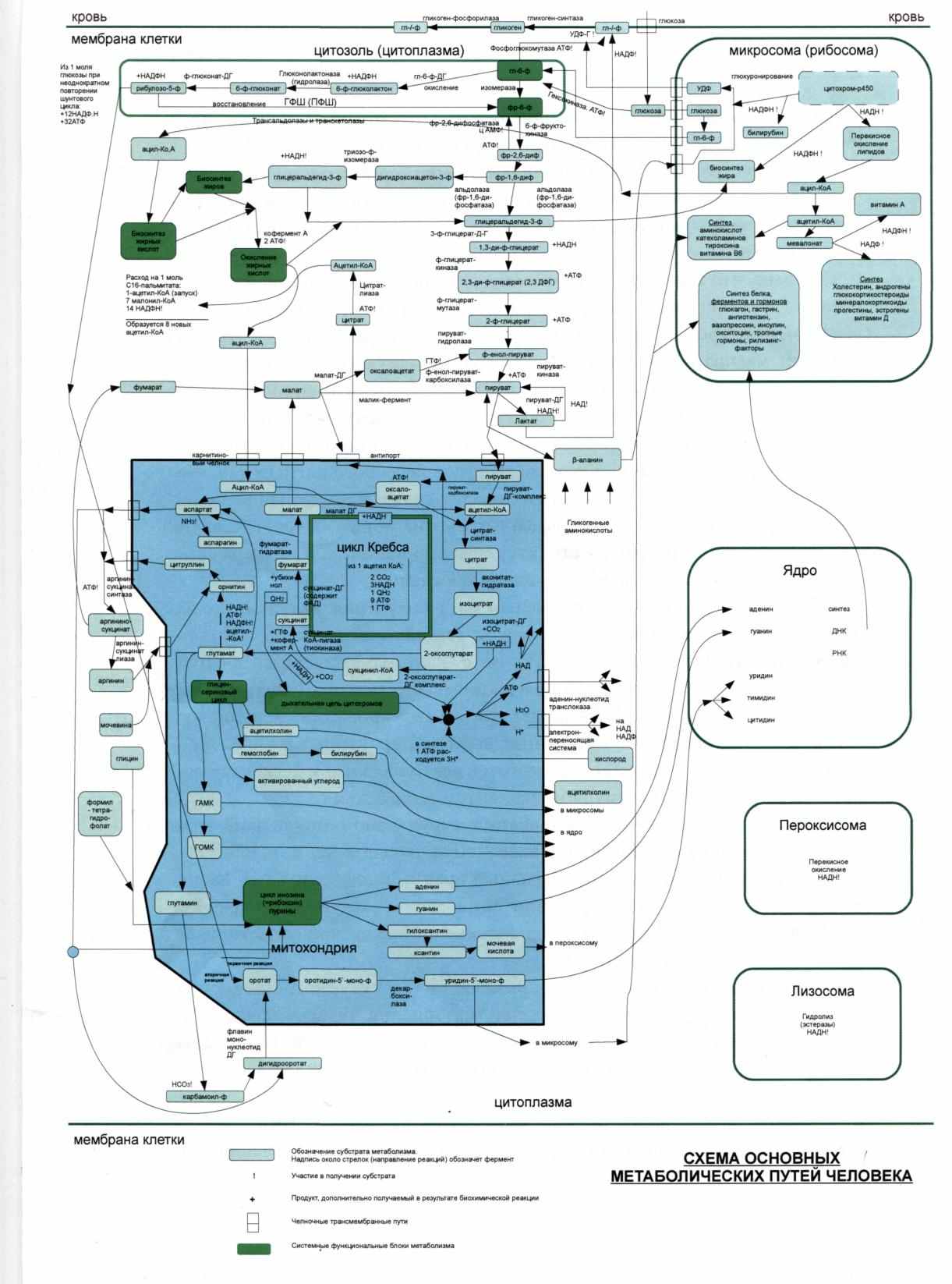
Следует обратить особое внимание на то, что метаболиты включаются не в клеточные структуры, а в метаболические пути. При этом интенсификация метаболизма и в том числе детоксицирующий эффект могут быть настолько велики, что уже отражаются на структуре организма.
Высокий уровень метаболизма в клетках “хозяина” (генетический вариант или “подкормка” метаболитами с активной индукцией СБК) способен переводить альтернативную инфекцию в мягкое или латентное течение, в частности, за счет создания шунтирующих метаболических путей, лишающих, в частности, вирус необходимых субстратов метаболизма.
Однако теоретические псевдоэкстраполяции, рекламирующие “непосредственное включение метаболитов в мембраны” клеток печени (эссенциале), интимы сосудов (эйконол), мукополисахариды типа хондроитина и т. п., на практике не подтверждаются.
Для понимания роли рекламируемых фармакопрепаратов в стимуляции функционирования разных органов следует представлять участие метаболитов в основных видах метаболизма.
Общий баланс цитратного цикла состоит в том, что из одного ацетильного остатка образуются 2 СО2, 3 НАДН + Н+ и одна молекула восстановленного убихинона (QН2). При этом за счет восстановленных форм коферментов путем окислительного фосфорилирования в клетке синтезируются 9, а с учетом трансформации одной молекулы ГТФ — 10 молекул АТФ.
Избыток цитрата (введение лимонтара) блокирует гликолиз в нескольких ферментных узлах, оставляя и даже ускоряя работу пентозофосфатного шунта, но блокируя ТГлипазу и ингибируя липолиз.
Цитратный цикл играет центральную роль в промежуточном метаболизме клетки. Наряду с катаболическими и анаболическими цикл выполняет и амфиболические функции. Промежуточные соединения цитратного цикла, включая такие важные метаболиты, как пируват и ацетил-КоА, способные окисляться до СО2, идентичны промежуточным соединениям многих катаболических путей. Образующиеся в цикле восстановительные эквиваленты окисляются в дыхательной цепи (окислительное фосфорилирование) с образованием АТФ (АТР).
Промежуточные соединения цитратного цикла включаются во многие процессы биосинтеза, например в биосинтез глюкозы (глюконеогенез: оксалоацетат и малат), синтез порфиринов (сукцинил-КоА) и синтез аминокислот (2-оксоглутарат, оксалоацетат). Кроме того, цитратный цикл поставляет в цитоплазму ацетил-КоА, необходимый для синтеза жирных кислот и изопреноидов.
В итоге, улучшение функционирования цитратного цикла (см. рис. 1) за счет введения лимонтара, сукцината, вторично—за счет аспартата, глутамата способно улучшить функциональное состояние многих систем и органов.
На этом основана широкая реклама по псевдоэкстраполяции этих данных на возможность влияния метаболической коррекции на восстановление структуры разных органов.
В частности, это касается альфа-липоевой кислоты (тиоктовая кислота; липоамид; тиолепта).
В пируватдегидрогеназной реакции участвуют три различных фермента. Пируватдегидрогеназа катализирует декарбоксилирование пирувата, перенос образованного гидроксиэтильного остатка на тиаминдифосфат (ТРР), а также окисление гидроксиэтильной группы с образованием ацетильного остатка. Этот остаток и полученные восстановительные эквиваленты переносятся на липоамид. Следующий фермент, дигидролипоамидацетилтрансфераза переносит ацетильный остаток с липоамида на кофермент А, при этом липоамид восстанавливается до дигидролипоамида. Последний снова окисляется до липоамида третьим ферментом, дигидролипоамиддегидрогеназой с образованием НАДН + Н+ (nadn + Н+). Электроны переносятся на растворимый НАД+ через ФАД и каталитически активный дисульфидный мостик субъединицы дигидролипоамид-ДГ.
Пять разных коферментов этой реакции различными способами ассоциированы с белковыми компонентами ферментов. Тиаминдифосфат нековалентно связан на пируват ДГ. Липоамид ковалентно связан с остатком лизина дигидролипоамидацетил-ТФ, а ФАД прочно ассоциирован в виде простетической группы на дигидролипоамид-ДГ. НАД+ (NAD+) и кофермент А (на базе витамина В3 пантотеновой кислоты) взаимодействуют с комплексом в виде растворимых коферментов.
Для оптимального кругооборота цикла Кребса промежуточные продукты (-кетоглутарат) должны забираться для синтеза мочевины, креатина, ацетил-холина, билирубина и нуклеиновых кислот с использованием коферментов: пиридоксаль-витамин В6; фолиевая кислота=Вс и цианокобаламин=витамин В12 (причем последние два задействованы еще и в глицин-сериновом цикле).
Избыток глутамата через глицин-сериновый цикл и нуклеиновые синтезы ядра клетки усиливает работу микросом по анаболизму, а через аспарагинат-урацил-уридин усиливает ресинтез гликогена по механизму УДФГ (одновременно ингибируется липолиз).
В цитратном цикле (цикл лимонной кислоты; метаболический процесс, протекающий в матриксе митоходрий) ацетильные остатки (СН3СО-) окисляются до диоксида углерода (СО2). Полученные при этом восстановительные эквиваленты переносятся на НАД+ или убихинон и включаются в дыхательную цепь.
Большая часть потребляемого в цитратном цикле ацетил-КоА получает ацетильные остатки, образовавшиеся в результате -окисления жирных кислот и окислительного декарбоксилирования пирувата, катализируемого пируватдегидрогеназой. Оба процесса протекают в матриксе митоходрий.
Ацетил-КоА, образующийся в матриксе митохондрий при участии пируватдегидрогеназы, не может проходить через внутреннюю митохондриальную мембрану. Поэтому ацетильный остаток конденсируется митохондриальной цитрат-синтазой с оксалоацетатом с образованием цитрата. Последний переносится в цитоплазму по механизму антипорта с малатом,где снова расщепляется АТФ-зависимой цитрат-лиазой с образованием ацетил-КоА и оксалоацетата. Образовавшийся оксалоацетат восстанавливается цитоплазматической малатдегидрогеназой в малат, который возвращается в митохондрии за счет антипорта или подвергается окислительному декарбоксилированию “малатферментом” с образованием пирувата. Образующийся НАДФ + Н+ принимает участие в биосинтезе жирных кислот.
Промежуточные продукты цитратного цикла присутствуют в митохондриях лишь в очень незначительных количествах. При окислении ацетил-КоА они вновь регенерируются, так что их концентрации остаются практически постоянными. В то же время анаболические процессы быстро истощают пул некоторых промежуточных продуктов цикла. Поэтому их запас постоянно пополняется за счет метаболитов, поступающих из других источников. Ферментативные процессы, пополняющие запас промежуточных продуктов цикла, называются анаплеротическими (возмещающими) реакциями.
Анаплеротический характер носит деградация большинства аминокислот, так как при этом образуются промежуточные соединения цикла или пируват (глюкогенные аминокислоты). Фактически глюконеогенез поддерживается в основном за счет деградации аминокислот. Особенно важной анаплеротической стадией в метаболизме животных является превращение пирувата в оксалоацетат.
Эта АТФ-зависимая реакция, катализируемая пируваткарбоксилазой, позволяет включать в глюконеогенез пируватпоставляющие аминокислоты и лактат.
В отличие от пирувата ацетил-КоА не является анаплеротическим метаболитом у высших животных. Его углеродный скелет полностью окисляется до СО2 и поэтому не принимает участия в биосинтезе. Поскольку при деградации жирных кислот образуется ацетил-КоА, клетки животных не в состоянии превращать жирные кислоты в глюкозу. Поэтому при голодании в организме прежде всего утилизируются не жиры, а белки. Высвободившиеся аминокислоты, напротив, могут превращаться и в жирные кислоты, и в глюкозу и, тем самым, поддерживать уровень сахара в крови.
Глюконеогенез поддерживается ресинтезом из лактата (цитозоль); из фумарата (через малат выходит в цитозоль) — с привлечением тирозина, фенилаланина, аспарагината, оксоглутарата (через него — пролина, гистидина, аргинина, глутамина); из пирувата (и через него — аланин, метионин, цистеин, серин, глицин, треонин, триптофан, лейцин, лизин); из сукцината (валин, изолейцин); из глицерина (выходит в цитозоль из микросом при распаде жира).
При распаде мышечного белка из лейцина, тирозина, фенилаланина образуется избыток ац-КоА, дающий кетоновые тела (ацетон, ацетоацетат, 3-гидроксибутират) и блокирующий дальнейший переход пирувата в митохондрии, а также “переворачивающий” метаболизм жиров от липолиза к микросомальному ресинтезу жира.
Некоторые из перечисленных аминокислот не могут синтезироваться в организме человека и должны поступать вместе с пищей (незаменимые аминокислоты: валин, лейцин, изолейцин, метионин, фенилаланин, триптофан, треонин, лизин). Из глутамата образуется -аминомасляная кислота (нейромедиатор), из дигидроксифенилаланина — дофамин (нейромедиатор и предшественник адреналина и норадреналина). В состав фосфолипидов входит серин и этаноламин, кофермента А — цистеамин и -аланин, витамина В12 — аминопропанол (производное треонина). Гликогенные аминокислоты — все, кроме кетогенных лизина и лейцина.
Аланин, аспарагиновая кислота, глицин принимают участие в переаминировании.
Тирозин, фенилаланин – в синтезе меланина, инсулина, папаина, адреналина, норадреналина, допамина, ДОФА.
Аргинин --- высвобождение глюкагона, пролактина, соматостатина, адреналина; участие в синтезе мочевины (с орнитином, цитруллином.
Глутамин --- переносчик аминогрупп; синтез триптофана, гистидина, пуринов, белков.
Глутамат как нейротрансмиттер имеет важное значение при многих физиологических функциях ЦНС: установлена роль ММБА- подтипа глутаматных рецепторов в процессах обучения и памяти; доказаны нейротоксические свойства (эксайтотоксичность) на рецепторы гиппокампа (применяется лечение мемантином).
Метионин и пролин --- синтез холина,адреналина,цистеина.
Серин --- синтез цистина, глицина, метионина,цистеина, триптофана.
Аспарагиновая кислота --- синтез нуклеиновых кислот.
Аспартат, глицин, глутамат сами являются медиаторами нервной системы.
Рибоксин --- усиливает синтез ряда нуклеиновых кислот, увеличивает образование 2,3-ДФГ и вторично усиливает отдачу кислорода оксигемоглобином (сдвиг кривой диссоциации).
В количественном отношении белки образуют самую важную группу макромолекул. В организме человека массой 70 кг содержится примерно 10 кг белка, причем большая его часть локализована в мышцах. По сравнению с белками доля других азотсодержащих веществ в организме незначительна. Поэтому баланс азота в организме определяется метаболизмом белков, который регулируется несколькими гормонами, прежде всего тестостероном и кортизолом.
В организме взрослого человека метаболизм азота в целом сбалансирован, то есть количества поступающего и выделяемого белкового азота примерно равны. Если выделяется только часть вновь поступающего азота, баланс положителен. Это наблюдается, например, при росте организма. Отрицательный баланс встречается редко, главным образом как следствие заболеваний.
Полученные с пищей белки подвергаются полному гидролизу в желудочно-кишечном тракте до аминокислот, которые всасываются и кровотоком распределяются в организме.
Через кишечник и в небольшом объеме также через почки организм постоянно теряет белок. В связи с этими неизбежными потерями ежедневно необходимо получать с пищей не менее 30 г белка. Эта минимальная норма едва ли соблюдается в некоторых странах, в то время как в индустриальных странах содержание белка в пище чаще всего значительно превышает норму. Аминокислоты не запасаются в организме, при избыточном поступлении аминокислот в печени окисляется или используется до 100 г аминокислот в сутки. Содержащийся в них азот превращается в мочевину и в этой форме выделяется с мочой, а углеродный скелет используется в синтезе углеводов, липидов или окисляется с образованием АТФ.
Предполагается, что в организме взрослого человека ежедневно разрушается до аминокислот 300—400 г белка (протеолиз). В то же время примерно то же самое количество аминокислот включается во вновь образованные молекулы белков (белковый биосинтез). Высокий оборот белка в организме необходим потому, что многие белки относительно недолговечны: они начинают обновляться спустя несколько часов после синтеза, а биохимический полупериод составляет 2—8 дней. Еще более короткоживущими оказываются ключевые ферменты промежуточного обмена. Они обновляются спустя несколько часов после синтеза. Это постоянное разрушение и ресинтез позволяют клеткам быстро приводить в соответствие с метаболическими потребностями уровень и активность наиболее важных ферментов. В противоположность этому особенно долговечны структурные белки, гистоны, гемоглобин или компоненты цитоскелета.
Из кишечника аминокислоты из переваренного белка пищи и экскретированные кишечником (из организма) всасываются в определенной оптимальной констелляции (>150 г в сутки).
Около 100 г аминокислот синтезируется из пирувата, фосфоенолпирувата, 3-фосфоглицерата, 2-кетокислот и фосфатов сахаров.
Существует несколько путей удаления аминогруппы во время распада аминокислоты (дезаминирования). Обычно NH2-группа переносится путем трансаминирования на 2-оксоглутарат. Образующийся глутамат в дальнейшем вновь превращается в 2-оксоглутарат с помощью глутаматдегидрогеназы (окислительное дезаминирование). В этой реакции образуется свободный аммиак (NH3), который у высших животных превращается в мочевину и выводится из организма. Аммиак освобождается также при гидролизе амидных групп аспарагина и глутамина (гидролитическое дезаминирование). Другим превращением, при котором образуется NH3, является элиминирующее дезаминирование серина в пируват.
