К лечению в настоящее время, то послужит впоследствии наилучшим материалом для будущей более счастливой терапии
| Вид материала | Исследование |
- Принципы терапии аллергических заболеваний, 781.38kb.
- Международная конвенция о подготовке и дипломированны моряков и несении вахты 1978, 91.82kb.
- Социализация и профессиональная адаптация, 100.74kb.
- Нную лицензию на правоведения образовательной деятельности 27 специальностям бакалавриата, 70.96kb.
- Н. В. Андрецова г. Донецк, Украина Сахарный диабет остается одной из самых актуальных, 177.59kb.
- Окружной конкурс «Фестиваль педагогического мастерства». Основы антропоэкологии и генетики, 738.12kb.
- Современные аспекты хирургического лечения ибс, 84.02kb.
- Программа курса «Человек и профессия», 335.03kb.
- Кошкина В. А, 165.97kb.
- Зодчество Древней Руси» пишет: «Сохранившийся почти полностью Никольский собор в настоящее, 799.57kb.
Основанием клинической медицины служит
самое подробное исследование данного случая,
которое если не всегда будет иметь приложение
к лечению в настоящее время, то послужит
впоследствии наилучшим материалом
для будущей более счастливой терапии.
(С.П. Боткин)
1 Актуальність, визначення
Злоякісні новоутворення різної локалізації діагностують щороку більше ніж у 10 млн людей, а 6 млн людей щороку гинуть, що становить 12 % від загальної смертності у світі. Вірогідність розвитку злоякісних новоутворень різко збільшується з віком:
- у віці до 39 років хворіє 1 із 58 чоловіків та 1 із 52 жінок;
- 40-59 років – 1 із 13 чоловіків, 1 із 11 жінок;
- 60-79 років – 1 із 3 чоловіків, 1 з 4 жінок;
- 76 % пухлин виникає після 55 років.
Сучасні методи діагностики й лікування онкологічних захворювань дають змогу вчасно виявити та призначити адекватне специфічне лікування більшості таких пацієнтів. На жаль, до лікарів звертаються 2/3 хворих із поширеним пухлинним процесом, що зумовлено такими основними при-чинами:
- зверненням на термінальній стадії;
- слабкою онкологічною настороженістю;
- низькою обізнаністю щодо ранніх симптомів раку, які можуть проходити під маскою доброякісних уражень, що одержали назву паранеопластичних синдромів. За слова-ми Є.М. Тарєєва, «паранеопластичний синдром несе в орга-нізмі "сторожову службу" як маркер назріваючого пухлин-ного процесу».
Паранеопластичний синдром (ПНС) - це клінічні прояви пухлини, що спостерігаються на відстані від первинного вогнища і виникають у результаті біохімічних, гормональних або імунологічних порушень, індукованих пухлиною, а не внаслідок її прямої дії на тканини та внутрішні органи (метастазування, проростання).
Термін «паранеопластичний синдром» введений у 1948 році та дослівно в перекладі означає «синдром, супутній пухлині» (para - біля, neoplasma – пухлина), хоча це синд-ром, який водночас безпосередньо нею зумовлений. Знання ПНС важливе для лікарів усіх спеціальностей, оскільки пух-лини різних локалізацій на певних етапах до появи місцевої симптоматики можуть проявлятися неспецифічними ознака-ми та помилково трактуватися як самостійне захворювання шкіри, суглобів, нирок тощо. Це, з одного боку, може при-звести до неоправданого лікування, а з іншого – до сповіль-нення онкологічного пошуку і запізнілої діагностики пух-лини.
Паранеоплазма, за своєю суттю, являє собою клінічний прояв спричинених пухлинним процесом патологічних змін гомеостазу, при якому сталість внутрішнього середовища організму порушується через виснаження функціональних ресурсів компенсаторних механізмів.
Термін «ПНС» охоплює велику групу захворювань, різ-них як за клінічними проявами, так і за патогенетичними механізмами, але обов'язковою умовою для їх виникнення є існування пухлини.
Види ПНС:
■ ендокринопатії;
■ гематологічні;
■ ревматологічні;
■ шлунково-кишкові;
■ ниркові;
■ шкірні;
■ неврологічні;
■ інші.
Частота ПНС становить 15 % у дебюті онкозахворюван-ня та 50-70 % на розгорнутій стадії.
Час виникнення ПНС:
- на фоні клінічних ознак злоякісної пухлини;
- передує появі перших клінічних ознак первинної пухлини місяці і навіть 1-2 роки;
- одночасно із симптомами пухлини.
2 Етіопатогенез
У більшості випадків причинами паранеопластичних ревматичних реакцій служать бронхогенний рак легень і нефрокарцинома. Серед інших локалізацій неопластичного процесу часто трапляється рак молочної залози, придатків матки, матки, передміхурової залози, шлунка і товстого кишківника, значно рідше - рак стравоходу, підшлункової залози, печінки, жовчного міхура, глотки, сечового міхура, щитовидної залози, наднирників, яєчок, залоз шкіри та ін.
У різних хворих один і той самий ревматичний ПНС (РПНС) може бути ознакою пухлин різної локалізації і неод-накової морфологічної будови, і, навпаки, при пухлинах однієї і тієї самої локалізації та подібної морфологічної будови можуть бути різні ревматичні прояви. Більше того, у одного і того ж хворого метахронні пухлини, що послідовно виникають протягом життя, здатні викликати різні РПНС. Для рецидивних і метастазуючих пухлин характерна одно-типність ревматичних симптомів. У деяких випадках вони виникають після оперативного лікування злоякісних ново-утворень, у тому числі іноді через декілька років, що може бути зв'язано з розвитком метастазів первинної пухлини чи з появою вогнища злоякісного росту тієї ж чи іншої локалі-зації.
Відомо, що для ревматичних і онкологічних хвороб є ха-рактерні спільні інфекційні тригери: HCV і HBV, вірус Еп-штейна - Барра, цитомегаловірус, ретровіруси тощо. Вірусна теорія стверджує участь Т-лімфотропних вірусів людини І типу, вірусу Епштейна-Барра у регуляції клітинної пролі-ферації й апоптозу, а також безпосередню пошкоджувальну дію вірусів.
В основі розвитку РПНС лежать гіперергічні імуноза-пальні реакції реагінового, імунокомплексного або ауто-імунного типу на метастатичні злоякісні клітини, «чужо-рідні» пухлинні антигени, які, ймовірно, реагують з антиге-нами нормальних тканин. Крім того, у розвитку паранео-пластичного імунного запалення може мати значення утво-рення в нормальних тканинах неоантигенів під впливом циркулюючих продуктів життєдіяльності неоплазми. Перед-бачають, що характер паранеопластичних ревматичних проявів визначається як антигенними властивостями пухли-ни, так і індивідуальними імунними реакціями хворого, а та-кож генетично детермінованим чи набутим дисбалансом основних ланок імунної системи. Участь імунних реакцій підтверджується їх виникненням не тільки при вісцераль-ному ракові, а й при новоутвореннях імунної системи (тимо-ма, лімфолейкоз, лімфома, лімфосаркома, лімфогрануле-матоз, парапротеїнози).
Спільними для онкологічної та ревматичної патології є такі імунопатологічні чинники, як онкопротеїни, туморсу-пресивні та онконевральні гени, гени проліферації.
Важливу роль відіграє прямий токсичний вплив пухлин-них субстанцій; обмінні порушення, зумовлені пухлиною: гіперкальціємія, гіперурикемія; ектопічна продукція гормо-нів і гормоноподібних субстанцій (адренокортикотропного, антидіуретичного, паратгормону, еритропоетину).
Тригерними агентами є хлорвініл та сполуки кремнію, різні олії, органічні розчинники, епоксидні смоли, лікарські засоби, харчові домішки та компоненти (блеоміцин, серото-нін, ерготамін, L-триптофан). Відомі мутагенний, промотор-ний, стимуляторний ефекти хімічних чинників у розвитку онкопатології та токсичний, ад'ювантний і мутагенний – у розвитку ревмопатології. Особлива роль хімічних чинників визнана у розвитку склеродермоподібних станів та поліміо-зиту. В онкологічній практиці описано розвиток постхіміо-терапевтичного ревматизму, що полягає в появі клінічних проявів системної склеродермії, системного червоного вов-чака, суглобового синдрому через 2-15 міс. після курсу хіміотерапії.
Дискутується також роль спільних етіологічних факто-рів і генетичної схильності у розвитку ревматичних захво-рювань і неопластичного процесу, меншою мірою пухлин-них захворювань імунної системи, на користь чого свідчить трансформація синдрому Шегрена у В-клітинну лімфому. Певну роль у розвитку паранеопластичних ревматичних реакцій, ймовірно, відіграє безпосередній вплив біологічно активних речовин, що виділяються пухлинними клітинами.
Вважають, що імунологічні розлади в організмі можуть з'являтися на ранніх стадіях злоякісної трансформації тка-нин, коли новоутворення внаслідок своїх невеликих розмірів ще не виявляється. Описані випадки розвитку злоякісних новоутворень у хворих, які протягом багатьох років хворіли на хронічні запальні ревматичні захворювання, наприклад ревматоїдний артрит чи дифузне захворювання сполучної тканини. Вважається, що ці випадки можуть бути пов'язані з тривалою імуносупресивною терапією, з фіброзом і епіте-ліальною перебудовою органів, що розвинулися у результаті ревматичного запалення, а також - генетичною схильністю до обох типів захворювання. Крім того, має значення збіль-шення тривалості життя хворих на хронічні ревматичні захворювання, оскільки в умовах сучасної адекватної терапії хворі доживають до «ракового» віку, і злоякісна пухлина виникає як друге захворювання. Проте описано багато випадків, коли симптоми ревматичного захворювання, що тривало існували до появи ознак злоякісної пухлини, зника-ли після радикального її лікування.
Зважаючи на невивченість детальних механізмів роз-витку паранеопластичних ревматичних синдромів, виділя-ють декілька варіантів їх патогенезу. Існує теорія «бло-кованої диференціації», згідно з якою відбуваються припи-нення диференціювання клітини на одному з етапів, її акти-вація й синтез гормонів або гормоноподібних субстанцій, що відіграють роль медіаторів ПНС. Теорія «забороненого контакту» стверджує, що тканинні продукти, які у нормі не взаємодіють з імунними клітинами, внаслідок неповноцін-ності судинного апарату й базальних мембран пухлинних тканин надходять до мікроциркуляторного русла та призво-дять до розвитку аутоімунного процесу.
Як варіанти етіопатогенезу ПНС розглядають: утворення неоантигенів й антиідіотипів; активацію онкогенів, прото-онкогенів, гальмування генів супресії; інактивацію гена р53, що контролює апоптоз; дисбаланс про- та протизапальних цитокінів.
Онкологічні та ревматичні захворювання мають подібні чи однакові тригерні агенти, вони часто є подібними за морфогенезом і характеризуються ембріональним типом реакції тканин, порушенням регуляторних механізмів (авто-номний чи напівавтономний ріст і функціонування клітин), дисбалансом ендогенних медіаторів (цитокінів, чинників росту), частим виникненням лімфопроліферативних захво-рювань та моноклональної гамапатії.
ПНС найчастіше виникає на фоні:
■ низькодиференційованих злоякісних новоутворень епітеліального походження (рак різної локалізації);
■ пухлинного ураження імунної системи (тимоми, лімфоми).
3 Форми ревматичних паранеопластичних синдромів
У клінічній практиці маніфестація РПНС різноманітна: це синдроми і симптомокомплекси, що подібні з дифузними захворюваннями сполучної тканини (ДЗСТ), артритами, метаболічними артропатіями й іншими захворюваннями кістково-м'язової системи.
Артрити при пухлинах характеризуються гострим почат-ком, асиметричним ураженням суглобів як верхніх, так і нижніх кінцівок. Характерним є невідповідність між тяжким станом хворих і відносно невираженим суглобовим синд-ромом. На думку про паранеопластичний характер артриту повинно наводити ураження суглобів у хворих похилого та старечого віку, хоча відомі випадки ювенільного артриту при пухлинах у дітей. Суглобовий синдром може поєдну-ватися з екстраартикулярними паранеопластичними ревма-тичними проявами. При цьому в одних випадках відмі-чаються окремі симптоми і синдроми, що свідчать про сис-темний характер імунозапального процесу (наприклад, гарячка неправильного типу, яка не піддається терапії анти-біотиками та глюкокортикоїдами), збільшення периферич-них лімфатичних вузлів, гепато- і спленомегалія, випітні серозити (плеврит, перикардит), міопатія, екзантема (вузлу-вата еритема, рецидивна кропив'янка, багатоформна ексуда-тивна еритема, геморагічні висипання, панікуліт), синдром Стівенса-Джонса (еритематозні, макульозні, папульозні, бульозні і/чи ерозивно-виразкові висипання на слизовій обо-лонці порожнини ротоглотки, кон'юнктивах та геніталіях), виражене підвищення швидкості осідання еритроцитів (ШОЕ), гіпергаммаглобулінемія, кріоглобулінемія, підви-щення у крові імуноглобулінів і циркулюючих імунних ком-плексів, наявність антинуклеарних антитіл, LE-клітин чи ревматоїдного фактора, анемія, лейкопенія і тромбоцитопе-нія аутоімунного генезу. Проте навіть за наявності ракових метастазів ШОЕ може бути у межах норми. Генералізована імунозапальна реакція може проходити під маскою ревма-тоїдного артриту з вісцеральними проявами за типом синд-рому Стілла або симптомокомплексу, що нагадує певне ДЗСТ (найчастіше це дерматоміозит-поліміозит) чи систем-ний васкуліт.
Екстраартикулярні паранеопластичні ревматичні прояви, так, як і артрит, можуть виникати на ранніх стадіях злоякіс-ного росту, вони відрізняються резистентністю до стероїдної терапії та зникають після радикального видалення пухлини. В окремих хворих зменшення чи навіть зникнення систем-них ревматичних реакцій відбувається у міру прогресування неопластичного процесу і наростання ракової інтоксикації.
Ранню діагностику РПНС ускладнює те, що він здатний розвиватися на тлі різних пухлинних процесів, а в той же час новоутворення виникають у людей, які страждають на ДЗСТ.
Взаємозв'язок поліартриту і злоякісного новоутво-рення підтверджується такими фактами:
- короткий проміжок часу (в середньому 10 місяців) між появою серонегативного артриту і розвитком злоякісної пухлини;
- зменшення вираженості клінічних проявів артриту на фоні лікування пухлини;
- рецидив артриту при рецидиві пухлини.
Виділяють такі основні форми РПНС:
- гіпертрофічну остеоартропатію;
- пахідермоперіостоз;
- ревматоїдоподібну артропатію;
- синдром рефлекторної симпатичної дистрофії;
- стеатонекротичний поліартрит;
- гіперкальціємічну артропатію;
- анкілозивний спондилоартрит;
- псевдосклеродермічний симптомокомплекс;
- пухлинний дерматоміозит;
- ревматичну поліміалгію;
- фіброміалгію;
- люпоїдний синдром;
- синдром Шегрена;
- панікуліт;
- рецидивний поліхондрит;
- васкуліти, синдром Світа;
- вузлувату еритему;
- антифосфоліпідний синдром;
■ онкогенну остеомаляцію;
■ гарячку гектичного типу з добовими коливаннями температури 1-2 градуси;
■ небактеріальний тромботичний ендокардит.
4 Паранеопластичне ураження суглобів
4.1 Гіпертрофічна остеоартропатія
Гіпертрофічна остеоартропатія (ГОА, синдром Марі – Бамбергера) вперше була описана у 1889 році Бамбергером у хворих на хронічні легеневі захворювання, а визначена Марі як «пневмонічна ГОА».
ГОА - множинний остеофікуючий періостоз із переваж-ною локалізацією в дистальних фалангах кистей. ГОА може бути первинною та вторинною, яка, у свою чергу, буває місцевою та генералізованою.
Місцева форма ГОА спостерігається у хворих з гемі-плегією, аневризмою, інфекційним артритом, відкритою боталовою протокою. Генералізована форма виникає при бронхогенному раку легень (10 %), мезотеліомі (50-60 %). У той самий час метастатичне ураження легень при пухлинах іншої локалізації не призводить до виникнення даного синд-рому. Як правило, синдром Марі - Бамбергера є проявом вісцеральної неоплазми, що клінічно не проявляється й локалізована у 90 % випадків інтраторакально. Встановлено, що при раку легені, що розвинувся на тлі ідіопатичного фіброзуючого альвеоліту (ІФА), частота ГОА досягає 95 %, а при ураженні легеневого інтерстицію без ознак неоплас-тичної трансформації її виявляють в 63 % хворих. При раку легені ГОА виявлено у 30 % хворих, причому частота вияв-лення «пальців Гіппократа» залежить від морфологічної форми раку легені і становить 35 % при недрібноклітинному варіанті та 4 % - при дрібноклітинному. Розвиток ГОА при раку легені зв'язують із гіперпродукцією гормону росту пухлинними клітинами. Паранеопластичну природу змін дистальних фалангів пальців рук за типом «барабанних паличок» підтверджує зникнення цього клінічного феномена після успішної резекції пухлини легені.
«Пальці Гіппократа» можуть бути паранеопластичним проявом пухлин, що локалізовані й поза межами легень: злоякісній пухлині тимуса, раку стравоходу, товстої кишки, гастриномі, саркомі легеневої артерії, лімфомі та лімфогра-нулематозі з метастазами в лімфатичні вузли середостіння, тератомі, ліпомі.
Паранеопластичне походження змін дистальних фалангів пальців рук за типом «барабанних паличок» можна припус-кати при швидкій їхній появі (особливо в пацієнтів без дихальної, серцевої недостатності й за відсутності інших причин гіпоксемії), а також при їх поєднанні з іншими мож-ливими позаорганними, неспецифічними ознаками злоякіс-ної пухлини: збільшенням ШОЕ, змінами картини перифе-ричної крові (особливо тромбоцитозом), тривалою лихо-манкою, суглобовим синдромом і рецидивними тромбозами різної локалізації.
ГОА реєструють також при хронічних запальних захво-рюваннях кишечнику (хворобі Крона, виразковому коліті) та цирозах печінки. При хворобі Крона зміна пальців за типом «барабанних паличок» може передувати її власне «кишко-вим» проявам. Однією з найчастіших причин феномена «пальців Гіппократа» є цироз печінки з портальною гіпертензією й прогресуючою дилатацією судин малого кола кровообігу, що призводить до гіпоксемії (так званий леге-нево-печінковий синдром). У даних хворих ГОА, як прави-ло, поєднується із шкірними телеангіектазіями.
Зміни дистальних фалангів пальців рук за типом «бара-банних паличок» є найбільш характерними для ІФА; ступінь їх виразності, яскравість ціанозу нігтьових валиків розгля-дають як ознаки, що чітко характеризують активність ура-ження легенів і прогноз захворювання. Частота виявлення «пальців Гіппократа» зростає в міру прогресування уражен-ня легенів і залежить від тяжкості дихальної недостатності. При інших захворюваннях легень зміни дистальних фалан-гів пальців рук за типом «барабанних паличок» виявляють рідше, як правило, при формуванні стійкої гіпоксемії й на термі-нальній стадії захворювання. Відносно рано «пальці Гіппократа» з'являються у пацієнтів, що страждають на азбестоз, і це завжди свідчить про високий ризик смерті.
«Пальці Гіппократа» традиційно відносять до неспеци-фічних, так званих позасерцевих, клінічних ознак інфек-ційного ендокардиту. На користь інфекційного ендокардиту у хворого з «пальцями Гіппократа» свідчать висока лихо-манка з ознобами, збільшення ШОЕ, лейкоцитоз, анемія, підвищення активності печінкових трансаміназ, різноманітні варіанти ураження нирок. Для підтвердження інфекційного ендокардиту у всіх випадках показане виконання черезстра-вохідної ехокардіографії.
Причиною виникнення ГОА є застосування блокаторів - рецепторів ангіотензину ІІ, лозартану та валсартану, після відміни яких зміни повністю регресували.
«Пальці Гіппократа» є непрямим маркером вживання наркотиків, що можна пояснити властивими наркоманам варіантами ураження легенів або інфекційним ендокарди-том. Проте зміну дистальних фалангів пальців за типом «барабанних паличок» описують у споживачів не тільки внутрішньовенних, але й інгаляційних наркотиків.
«Пальці Гіппократа» реєструють у ВІЛ-інфікованих, причому, у хворих як із ураженими легенями, так і інтактними. У ВІЛ-інфікованих дітей поява «пальців Гіппо-крата» - ймовірна вказівка на легеневий туберкульоз.
Стійке зниження парціального тиску кисню у крові й розвиток тканинної гіпоксемії мають важливе значення у розвитку ГОА. Клінічно цей зв'язок підтверджують не тільки висока частота цієї клінічної ознаки у хворих на хронічні захворювання легенів з дихальною недостатністю, але й неодноразово описана можливість зникнення його після трансплантації легенів (наприклад, у дітей з муко-вісцидозом, коли зміни пальців рук регресували протягом перших 3 місяців після трансплантації легені).
Детальне вивчення патогенезу ГОА при хронічній дихальній недостатності дозволило уточнити деякі меха-нізми її розвитку. Гіпоксія індукує активацію тканинних факторів росту: тромбоцитарного, фактора росту гепато-цитів, судинного фактора росту. Зв'язок росту активності останнього зі зниженням парціального тиску кисню в артеріальній крові вважають найбільш очевидним.
Поряд із цим «пальці Гіппократа» спостерігають при захворюваннях, що безпосередньо не обумовлюють зниження парціального тиску кисню в артеріальній крові й зменшення інтенсивності його транспорту до периферичних тканин.
Патоморфологічним субстратом формування деформа-ції пальців у вигляді барабанних паличок є набряк м'яких тканин, звуження кровоносних судин, проліферація фібро-бластів з розростанням колагенових волокон, зумовлені місцевою тканинною гіпоксією, порушеннями вегетативної іннервації і, можливо, впливом продуктів пухлинних клітин. Кісткова структура нігтьових фалангів змінюється лише у дуже тяжких випадках, коли вони стоншуються, а іноді повністю розсмоктуються (мал. 1). Окістя уражається пере-важно у кінцевих відділах довгих трубчастих кісток (най-частіше передпліч, гомілок), а також п'ясткових, плеснових кісток, основних і середніх фалангів. Періостальні нашару-вання оточують кістку з усіх боків, мають гладеньку або дещо шершаву поверхню й досить швидко осифікуються, а з часом зливаються з діафізом кістки в єдину кісткову масу. У подальшому розвивається сполучнотканинна гіперплазія суглобової капсули з ознаками неспецифічної дегенерації суглобового хряща, а в порожнині суглоба накопичується прозора рідина жовтого кольору.
Розвиток специфічних змін пальців і гіперпластичного процесу окістя обумовлений: токсичним впливом гумораль-ного пухлинного чинника, порушеннями з боку вегетативної нервової системи, аутоімунним процесом, а також – тривалою гіпоксією й тканинною гіпоксемією.
Клінічні особливості паранеопластичної ГОА:
- передує місяці до клінічних проявів раку;
- формування відбувається протягом кількох тижнів/ місяців;
- біль відсутній або наявний різкий біль у кістках кін-цівок (особливо верхніх) самостійний чи при натисканні на уражену кістку при швидкому прогресуванні;
- біль не зникає у стані спокою і під впливом лікування НПЗЗ;
- біль може виникати за відсутності об'єктивних ознак запального процесу в суглобах;
- як правило, періартикулярні тканини запалені, шкіра над ураженим суглобом потовщена, спостерігають набряки й навіть помірний суглобовий випіт;
- частіше до патологічного процесу залучаються симетричні дистальні суглоби кінцівок;
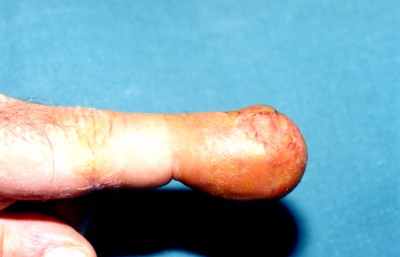
Малюнок 1 - Синдром Марі-Бамбергера (спостереження – Depart-ment of Internal Medicine, Rimini Hospital, Rimini, Italy).
- пальці Гіпократа: деформація пальців обох рук за ти-пом “барабанних паличок”, зміна нігтів – “годинникові скельця” (мал. 2-4);

Малюнок 2 - Симптом годинникових скелець у хворого на рак легень.
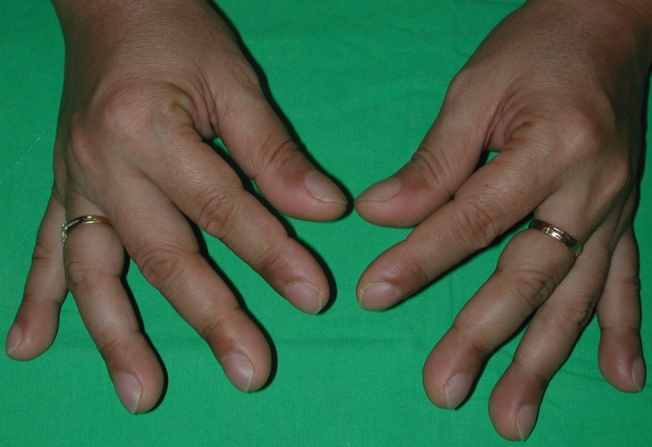
Малюнок 3 – Симптом «барабанних паличок» та «годинникових скелець» у жінки 43-х років хворої на аденокарциному легень (спосте-реження Jenn-Yu Wu, 2008).
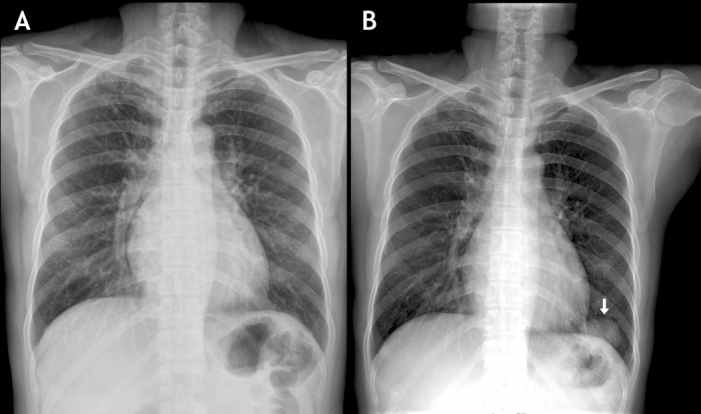
Малюнок 4 – Рентгенограма органів грудної клітки цієї ж пацієнтки з інтервалом 6 місяців (спостереження Jenn-Yu Wu, 2008).
- нейровегетативні зміни: локальна гіперемія шкіри, підвищена ТºС тіла, посилене потовиділення;
- ймовірна патологічна пігментація, фіброзні контрак-тури;
- періостит у ділянці кінцевих відділів довгих трубчас-тих кісток (передпліч, гомілок), що супроводжується осал-гією, артралгією, локальною пальпаторною болючістю.
Рентгенологічні зміни:
- субперіостальна проліферація фалангів п'ясткових і плеснових кісток;
- на рівні довгих кісток періостоз детермінує утворен-ня подвійного діафізарного кортикального шару (симптом «трамвайних рельсів»);
- генералізований остеофітоз чи остеопороз (мал. 5-8).
Синовіальна рідина: прозора, нормальної в’язкості, <1000 клітин в 1 мл, переважають мононуклеари, ревма-тоїдний фактор не визначається.
Диференціальну діагностику при ГОА потрібно проводити із онкологічними і неонкологічними захворюван-нями. Наводимо перелік захворювань, при яких можуть виникати «пальці Гіппократа» - хвороби дихальної системи:
- пухлини легень (бронхогенний рак найчастіше);
- інтерстиціальні захворювання легень (ІФА);
- хронічне обструктивне зхворювання легень;
- муковісцидоз;
- бронхоектатична хвороба;
- професійні ураження легень (азбестоз);
хвороби серцево-судинної системи:
- уроджені вади серця синього типу;
- підгострий інфекційний ендокардит;
хвороби печінки та шлунково-кишкового тракту:
- цироз печінки;
- хвороба Крона;
- неспецифічний виразковий коліт;
- пухлини кишечника;
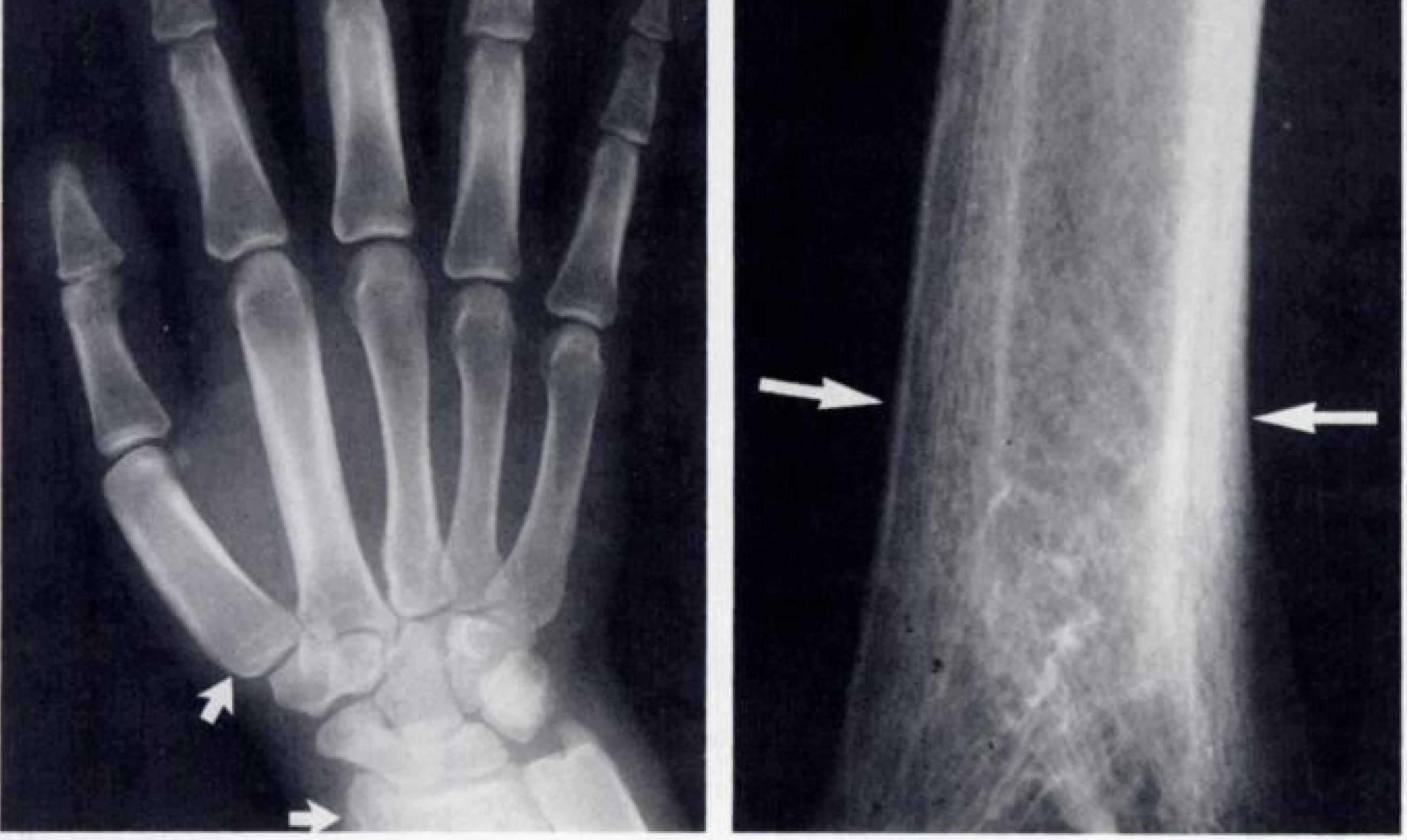
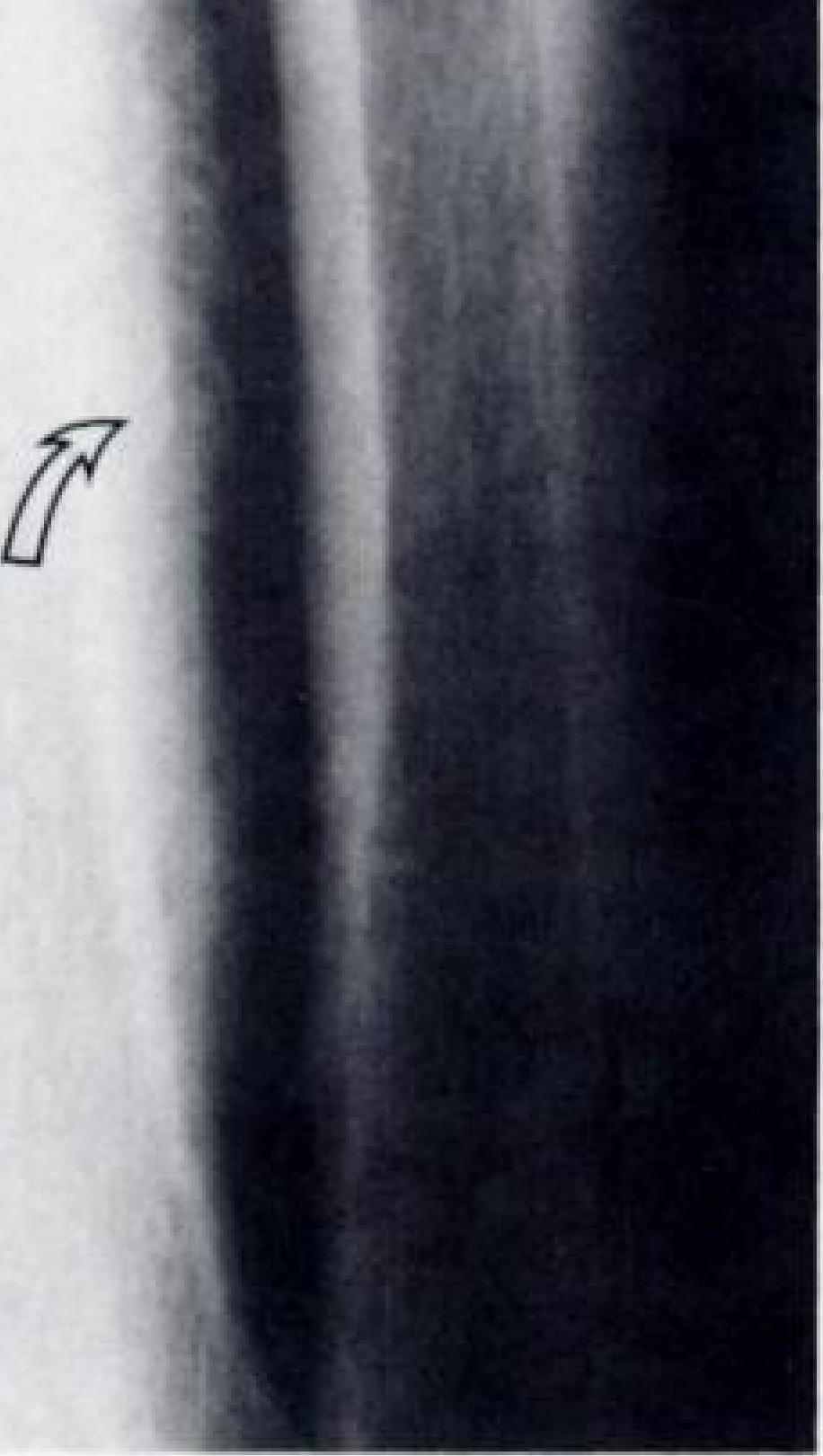

Малюнки 5-8. Рентгенограми при ГОА (спостереження C.J. Pineda, 1987).
хвороби середостіння:
- карцинома стравоходу;
- тимома;
інші:
- сімейна (уроджена) первинна ГОА;
- тривале перебування у високогір'ї;
- хвороба Грейвса, таласемія;
- деякі медикаменти;
- наркоманія;
- СНІД.
При визначенні причини зміни дистальних фалангів пальців рук за типом «барабанних паличок» варто розгля-нути можливість наявності різноманітних захворювань, серед яких основне місце займають захворювання, пов'язані з гіпоксією, що проявляються клінікою серцевої та дихаль-ної недостатності, а також злоякісні пухлини й підгострий інфекційний ендокардит.
Відмінністю синдрому Марі-Бамбергера, що виникає на фоні хронічних неонкологічних захворювань, є те, що характерні зміни пальців рук розвиваються поступово протягом кількох років при відносно задовільному стані хворих і не супроводжуються вираженими артритичними явищами. При ракові легень формування «пальців Гіп-пократа» відбувається протягом кількох тижнів чи місяців з різко вираженим больовим синдромом, причому у деяких хворих воно передує появі клінічних ознак неопластичного процесу та проявляється єдиним паранеопластичним ревма-тичним синдромом. При цьому, окрім ознак основного патологічного процесу (якщо вони мають місце), спосте-рігаються загальнотоксичні явища, наростаюче похудіння, значне підвищення ШОЕ. Після радикального лікування пухлини синдром Марі-Бамбергера протягом кількох місяців зникає.
Деформація нігтьових фалангів за типом барабанних паличок може формуватися як симптом акропатії у хворих з порушенням функції щитоподібної залози, акромегалією, поєднуючись у таких випадках з ураженням кісток (пері-оститами). Тиреоїдна акропатія також може нагадувати ГОА, однак обов'язково поєднується з екзофтальмом. Акро-мегалія, окрім ГОА, характеризується одночасним збільшен-ням розмірів кистей і стоп. Періостити можуть спосте-рігатися за наявності багатьох захворювань: псевдоартриту, хвороби Рейтера, васкуліту, ниркової остеодистрофії та інших, що потрібно враховувати під час проведення дифе-ренціальної діагностики. Барабанні палички регресують піс-ля лікування пухлини, пересадження легенів чи печінки. Здебільшого НПЗЗ, колхіцин малоефективні.
