Конспект лекций для студентов всех специальностей дневной и заочной формы обучения Челябинск
| Вид материала | Конспект |
- Конспект лекций по курсу Начертательная геометрия (для студентов заочной формы обучения, 1032.28kb.
- Краткий конспект лекций Кемерово 2002 удк: 744 (075), 1231.26kb.
- Конспект лекций по курсу "Начертательная геометрия и инженерная графика" Кемерово 2002, 786.75kb.
- Методические указания по подготовке к семинарским занятиям для студентов дневной формы, 1587.03kb.
- Тематический план, рабочая программа и методические рекомендации к семинарским занятиям, 755.58kb.
- Планы семинарских занятий по дисциплине «Экономическая теория» для студентов технических, 527.66kb.
- Конспект лекций для студентов заочной формы обучения по дисциплине " Организация производства", 16.36kb.
- Методические указания для студентов всех специальностей дневной формы обучения Новосибирск, 320.91kb.
- Тематический план, рабочая программа и методические рекомендации к семинарским занятиям, 755.41kb.
- Методические указания к выполнению задания по черчению для студентов всех специальностей, 589.35kb.
Катодную поляризацию можно осуществить путём присоединения защищаемой конструкции к отрицательному полюсу (катоду) внешнего источника тока или к металлу, имеющему меньший электродный потенциал. Положительный полюс подсоединяется к вспомогательному электроду, аноду. В процессе защиты анод активно разрушается и подлежит периодическому обновлению. В качестве материла анода применяют лом чугуна, стали, графита и т.п.
Защитный эффект можно оценить по формулам:
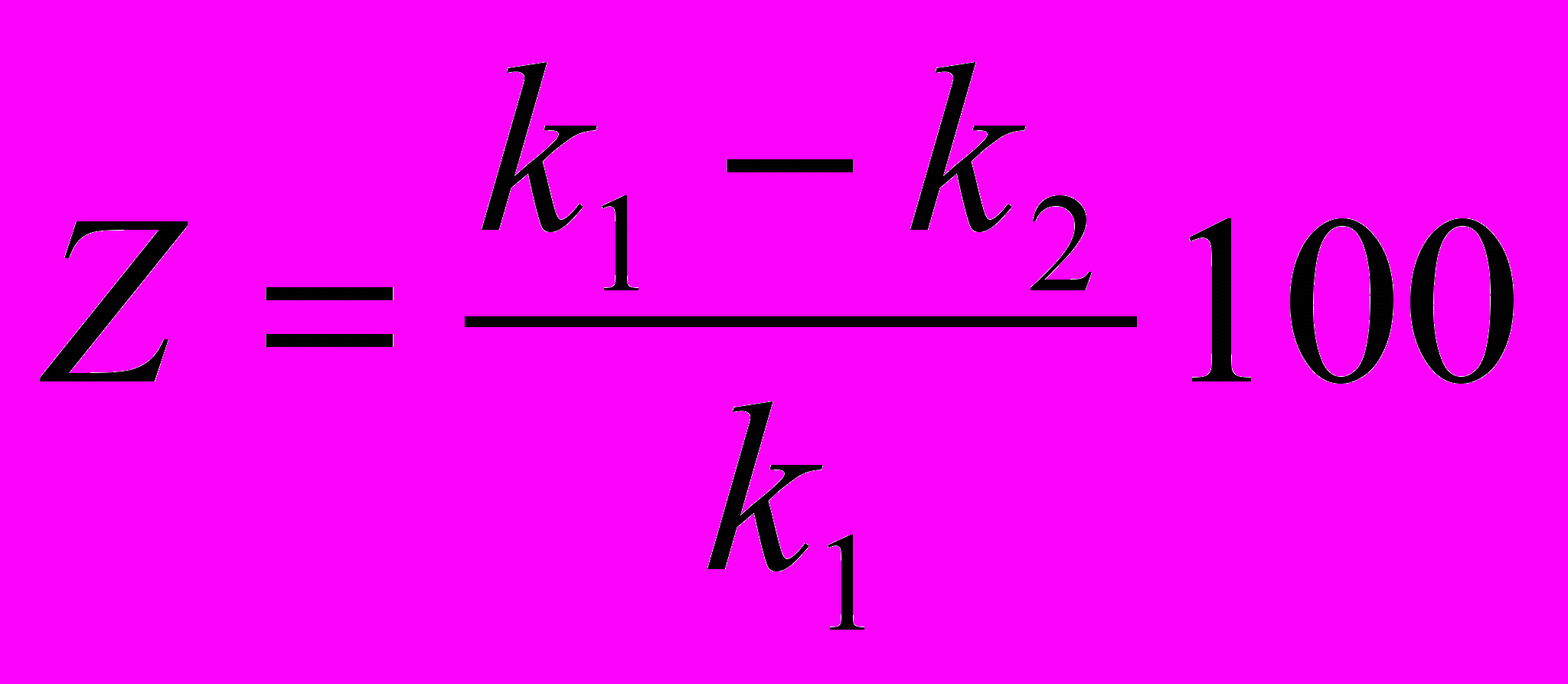 ,
, 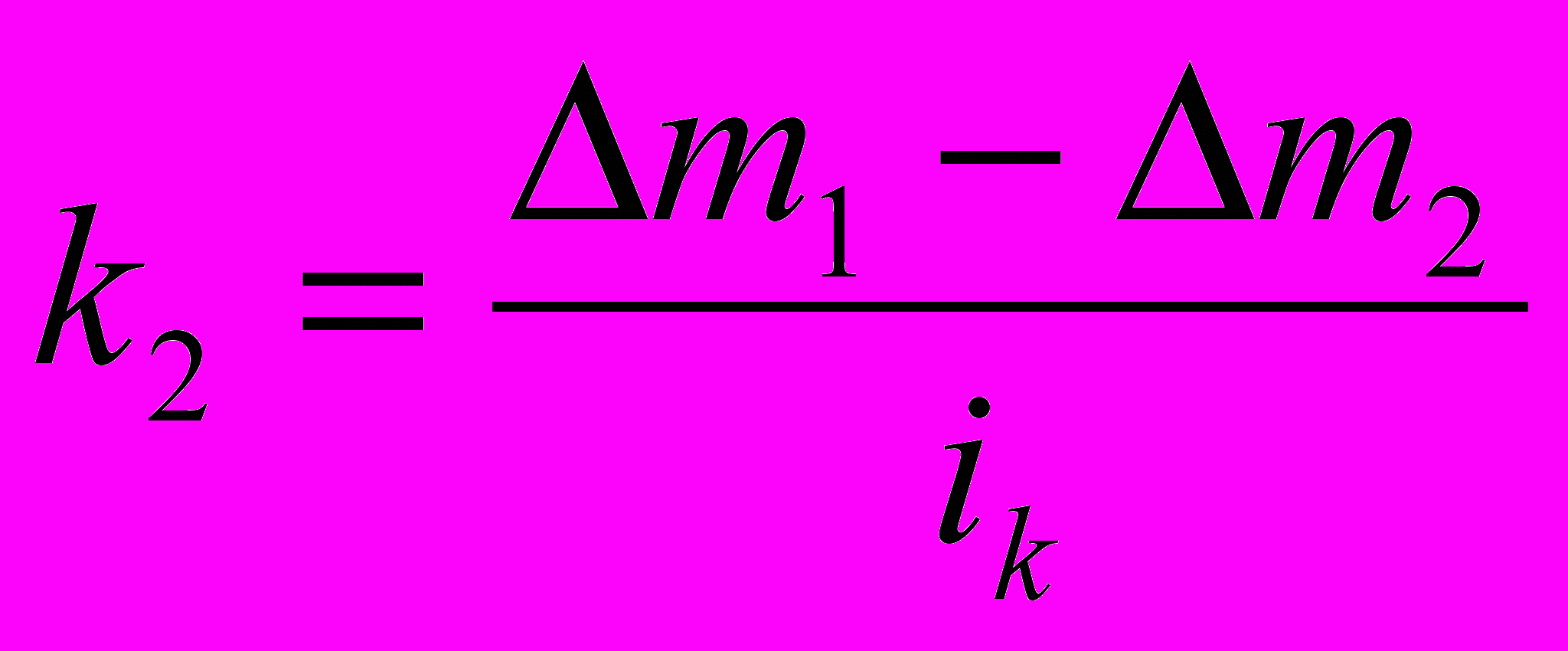 .
.Здесь z – защитный эффект, к1 – показатель скорости коррозии металла без катодной защиты, к2 – при катодной защите, Δm1 – уменьшение массы металла без катодной защиты, Δm2 – при катодной защите, ik – катодная плотность тока.
Протекторная защита. К защищаемой конструкции присоединяют более электроотрицательный металл – протектор, который, растворяясь в окружающей среде, посылает электроны и катодно поляризует конструкцию. После полного растворения протектора или потери контакта его с защищаемой конструкцией протектор необходимо возобновлять. В качестве протектора чаще всего используют сплавы магния и цинка. Алюминий применяется реже, так как он быстро покрывается очень плотной оксидной плёнкой, которая пассивирует его и ограничивает токоотдачу. Протектор работает эффективно, если его переходное сопротивление (между ним и окружающей средой) невелико. В процессе работы протектор может покрываться слоем продуктов коррозии, которые изолируют его от окружающей среды и резко увеличивают переходное сопротивление. Для борьбы с этим протектор помещают в наполнитель (смесь солей), облегчающую растворение продуктов коррозии. Действие протектора ограничивается определенным расстоянием (радиусом действия). В настоящее время протекторную защиту применяют для борьбы с коррозией металлических конструкций в морской и речной воде, грунте и других нейтральных средах. Использование протекторной защиты в кислых средах ограничивается высокой скоростью саморастворения протектора.
Анодная защита. Скорость электрохимической коррозии металла может быть уменьшена и при его анодной поляризации, если она смещает потенциал защищаемого металла в пассивную область.
Метод анодной защиты имеет относительно ограниченное применение, так как пассивация эффективна в основном в окислительных средах при отсутствии активных ионов (например, ионов хлора для железа). Кроме того, анодная защита потенциально опасна: в случае прерывания подачи тока возможно активирование металла и его интенсивное анодное растворение. поэтому анодная защита требует тщательной системы контроля. Защитная плотность тока достаточно низкое и потребление электроэнергии невелико. Другое достоинство анодной защиты – высокая рассеивающая способность, то есть возможность защиты на более удаленном от катода расстоянии и в электрически экранированных участках.
Метод анодной защиты используют для металлов и сплавов, легко пассивирующихся при анодной поляризации; в химической промышленности – для снижения скорости коррозии низкоуглеродистой стали в серной кислоте и в растворах, содержащих аммиак и нитрат аммония.
Защита от коррозии блуждающими токами
Борьба с коррозией блуждающими токами заключается в их уменьшении. Это достигается:
1) Поддержанием в хорошем состоянии контактов между рельсами;
2) Увеличением сопротивления между рельсом и землей (использование шпал, применение щебёночного балласта);
3) Электродренажной защитой. Она обеспечивается путём отвода блуждающих токов от металлического сооружения в сторону их источника. Для этого подземное металлическое сооружение через дренажное устройство соединяется с отрицательной шиной или отсасывающей линией;
4) Применением токоотводов. С этой целью анодные зоны (например, на трубопроводе) с помощью медного проводника соединяют с чугунным ломом (анодом). В результате блуждающие токи вызывают коррозию только этого лома – анода.
Ингибиторы коррозии
Уменьшить коррозию металлической аппаратуры, например, в теплообменных трубках охлаждения дизелей на тепловозах, можно введением в агрессивную среду соединений, значительно снижающих коррозионный процесс. Такой способ снижения скорости коррозии называется ингибированием, а вводимые в среду вещества ингибиторами ил замедлителями коррозии.
Итак, ингибиторы – это такие вещества, введение небольших количеств которых в коррозионную среду, упаковочные средства и во временные защитные покрытия снижает скорость коррозии и уменьшает ее вредные последствия. Защитное действие ингибиторов связано с изменением в состоянии поверхности защищаемого металла и в кинетике реакций, лежащих в основе коррозионного процесса.
Скорость коррозии благодаря введению ингибитора может быть снижена в любое желаемое число раз, а степень защиты доведена почти до 100%. Эффективность ингибитора определяется как его природой, так и природой корродирующего металла, и зависит от температуры.
Ингибиторы коррозии можно классифицировать по различным признакам.
- По составу их подразделяют на две группы: неорганические и органические. В последнее время широко применяют метало- и кремнийорганические ингибиторы.
- По областям применения ингибиторы бывают: кислотной коррозии, щелочной коррозии и коррозии в нейтральных средах.
- По условиям применения – существуют низкотемпературные и высокотемпературные ингибиторы.
- По особенностям механизма действия ингибиторов бывают адсорбционные и ингибиторы пассивирующего действия.
Ингибиторы коррозии пассивирующего действия для нейтральных сред делятся на:
- Ингибиторы окислительного типа, которые проявляют своё действие и в отсутствие кислорода воздуха. Примеры: нитрит натрия NaNO2, нитрит аммония NH4NO2, хромат калия K2CrO4, дихромат калия K2Cr2O7, молибдат натрия Na2MoO4 и др.
- Ингибиторы, не обладающие окислительными свойствами, которые для проявления своего действия нуждаются в кислороде воздуха. Примеры: гидроксид аммония NH4NO3, гидроксид натрия NaOH, карбонат натрия Na2CO3, силикат, ортофосфат и тетраборат натрия Na2SiO3 , Na3PO4 и Na2B4O7.
Ингибиторы пассивирующего действия в нейтральных средах окислительного типа при отсутствии хлоридов и сульфатов по отношению к низкоуглеродистым сталям обладают примерно в сто раз большей эффективностью, чем ингибиторы, не обладающие окислительными свойствами. Наименьшая защитная концентрация ингибиторов–окислителей составляет 10–3 10–4 %, а ингибиторов, не обладающих окислительными свойствами – 0,1 0,05%. Ингибиторы коррозии могут вводиться в жидкие среды любой кислотности и в твёрдые материалы: масла, топлива, различные органические жидкости, лакокрасочные, полимерные, фосфатные, оксидные и другие покрытия, а также в упаковочные материалы. Наиболее перспективным является внесение в упаковочные материалы летучих ингибиторов (бензоат аммония, бензоат триэтаноламина, уротропин в смеси с нитритом натрия, нитрит дициклогексиламмония), которые, испаряясь в атмосферу внутри упаковки и адсорбируясь на поверхности металла, переводят его в пассивное состояние.
Замедление скорости коррозии связано прежде всего с исключением из коррозионного процесса части поверхности из-за её экранирования ингибитором. При выборе ингибиторов следует исходить не только из того, как они уменьшают скорость перехода металла в окружающую среду, но и из того, как они влияют на металлические свойства. Поверхностно-активные органические вещества (ПАОВ) с преобладающей катионной функцией более предпочтительны, чем с анионной функцией. Применение подобранных ингибиторов может не только предотвратить растворение металла, но и улучшить его механические свойства.
Защитное действие пассивирующих ингибиторов основано на смещении потенциала металла в положительную сторону и переводе его в пассивное состояние. Такой эффект может быть достигнут различными путями, но во всех случаях причиной снижения скорости коррозии является образование поверхностного защитного слоя. Ингибиторы могут непосредственно участвовать в образовании этого слоя.
Ингибиторы кислотной коррозии применяют при травлении изделий из черных и цветных металлов для удаления с их поверхности окалины и ржавчины, кислотной промывке теплосилового оборудования, при производстве кислот.
Действие ингибиторов атмосферной коррозии так же, как и других типов ингибиторов, сводится прежде всего к изменению ими кинетики электрохимических реакций, лежащих в основе коррозии. Эффективность любых ингибиторов зависит от их концентрации в коррозионной среде, и при некоторых минимальных значениях падает до нуля. Объем окружающей нас воздушной атмосферы практически безграничен и содержание в ней защитной концентрации ингибитора представляется экономически бессмысленно. применение ингибиторов для защиты металлов от атмосферной коррозии возможно поэтому лишь в том случае, если удается ограничить пространство, в которое помещается защищаемый объект, и отделить его от остальной атмосферы. Для этого ингибиторы вводят в смазки, полимерные и другие покрытия; помещают металл в упаковочный материал с внесением ингибитора в свободное пространство между упаковочным материалом и металлическим изделием, или в сам упаковочный материал (например, бумагу).
ЛЕКЦИЯ ПО ТЕМЕ: «Полимеры»
План
1. Методы получения полимеров
2. Строение полимеров
3. Свойства полимеров
4. Применение полимеров
Полимеры – высокомолекулярные соединения, которые характеризуются молекулярной массой от нескольких тысяч до нескольких миллионов. Молекулы полимеров (макромолекулы) состоят из большого числа повторяющихся звеньев. Отдельную группу соединений составляют олигомеры, которые по значению молекулярной массы занимают промежуточное положение между низкомолекулярными и высокомолекулярными соединениями. Различают неорганические, органические и элементоорганические полимеры. Органические полимеры в свою очередь подразделяют на природные и синтетические.
Методы получения полимеров
Полимеры получают методами полимеризации и поликонденсации.
Полимеризация – это реакция образования полимеров путём последовательного присоединения молекул низкомолекулярного вещества (мономера). При полимеризации не образуются побочные продукты и соответственно элементный состав макромолекул не отличается от состава молекул мономеров. В качестве мономеров используют соединения с кратными связями: С≡С, С≡N, C=C, C=O, C=N, либо соединения с циклическими группировками, способными раскрываться. В процессе полимеризации происходит разрыв кратных связей или раскрытие циклов у мономеров и возникновение химических связей между группами с образованием макромолекул, например:
n СН2=СН2 → (–СН2–СН2–)n ; n СН2=СН(С6Н5) → (–СН2–СН(С6Н5)–)n
Этилен Полиэтилен Стирол Полистирол
n
 RC≡N → (–C(R)=N–)n ; n CH2=CCH3COOCH3 → (–CH2–C(CH3)–)n
RC≡N → (–C(R)=N–)n ; n CH2=CCH3COOCH3 → (–CH2–C(CH3)–)n н
 итрил полинитрил COOCH3
итрил полинитрил COOCH3метилметакрилат полиметилметакрилат
n

 CH2–CH2 → (–CH2–CH2O–)n ; n CH≡CH → (–CH=CH–)n
CH2–CH2 → (–CH2–CH2O–)n ; n CH≡CH → (–CH=CH–)n O ацетилен полиацетилен
Этиленоксид полиэтиленоксид
n CH2=CHCH=CH2 → (–CH2–CH=CH–CH2–)n
бутадиен полибутадиен
По числу участвующих мономеров различают гомополимеризацию (один вид мономера) и сополимеризацию (два и более видов мономеров). Полимеризация – самопроизвольный экзотермический процесс (ΔG<0, ΔH<0), так как разрыв двойных связей или циклов с образованием одинарных связей ведет к уменьшению энергии системы. Однако без внешнего воздействия (инициаторов, катализаторов, нагревания или облучения) полимеризация если и протекает, то очень медленно. Полимеризация является цепной реакцией. В зависимости от характера активных частиц различают радикальную и ионную полимеризацию.
При радикальной полимеризации процесс инициируется свободными радикалами и проходит через несколько стадий: инициирование, рост цепи, передача или обрыв цепи. Радикальная полимеризация служит промышленным способом синтеза таких полимеров, как поливинилхлорид (-СН-СНСl-)n, поливинилацетат (-СН2-СН(ОСОСН3)-)n, полистирол (-СН2-СН(С6Н5)-)n, полиакрилат (-СН2-СН(СН3)(СООR)-)n, полиэтилен (-СН2-СН2-)n, полидиены (-СН2-СR=CH-CH2-)n и различных сополимеров.
Ионная полимеризация также проходит через стадию образования активных центров, роста и обрыва цепи. Роль активных центров играют катионы и анионы и соответственно различают катионную и анионную полимеризацию. Метод ионной полимеризации используют в производстве полиизобутилена (-СН2-С(СН3)2-)n, полиформальдегида (-СН2О-)n, полиамидов, например, поликапроамида (капрона) (-NH-(CH2)5-CO-)n, синтетических каучуков, например, бутадиенового каучука (-СН2-СН=СН-СН2-)n. Методом полимеризации получают ¾ всего объёма выпускаемых полимеров. Полимеризацию проводят в массе, растворе, эмульсии, суспензии или в газовой фазе.
Полимеризация в массе (блоке) – это полимеризация жидкого мономера в неразбавленном состоянии, при этом получают достаточно чистый мономер. Эмульсионная полимеризация (в эмульсии) происходит при полимеризации мономера, диспергированного в воде, в присутствии ПАВ для стабилизации эмульсии. Достоинство способа – лёгкость отвода теплоты, возможность получения полимеров с большой молекулярной массой, высокая скорость реакции; недостаток – необходимость отмывки полимера от эмульгатора. Способ применяется в промышленности для получения каучуков, полистирола, поливинилхлорида, поливинилацетата, полиметилметакрилата и других полимеров.
При полимеризации в суспензии полимер находится в виде капель, диспергированных в воде или другой жидкости. В результате реакции образуются полимерные гранулы размером от 10-6 до 10-3 м. При газовой полимеризации мономер находится в газовой фазе, а полимерные продукты – в жидком или твёрдом состоянии. Метод применяют для получения полипропилена и других полимеров.
Поликонденсация – это реакция синтеза полимера из соединений, имеющих две или более функциональные группы, сопровождающаяся образованием побочных низкомолекулярных продуктов (воды, аммиака, хлороводорода и др.). Поэтому элементные составы полимеров и исходных веществ не совпадают. Этим поликонденсация отличается от полимеризации. Поликонденсация протекает по ступенчатому механизму, при этом промежуточные продукты являются стабильными, то есть поликонденсация может остановиться на любой стадии. Образующиеся низкомолекулярные продукты реакции могут взаимодействовать с промежуточными продуктами поликонденсации, вызывая их расщепление (гидролиз, аминолиз, ацидолиз и т.д.).
Поликонденсацию проводят либо в расплаве, либо в растворе, либо на межфазной границе. Методом поликонденсации получают примерно ¼ часть выпускаемых полимеров, например, поликапроамид (капрон), полигексаметиленадипинамид (найлон) (-NH(CH2)6-NHCO(CH2)4CO-)n, полиэфиры - полиэтилентерефталат (-ОСС6Н4(СО)ОСН2СН2-)n, полиуретаны (-OROCONHR/NHCO-)n, полисилоксаны (-SiR2-O-)n, полиацетали (-OROCHR/-)n, фенолформальдегидные смолы (-C6H3OH-CH2-)n, мочевиноформальдегидные смолы и другие.
Строение полимеров
Форма и структура макромолекул
Макромолекулы могут быть линейными, разветвленными и сетчатыми. Линейные полимеры образуются при полимеризации мономеров или линейной поликонденсации. Разветвлённые полимеры могут образоваться как при полимеризации, так и при поликонденсации. Сетчатые полимеры образуются в результате сшивки цепей при вулканизации, образовании термореактивных смол и так далее. Форма макромолекул влияет на структуру и свойства полимеров.
Линейные и разветвлённые макромолекулы из-за способности атомов и групп атомов вращаться вокруг одинарных связей постоянно изменяют свою пространственную форму, или, другими словами, имеют много конформационных структур. Это свойство обеспечивает гибкость макромолекул, которые могут изгибаться, скручиваться, распрямляться. Поэтому для линейных и разветвленных полимеров характерно высокоэластичное состояние, то есть способность к обратимой деформации под действием относительно небольших внешних сил. Они также обладают термопластичными свойствами, то есть способны размягчаться при нагревании и затвердевать при охлаждении без химических превращений. При разветвлении полимеров эластические термопластичные свойства уменьшаются. При образовании сетчатой структуры термопластичность теряется.
Кристаллическое состояние полимеров.
Некоторые полимеры в определенных условиях могут иметь кристаллическую структуру. Способны кристаллизоваться только стереорегулярные полимеры. Процесс кристаллизации протекает через несколько стадий. 1 стадия – возникновение пачек – ассоциатов упорядоченно расположенных молекул. Из пачек образуются фибриллы и сферолиты. Фибриллы представляют собой агрегаты пачек продолговатой формы, а сферолиты – игольчатые образования, радиально расходящиеся из одного центра. Наконец, из фибрилл и сферолитов образуются единичные кристаллы. Между кристаллами находятся участки с неупорядоченной структурой (аморфные области). Поэтому такие полимеры характеризуются определенной степенью кристалличности, например, степень кристалличности полиэтилена может достигать 80%.
Физическое состояние аморфных полимеров
Аморфные полимеры находятся в стеклообразном, высокоэластичном и вязкотекучем состояниях. Для определения температурных границ существования этих состояний изучают зависимость деформации полимера от температуры, на основании которой строят термохимическую кривую.
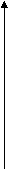 Деформация
ДеформацияТермомеханическая кривая полимеров



I II III

 Тст Тт Тр температура
Тст Тт Тр температураПри низкой температуре полимер находится в стеклообразном состоянии (область I), в котором полимер ведёт себя как упругое твёрдое тело. При повышении температуры полимер переходит в высокоэластичное состояние, свойственное высокомолекулярным соединениям (область II). Высокоэластичное состояние проявляется в интервале температур от Тст (температуры стеклования) до Тт (температуры текучести). Если температурный интервал Тст–Тт достаточно широк и захватывает обычные температуры, то такие полимеры называют эластиками или эластомерами, или каучуками. Полимеры с узким интервалом температур Тст–Тт, смещенным в область повышенных температур, называют пластиками или пластомерами. При обычных температурах пластики находятся в стеклообразном состоянии. При температуре выше Тт (область III) полимер переходит в вязкотекучее состояние. Повышение температуры выше Тр ведет к деструкции, разрушению полимера. вещество в вязкотекучем состоянии под действием напряжений сдвига течёт как вязкая жидкость, причём деформация полимера является необратимой (пластической).
Свойства полимеров
Химические свойства полимеров зависят от состава, молекулярной массы и структуры. Полимерам свойственны реакции соединения макромолекул поперечными связями, взаимодействие функциональных групп друг с другом и низкомолекулярными веществами, деструкция. Наличие у макромолекул двойных связей и функциональных групп обуславливает повышение реакционной способности полимеров.
Вследствие наличия двойных связей и функциональных групп отдельные макромолекулы могут сшиваться поперечными связями, например, при вулканизации каучука происходит переход линейных макромолекул в сетчатую структуру резины (0,5-5% серы) или эбонита (более 20% серы).
К реакциям взаимодействия функциональных групп с низкомолекулярными веществами относятся галогенирование полиолефинов, гидролиз полиакрилатов и др. Полимеры могут подвергаться деструкции, то есть разрушению под действием кислорода, света, теплоты и радиации. В результате деструкции уменьшается молекулярная масса макромолекул, изменяются физические и химические свойства. Процесс ухудшения свойств полимеров во времени в результате деструкции называется старением и в конце концов полимеры становятся непригодными для дальнейшего применения. Для замедления деструкции вводят стабилизаторы, чаще всего антиоксиданты, то есть ингибиторы реакции окисления (фосфиты, фенолы, ароматические амины).
Механические свойства полимеров
Они определяются элементным составом, молекулярной массой, структурой и физическим состоянием макромолекулы.
Механическая прочность полимеров возрастает с увеличением их молекулярной массы, при переходе от линейных к разветвленным и далее к сетчатым структурам. Стереорегулярные структуры имеют более высокую прочность, чем полимеры с разупорядоченной структурой. Дальнейшее увеличение механической прочности полимеров наблюдается при их переходе в кристаллическое состояние. Механическая прочность может быть также повышена путём добавления наполнителей, например, сажи и мела, армированием волокнами (например, стекловолокном).
Электрические свойства полимеров
По этим свойствам все вещества подразделяются на диэлектрики, полупроводники и проводники.
Диэлектрики имеют очень низкую проводимость (σ<10-8 Ом-1см-1), которая увеличивается с повышением температуры. Большинство полимеров относится к диэлектрикам. Однако их диэлектрические свойства лежат в широких пределах и зависят от состава и структуры макромолекул, в значительной степени определяются наличием, характером и концентрацией полярных групп в макромолекулах. Наличие галогенных, гидроксильных карбоксидных и других полярных групп ухудшают диэлектрические свойства полимеров. Поэтому хорошими диэлектриками являются полимеры, не имеющие полярных групп, такие, как фторопласт, полиэтилен, полиизобутилен, полистирол. С увеличением молекулярной массы полимера улучшаются его диэлектрические свойства. При переходе к стеклообразному к высокоэластичному и вязкотекучему состояниям возрастает удельная электрическая проводимость.
Некоторые функциональные группы, например, гидроксильные, обуславливают гидрофильность полимеров. Такие полимеры поглощают воду, которая приводит к повышению электрической проводимости. Поэтому гидроксильные группы связывают между собой или с другими группами реакциями конденсации. Полимерные диэлектрики широко используют в электро- и радиотехнике как материалы различных электротехнических изделий, защитных покрытий кабелей, проводов, изоляционных эмалей и лаков.
К органическим полупроводникам относят вещества, электрическая проводимость которых лежит в пределах 10-10–10-3 Ом-1см-1. Электрическая проводимость полупроводников возрастает с увеличением температуры и при воздействии света. Некоторые полимеры с системой сопряженных двойных связей обладают полупроводниковыми свойствами, которые обусловлены наличием нелокализованных π-электронов сопряженных двойных связей. Примеры органических полупроводников: полиацетилен (-СН2=СН2-)n, поливинилены (-СН=СR-)n, полинитрилы (-N=CR-)n и другие. Электрическая проводимость может резко возрастать при химическом или электрохимическом окислении или восстановлении некоторых полимеров, например, полиацетилена, полианилина (-C6H3NH2-)n, полипиролла (-C4H3N-)n, других. При электрохимическом окислении в состав полимера внедряются анионы, например, ClO4–, при восстановлении – катионы (например, Li+). Такие органические полупроводники применяют в качестве электродных материалов аккумуляторов, пластин конденсаторов, материалов сенсоров, а в перспективе и для замены металлов (органические металлы).
Смесь некоторых полимеров, находящихся в аморфном состоянии, например, полиэтиленоксида (-СН2-СН2-О-)n с солями металлов, например,
LiClO4, обладает ионной проводимостью. Такие твёрдые электролиты могут получить применение в аккумуляторах.
Применение полимеров
На основе полимеров получают следующие материалы: волокна, плёнки, резины, лаки, клеи, пластмассы, композитные материалы (композиты).
Волокна получают путём продавливания растворов или расплавов полимеров через тонкие отверстия (фильеры) в пластине с последующим затвердеванием. К волокнообразующим полимерам относятся полиамиды, полиакрилонитрилы и другие.
Полимерные плёнки из расплавов полимеров используют в качестве электроизоляционного и упаковочного материала, основы магнитных лент и так далее.
Лаки – растворы плёнкообразующих веществ в органических растворителях. Кроме полимеров, лаки содержат вещества, повышающие пластичность (пластификаторы), растворимые красители, отвердители и др. Применяются для электроизоляционных покрытий, в качестве основы грунтовочного материала и лакокрасочных эмалей.
Клеи – композиции, способные соединять различные материалы за счёт образования прочных связей между поверхностями и клеевой прослойкой. Клеи подразделяют на термопластические, термореактивные и резиновые. В качестве полимерной основы термореактивных клеев служат фенол- и мочевиноформальдегидные и эпоксидные смолы, полиуретаны, полиэфиры и др., термопластичных – полиакрилы, полиамиды, поливинилацетали, поливинилхлорид и другие полимеры.
Пластмассы – это материалы, содержащие полимер, который при формировании изделия находится в вязкотекучем состоянии, а при его эксплуатации – в стеклообразном. Они подразделяются на термопласты и реактопласты. При формовании реактопластов происходит необратимая реакция отвердевания, к ним относятся материалы на основе фенолформальдегидных, мочевиноформальдегидных, эпоксидных и других смол. Термопласты способны многократно переходить в вязкотекучее состояние при нагревании, и стеклообразное – при охлаждении. К ним относятся материалы на основе полиэтилена, полипропилена, политетрафторэтилена, поливинилхлорида, полистирола и др. Кроме полимеров, в состав пластмасс входят пластификаторы (диоктилфталат, дибутилсебацинат, хлорированный парафин), снижающие температуру стеклования и повышающие текучесть полимеров; красители и наполнители (графит, сажа, мел, металл, бумага, ткань и др.), улучшающие физико-механические свойства полимеров.
Композиты – состоят из основы (органической, полимерной, углеродной, керамической, металлической), армированной наполнителем (высокопрочными волокнами или нитевидными кристаллами). Армирующие наполнители в значительной степени определяют механические, теплофизические и электрические свойства композитов. Композиты на основе полимеров используются как конструкционные, электро- и теплоизоляционные, коррозионностойкие, антифрикционные материалы в автомобильной, станкостроительной, электротехнической, авиационной, радиотехнической, горнорудной промышленности, космической технике, химическом машиностроении и строительстве.
В настоящее время широко применяется большое число различных полимеров. Физические и химические свойства некоторых термопластов приведены в таблице 14.2 и 14.3 [1].
ЛЕКЦИЯ ПО ТЕМЕ: «Методы химической идентификации веществ»
План
1. Единицы количества вещества: моль, молярная масса, молярный объём.
2. Способы выражения концентрации: массовая, молярная, мольная, нормальная.
3. Химическая идентификация веществ: качественный и количественный анализ, аналитический сигнал, инструментальные методы анализа; химический анализ
Единицы количества вещества
Количество вещества – это число структурных элементов (атомов, молекул, ионов) в системе. Единицей измерения вещества является моль, то есть количество вещества в системе, которое содержит столько определенных структурных элементов (молекул, атомов, ионов, электронов и др.), сколько атомов содержится в 0,012 кг углерода-12. Используя термин «моль», следует указывать частицы, к которым он относится: «моль молекул», «моль атомов», «моль электронов» и т.д. Масса одного моля вещества называется молярной массой М с единицей измерения кг/моль или г/моль. Моль любого газа при нормальных условиях (0оС и 1.033˙105 Па) занимает объём 22,416 л. Этот объём называется молярным.
Способы выражения концентрации приведены в главе «Растворы» [1].
Химическая идентификация веществ
Химическая идентификация (качественный анализ) и измерение (количественный анализ) являются предметом аналитической химии.
Химическая идентификация (обнаружение) – это установление вида и состояния фаз, молекул, атомов, ионов и других составных частей вещества на основе сопоставления экспериментальных и соответствующих справочных данных для известных веществ. Идентификация является целью качественного анализа. При идентификации обычно определяют комплекс свойств веществ: цвет, фазовое состояние, плотность, вязкость, температуры плавления и кипения, фазового перехода; растворимость, электродный потенциал, энергию ионизации и (или) другие. При анализе многокомпонентных систем используют универсальные приборы (спектрометры, спектрофотометры, хроматографы, полярографы и др.), снабженные компьютерами, в памяти которых имеется справочная химико-аналитическая информация. На базе этих универсальных установок создается автоматизированная система анализа и обработки информации.
В зависимости от вида определяемых частиц различают элементный, молекулярный, изотопный и фазовый анализы. Чаще используют первые два вида анализа.
В зависимости от массы сухого вещества или объёма раствора анализируемых веществ различают макрометод (0,5-10 г или 10-100 мл), полумикрометод (10-50 мг или 1-5 мл), микрометод (1-5 мг или 0,1-0,5 мл) и ультрамикрометод (ниже 1 мг или 0,1 мл) идентификации.
Качественный анализ характеризуют пределом обнаружения сухого вещества, т есть минимальным количеством надёжно идентифицируемого вещества, и предельной концентрацией раствора Сх, min. Эти две величины связаны:
