Сердечно-сосудистая патология у пациентов с алкогольной болезнью: проспективное исследование 14. 01. 05 кардиология
| Вид материала | Исследование |
- Расписание лекций по патологической физиологии на VI семестр 2011 2012 учебного года, 13.37kb.
- Отдаленные результаты хирургического лечения и качество жизни больных, оперированных, 305.19kb.
- Исследование eurika (Эпидемиологическое исследование среди пациентов с риском сердечно-сосудистых, 51.36kb.
- Оптимизация диагностической и лечебной тактики у больных с ангиодисплазиями 14. 00., 872.41kb.
- Клинико-социальные особенности больных с сердечно-сосудистыми заболеваниями и оптимизация, 500.91kb.
- Артериальная гипертония и атеросклероз сонных артерий: особенности диагностики, течения,, 282.52kb.
- Керимович хроническая сердечная недостаточность у больных ишемической болезнью сердца:, 509.58kb.
- Лекция 1: «Болезни сердечно-сосудистой системы», 581kb.
- А. Н. Бакулева на правах рукописи Какучая Теа Тамазовна «Результаты применения клеточных, 619.24kb.
- Вегетативно сосудистая дистония, 53.17kb.
1 2
На правах рукописи
Аксельрод Анна Сергеевна
Сердечно-сосудистая патология у пациентов с алкогольной болезнью:
проспективное исследование
14.01.05 – кардиология
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
доктора медицинских наук
Москва 2012
Работа выполнена в Первом Московском государственном
медицинском университете имени И.М. Сеченова
Научный консультант:
доктор медицинских наук, профессор Абрам Львович СЫРКИН
Официальные оппоненты:
доктор медицинских наук, профессор Жанна Михайловна СИЗОВА
доктор медицинских наук, профессор Борис Яковлевич БАРТ
доктор медицинских наук, профессор Давид Меерович АРОНОВ
Ведущее учреждение:
Научный центр сердечно-сосудистой хирургии им. А.Н. Бакулева РАМН
Защита диссертации состоится «____»______________2012 г. в _______ч. на заседании диссертационного совета Д 208.040.05 при Первом Московском государственном медицинском университете имени И.М. Сеченова (119991, г. Москва, ул. Трубецкая, д.8, стр.2).
С диссертацией можно ознакомиться в ГЦНБ ГОУ ВПО Первый Московский государственный медицинский университет имени И.М. Сеченова (117998, Москва, Нахимовский пр-т, д.49).
Автореферат разослан «____»____________2012 г.
Ученый секретарь диссертационного совета,
Доктор медицинских наук, профессор Елена Васильевна ВОЛЧКОВА
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы.
В течение последних 10 лет в отечественной и зарубежной литературе имеются многочисленные публикации о жизнеугрожающих симптомах поражения сердечно-сосудистой системы у пациентов с алкогольной болезнью (АБ). Анализ сердечно-сосудистой смертности и потребления алкоголя в России за период 1980-2007 гг., представленный в докладе Общественной палаты Российской Федерации в 2009 г., показал, что общая смертность, связанная с алкоголем, составляет 426,0 тысяч случаев в год (23.4% всех смертей). При этом самый высокий вклад в общую смертность вносят сердечно-сосудистые заболевания – 194,4 тыс. в год (19.4% в общей сердечно-сосудистой смертности). Высокий риск сердечно-сосудистой смертности этих больных связан с неконтролируемыми подъемами артериального давления (АД), пароксизмальными желудочковыми нарушениями сердечного ритма и прогрессированием явлений сердечной недостаточности на фоне алкогольной (дилатационной) кардиомиопатии.
Однако по-прежнему немногочисленными остаются наблюдения пациентов, полностью прекративших употреблять алкоголь. Такие больные составляют не более 20% среди всех пациентов с АБ, при этом ремиссия заболевания редко длится более 3 лет.
Можно с уверенностью сказать, что среди всех пациентов с АБ, прекративших употреблять алкоголь, чаще всего в поле зрения кардиолога попадают лишь пациенты с тяжелой дилатационной кардиомиопатией. Несколько реже к кардиологу обращаются больные с АГ, которая, как правило, не связывается врачом с алкогольной зависимостью. Оба обращения происходят обычно уже после выписки пациента из наркологического стационара.
Кроме того, существующие на сегодняшний день медико-экономические стандарты по обязательному медицинскому страхованию не позволяют произвести пациентам с АБ детальное кардиологическое обследование во время пребывания в наркологическом стационаре. Таким образом, пароксизмальные нарушения сердечного ритма (например, пароксизмальная желудочковая тахикардия) часто остаются не выявленными, поскольку в наркологическом стационаре не проводится суточное мониторирование ЭКГ. Суточное мониторирование АД в наркологическом стационаре также не проводится, поэтому нередко незамеченными остаются подъемы и резкие снижения АД в ночные часы.
Стоит отметить, что пациенты с АБ значительно различаются по степени выраженности симптомов поражения сердечно-сосудистой системы как во время алкогольного абстинентного синдрома (ААС, первые 72 часа после прекращения употребления алкоголя), так и в раннем (первый месяц после прекращения употребления алкоголя) и позднем постабстинентном периоде (ПАП). Например, на 5-7 сутки после прекращения употребления алкоголя у этих больных можно увидеть как очень высокие (до 220/120 мм рт.ст.), так и умеренные (до 150-160/90-100 мм рт.ст.) подъемы АД. Синусовая тахикардия может быть выраженной (средняя ЧСС около 110 в минуту по данным холтеровского мониторирования) или, напротив, умеренной (средняя ЧСС нередко не превышает 90 в минуту). Среди пациентов с АБ встречаются лица с частой (тысячи) симптомной одиночной и групповой суправентрикулярной и желудочковой экстрасистолией, симптомными пароксизмальными суправентрикулярными (фибрилляция и трепетание предсердий, пароксизмальная суправентрикулярная тахикардия) и симптомными желудочковыми (желудочковая тахикардия) нарушениями ритма.
На сегодняшний день причины клинического полиморфизма кардиальных симптомов остаются неясными. Лиц с высоким риском осложненного течения сердечно-сосудистой патологии можно увидеть как среди пациентов молодого возраста с алкогольным анамнезом 5-7 лет, так и среди пациентов старше 50 лет с длительным употреблением алкоголя. В литературе имеются результаты немногочисленных исследований, из которых очевидно, что описанные клинические различия не могут быть объяснены ни возрастом больных, ни длительностью алкогольного анамнеза.
Дальнейшее длительное динамическое наблюдение таких больных кардиологом является сложной проблемой в силу разных причин.
Во-первых, для пациентов с АБ, как продолжающих употреблять алкоголь, так и прекративших его употребление, характерна низкая приверженность к лечению, что является основной причиной отсутствия стандартов и практических рекомендаций по инструментальному обследованию и кардиальной терапии этих больных.
Во всех опубликованных на сегодняшний день исследованиях и монографиях не предлагается четкий алгоритм диагностического кардиологического обследования этих больных, не анализируются варианты наиболее эффективной гипотензивной и антиаритмической терапии.
Имеются публикации об анализе взаимосвязи АГ с генетическим полиморфизмом ферментов, метаболизирующих алкоголь -алкогольдегидрогеназы 2 и альдегиддегидрогеназы [В.С. Моисеев, П.П. Огурцов, Ж.Д. Кобалава, Н.С. Овчинникова и др., 2005]. При этом авторами были получены достоверные различия АД и ЧСС, позволяющие предположить взаимосвязь генетического полиморфизма этих ферментов и выраженности АГ во время ААС. Однако на сегодняшний день отсутствует информация о вариантах генетического полиморфизма систем a- и b-адренорецепции, рецепторов дофамина и системы ингибиторов АПФ, которые также являются важными и доказанными звеньями патогенеза АГ и нарушений сердечного ритма у пациентов с АБ. Изучение генетического полиморфизма этих систем внесло бы большую ясность в представления о патогенезе поражения сердечно-сосудистой системы этих больных, и, следовательно, могло бы оптимизировать подбор эффективной кардиальной терапии при их дальнейшем наблюдении.
Таким образом, в настоящее время проспективное кардиологическое исследование пациентов с АБ, прекративших употреблять алкоголь, является необходимым и актуальным, поскольку в литературе отсутствуют практически рекомендации и стандарты кардиологического обследования и терапии пациентов с АБ.
Целью настоящего исследования явилось комплексное кардиологическое обследование и подбор кардиотропной терапии у пациентов с АБ в течение 3 лет после прекращения употребления алкоголя.
Для достижения данной цели были поставлены следующие задачи:
- Изучить распространенность и структуру симптомов поражения сердечно-сосудистой системы (АГ, нарушения сердечного ритма и проводимости, АКМП, ИБС) у пациентов с АБ в раннем (в течение 1 месяца) и позднем (в течение 36 месяцев наблюдения) постабстинентном периоде.
- Изучить особенности динамики симптомов поражения сердечно-сосудистой симптомы у пациентов с АБ в позднем постабстинентном периоде.
- Изучить распространенность осложненного течения сердечно-сосудистой патологии у приверженных и не приверженных к терапии пациентов с АБ в позднем постабстинентном периоде.
- Определить связь смертности пациентов с их приверженностью к лечению в течение 36 месяцев наблюдения.
- Оценить связь полиморфизма генетических детерминант для структуры кардиальной патологии системы ингибиторов АПФ (гены АСЕ, AGT, AGTR1, AGTR2), гена синтазы оксида азота (NOS), дофаминовых рецепторов гена DRD2 (рецептор дофамина типа 2) и гена DRD4 (рецептор дофамина типа 4), адренорецепторов ADRA2A (a2A-адренергический рецептор), ADRB2 (b2-адренорецептор) и ADRB1 (b1-адренорецептор).
- Определить наиболее эффективные классы, оптимальные дозы и среднюю продолжительность терапии антигипертензивными, антиаритмическими и антиангинальными препаратами у пациентов с АБ.
- Определить необходимую продолжительность кардиологического наблюдения пациентов с АБ после прекращения употребления алкоголя.
Научная новизна исследования.
Работа является комплексным научным исследованием пациентов с АБ в реальной клинической практике.
Впервые проведено проспективное кардиологическое исследование с комплексным (физикальным, лабораторным, инструментальным и генетическим) обследованием в раннем и позднем постабстинентном периодах у пациентов с АБ после прекращения употребления алкоголя.
Впервые проанализированы наиболее эффективные классы гипотензивных и антиаритмических препаратов у пациентов с АБ после прекращения употребления алкоголя.
Впервые проанализирована связь генетического полиморфизма систем ингибиторов АПФ (гены АСЕ, AGT, AGTR1, AGTR2), гена синтазы оксида азота (NOS), дофаминовых рецепторов гена DRD2 (рецептор дофамина типа 2) и гена DRD4 (рецептор дофамина типа 4), адренорецепторов ADRA2A (a2A-адренергический рецептор), ADRB2 (b2-адренорецептор) и ADRB1 (b1-адренорецептор) с вариантами сердечно-сосудистой патологии у пациентов с АБ.
Впервые проведен анализ динамики симптомов сердечно-сосудистой патологии в зависимости от этих вариантов генетического полиморфизма. Впервые проанализирована связь генетического полиморфизма с наиболее эффективной кардиотропной терапией в течение 3 лет наблюдения.
Практическая значимость работы.
Полученные результаты могут использоваться в практической кардиологии и наркологии для динамического наблюдения пациентов с АБ.
Результаты работы позволяют выбрать оптимальную диагностическую тактику в раннем постабстинентном периоде, а также осуществить быстрый подбор наиболее эффективной кардиотропной терапии в раннем и позднем постабстинентном периоде у пациентов с АБ, прекративших употреблять алкоголь.
Результаты генетического исследования расширяют современные представления о наиболее эффективных вариантах гипотензивных препаратов для коррекции АГ у пациентов с АБ.
Основные положения, выносимые на защиту:
- Для пациентов с АБ, прекративших употреблять алкоголь, характерны частые (всего у 73.1% больных) симптомы поражения сердечно-сосудистой системы в раннем и позднем постабстинентном периоде. Наиболее частыми симптомами поражения сердечно-сосудистой системы являются АГ (56.9%) и нарушения сердечного ритма (23.1%), наиболее редким – нарушения сердечной проводимости (1.2%).
- Динамика АГ и нарушений сердечного ритма, а также доля пациентов, нуждающихся в непрерывном приеме кардиотропных препаратов, значительно различаются в раннем и позднем постабстинентном периодах. Необходимость постоянного приема гипотензивных и антиаритмических препаратов к 12 месяцам наблюдения сохраняется и возникает не менее чем в 52.2% случаев.
- Пациенты с АБ, страдающие АГ и желудочковыми нарушениями сердечного ритма, наиболее часто (92.3%) нуждаются в постоянном непрерывном приеме гипотензивных и антиаритмических препаратов.
- Наиболее эффективными гипотензивными препаратами у пациентов с АБ являются b-адреноблокаторы, наименее эффективными – препараты класса ингибиторы АПФ. При неэффективности монотерапии высокий гипотензивный эффект оказывает комбинация «b-адреноблокатор+антагонист кальция».
- Наиболее эффективными антиаритмическими препаратами для коррекции суправентрикулярных и желудочковых нарушений сердечного ритма являются b-адреноблокаторы, а также комбинация «b-адреноблокатор+амиодарон». При необходимости достижения одновременного гипотензивного и антиаритмического эффекта наиболее эффективной комбинацией является «b-адреноблокатор+антагонист кальция+амиодарон».
- Среди пациентов с АБ достоверно реже по сравнению со здоровыми лицами встречается вариант генетического полиморфизма АСЕ I/D, недостоверно чаще - неблагоприятный вариант генетического полиморфизма АСЕ D/D.
- Пациенты с АБ, прекратившие употреблять алкоголь, нуждаются в длительном (24-36 месяцев после прекращения употребления алкоголя) динамическом кардиологическом наблюдении.
Внедрение результатов исследования в практику.
Результаты исследования внедрены в работу клиники кардиологии УКБ №1 и наркологического отделения Клиники психических болезней им. С.С. Корсакова Первого МГМУ им. И.М. Сеченова. Материалы диссертации включены в лекционный курс на кафедре профилактической и неотложной кардиологии ФППОВ Первого МГМУ им. И.М. Сеченова.
Основные положения работы могут быть рекомендованы для широкого применения в других кардиологических и наркологических центрах.
Апробация материалов исследования.
Материалы диссертации доложены и обсуждены на Международном конгрессе «Кардиостим-2008» (г. Санкт-Петербург, 2008), 10-м Юбилейном научно-образовательном форуме «Кардиология-2008» (г. Москва, 2008).
Апробация диссертации состоялась 01.11.2011 г. на совместном заседании кафедры профилактической и неотложной кардиологии ФППОВ и клиники кардиологии УКБ №1 Первого Московского государственного медицинского университета им. И.М. Сеченова Минздравсоцразвития России.
Личный вклад автора.
Автор самостоятельно сформировала и в процессе работы корректировала направление и дизайн исследования, проводила отбор пациентов в соответствии с критериями включения и исключения. С пациентами в процессе проспективного наблюдения автором производились физикальные и инструментальные осмотры. Автором самостоятельно производились и анализировались результаты инструментальных методов исследования (ЭКГ покоя, суточное мониторирование ЭКГ, суточное мониторирование АД, нагрузочный тредмил-тест), назначалась терапия гипотензивными, антиаритмическоми и антиангинальными препаратами, терапия пациентов с ХСН.
Автором разработана документация для сбора информации о больных с алкогольной болезнью, лично проанализирован материал, разработан алгоритм подбора эффективной терапии у пациентов с алкогольной болезнью. Все полученные результаты статистически обработаны лично автором. На всех этапах исследования (от постановки задач, их клинической реализации до обсуждения результатов в научных публикациях и формулировке выводов и практических рекомендаций) вклад автора является определяющим.
Публикация материалов исследования.
По материалам диссертации опубликовано 15 научных работ, в том числе 12 – в рецензируемых журналах.
Объем и структура работы.
Диссертация изложена на 265 страницах машинописного текста и состоит из введения, обзора литературы, материала и методов исследования, их обсуждения, главы собственных результатов, выводов, практических рекомендаций, приложений и библиографии, включающей 42 отечественные и 149 зарубежных литературных источников. Диссертация иллюстрирована 57 рисунками и 65 таблицами.
ОСНОВНОЕ СОДЕРЖАНИЕ РАБОТЫ
Общая характеристика изученной выборки.
Всего скринировано 1740 пациентов с диагнозом «зависимость от алкоголя» 2-3 стадии (F-10.2 по МКБ-10) в возрасте от 22 до 77 лет. В соответствии с критериями включения и исключения в исследование было включено 388 пациентов, однако в течение первых 2 месяцев наблюдения вследствие низкой приверженности к лечению из исследования выбыло 128 пациентов. Таким образом, в исследовании приняло участие 260 пациентов мужского пола в возрасте от 22 до 74 лет (средний возраст составил 466,6 лет), рисунок 1.
Рис. 1. Дизайн исследования.

Пациенты включались в исследование на 5-7 сутки стационарного лечения по поводу алкогольного абстинентного синдрома (ААС) в наркологическом отделении Клиники психических болезней им. С.С. Корсакова после получения добровольного согласия на участие в исследовании и при условии полного прекращения употребления алкоголя.
Критериями исключения пациентов являлись отказ пациента от участия в исследовании, острая и хроническая почечная и печеночная недостаточность, острый и хронический вирусный гепатит, цирроз печени, любые тяжелые хронические соматические заболевания, делающие невозможным стандартное обследование (например, нагрузочный тест), выраженная алкогольная энцефалопатия, вследствие которой адекватный контакт с пациентом был невозможен, а также психотическое состояние.
Наблюдение пациентов осуществлялось в два этапа:
- период стационарного наблюдения (с 5-7 дня пребывания в наркологическом стационаре до момента выписки пациента из стационара);
- период амбулаторного наблюдения (в течение следующих 36 месяцев).
В период пребывания пациента в наркологическом отделении (период стационарного наблюдения) осуществлялись первые визиты пациентов в Клинику кардиологии Первого МГМУ им. И.М. Сеченова, во время которых проводилось стандартное обследование: физикальный осмотр, регистрация ЭКГ покоя, суточное мониторирование ЭКГ по Холтеру, суточное мониторирование АД, трансторакальная эхокардиография, общий и биохимический анализы крови, анализ уровня тиреоидных гормонов крови. Количество визитов в период госпитализации определялось индивидуально в каждом случае. Оценка эффективности гипотензивной, антиаритмической и антиангинальной терапии производилась при помощи контрольных инструментальных исследований (суточное мониторирование АД, суточное мониторирование ЭКГ, контрольный нагрузочный тредмил-тест). На 4-8 неделе после прекращении употребления алкоголя (период амбулаторного наблюдения) всем пациентам проводился нагрузочный тредмил тест. В дальнейшем осуществлялись обязательные контрольные визиты пациентов не реже 1 раза в 3 месяца в течение первого года наблюдения и не реже 1 раза в 2 месяца на 2 и 3 годах наблюдения. Дополнительные визиты осуществлялись по мере необходимости по желанию врача и пациента в течение всего периода наблюдения. Их частота определялась индивидуально в каждом случае и зависела от эффективности кардиотропной терапии, которая оценивалась по результатам контрольных инструментальных исследований.
По результатам наблюдения за первые 8 недель все пациенты были распределены на 2 группы:
Группа А (n=190) - пациенты с АБ, имеющие какую-либо сердечно-сосудистую патологию (подъемы АД, нарушения сердечного ритма и проводимости, АКМП, верифицированную ИБС в анамнезе);
Группа АК (n=70) - пациенты с АБ, у которых по результатам обследования не было выявлено сердечно-сосудистой патологии.
Пациентам мужского пола славянской этнической принадлежности, не родственным между собой, производился также анализ генетического полиморфизма ренин-ангиотензин-альдостероновой системы (АСЕ, AGT, AGTR1), гена синтазы оксида азота (NOS), дофаминовой рецепции (DRD2, DRD4) и - и -адренорецепции (ADRA2A, ADRB2, ADRB1) в лабораториях генетики Национального научного центра наркологии и Научно-исследовательского института физико-химической медицины. Генетическое исследование проводилось однократно, являлось дополнительным методом обследования и не влияло на распределение пациентов на группы.
Анализ генетического полиморфизма ренин-ангиотензин-альдостероновой системы (РААС), NOS проводился в лаборатории Генетики человека на базе ФГУ НИИ физико-химической медицины. ДНК лейкоцитов выделяли из 2 мл цельной крови с помощью набора Wizard (Promeda, США) в соответствии с инструкцией производителя. Анализ полиморфных маркеров получен в ходе ПЦР–амплификации при помощи олигонуклеотидных пар праймеров с определенными последовательностями. Для идентификации точечных олигонуклеотидных замен в исследуемых генах использовали подходящие смеси дезокси- и дидезоксинуклеотидтрифосфатов (dNTP и ddNTP) и следующие олигонуклеотидные зонды с последующей реакцией термоциклического минисеквенирования. Для очистки продукции минисеквенирования и секвенирования использовали SpectroCLEAN Kit (Sequenom, США) в соответствии с инструкцией фирмы-производителя. Варианты исследуемых полиморфизмов представлены в таблице 1.
Анализ генетического полиморфизма рецепторов дофамина (DRD2, DRD4) и - и -адренергических рецепторов (ADRA2A, ADRB2, ADRB1) производился в лаборатории Молекулярной генетики Национального научного центра наркологии.
Генотипирование образцов ДНК, полученных из 2 мл цельной венозной крови путем фенолхлороформной экстракции, для нуклеотидных полиморфизмов проводили методом полимеразной цепной реакции (ПЦР) с последующим рестрикционным анализом, для полиморфизма числа коротких повторов (48 н.п.) и дупликации (120 н.п.) – методом ПЦР фрагмента экзона 3 гена DRD4 (V48) и 5,-области гена (V120) с последующим анализом в 2% агарозном геле. Условия реакции и дизайн олигонуклеотидных праймеров доступен по запросу. Варианты исследуемых полиморфизмов представлены в таблице 1.
Табл. 1. Варианты исследуемых полиморфизмов ренин-ангиотензин-альдостероновой системы, гена синтазы оксида азота, рецепторов дофамина и адренергических рецепторов.
| Ген | Название гена | Вариант полиморфизма |
| АСЕ | ген ангиотензин-превращающего фермента | I/D |
| AGT | ген ангиотензиногена | М174Т Т235М |
| NOS | ген синтазы оксида азота | G298А G894E |
| AGTR1 | ген рецептора 1 типа ангиотензина II | А1166С |
| ADRB1 | 1-адренергический рецептор | S49G |
| R389G | ||
| ADRB2 | 2-адренергический рецептор | C589T Q27E |
| ADRA2A | 2A-адренергический рецептор | Msp 1 |
| A261G | ||
| C68T | ||
| DRD2 | D2 рецептор дофамина | Taq I |
| Nco I | ||
| DRD4 | D4 рецептор дофамина | 48-bр |
| 120-bр |
Для анализа частоты встречаемости исследуемых аллелей была сформирована группа контрольная группа здоровых лиц в возрастном диапазоне 22-76 лет.
Критериями включения здоровых лиц в контрольную группу являлись:
- Согласие добровольца на участие в исследовании.
- Оптимальные, нормальные и нормальные высокие значения АД по результатам суточного мониторирования АД и при физикальном осмотре (в соответствии с Национальными клиническими рекомендациями ВНОК, 2009 и Рекомендациями Европейского Общества по артериальной гипертензии, 2007)
- Отсутствие значимых нарушений сердечного ритма и проводимости во время суточного мониторирования ЭКГ по Holter.
- Соответствие суточного профиля при проведении суточного мониторирования АД рекомендованным значениям среднесуточного АД, среднего дневного и среднего ночного АД (в соответствии с Национальными клиническими рекомендациями ВНОК, 2009 и Рекомендациями Европейского Общества по артериальной гипертензии, 2007)
- Отрицательный результат нагрузочной пробы, нормотонический тип реакции на нагрузку и отсутствие индукции нарушений сердечного ритма и проводимости при проведении нагрузочного тредмил-теста.
- Отсутствие какой-либо патологии при проведении трансторакальной эхокардиографии.
Критерии исключения здоровых лиц из исследования:
- Поражение других органов и систем, влекущие за собой вторичные изменения со стороны сердечно-сосудистой системы (тиреотоксикоз, острая или хроническая анемия и т.п.).
- Соматические и психотические состояния, препятствующие обследованию, наблюдению и контакту с пациентом.
Статистическая обработка.
Статистическая обработка проводилась при помощи статистической программы SPSS 10/11, а также Primer of Biostatistics 4.03. Большинство данных в таблицах и графиках представлены в формате «среднее значениестандартное отклонение» (М). Частотные переменные представлены в виде абсолютной частоты и в виде процентов. Для проверки характера распределения интервальных переменных использовали непараметрический тест Колмогорова-Смирнова. В зависимости от типа распределения переменных и количества наблюдений применялись методы параметрической и непараметрической статистики. При анализе значимости различий между двумя несвязанными выборками использовали Т-тест Стьюдента или критерий Манна-Уитни, между двумя связанными выборками - Т-тест Стьюдента или критерий Уилкоксона.
При оценке достоверности различий частоты полиморфизмов в генетических исследованиях использовался критерий 2, связь признаков анализировали с помощью таблиц сопряженности. При достигнутом уровне значимости р0.05 дополнительно проводился попарный анализ межгрупповых различий генеральных (популяционных) долей каждой категории соответствующей переменной с помощью -критерия для качественных данных (после проверки допущений).
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ.
1. Клинико-демографическая характеристика групп.
Пациенты обеих групп достоверно не различались по возрасту, семейному и социальному положению, алкогольному анамнезу, продолжительности госпитализации в наркологическое отделение (таблица 2.).
Табл. 2. Сравнительная характеристика пациентов групп 1 и 2.
| Параметр | Группа 1 (n=190) | Группа 2 (n=70) | Р |
| Пол | мужской | мужской | - |
| Возраст, лет | 457.9 | 466.3 | 0.965 |
| Алкогольный анамнез 10-15 лет, % | 77.4 | 70.0 | 0.45 |
| Наиболее частый вариант алкогольного напитка (водка, виски), % | 81.1 | 78.6 | 0.613 |
| Семейная отягощенность | 94.2 | 92.9 | 0.622 |
| Первое употребление алкоголя до 18 лет, % | 83.7 | 85.7 | 0.892 |
У пациентов группы 1 (n=190) были выявлены симптомы сердечно-сосудистой патологии, представленные в таблице 3.
Табл. 3. Структура сердечно-сосудистой патологии среди пациентов групп 1 и 2.
| Группа | Вариант сердечно-сосудистой патологии | Количество пациентов, чел | % среди всех пациентов с АБ |
| Группа 1 (n=190) | Артериальная гипертензия без других симптомов поражения сердечно-сосудистой системы | 106 | 40.8 |
| Симптомные пароксизмальные наджелудочковые нарушения сердечного ритма | 37 | 14.2 | |
| Симптомные пароксизмальные желудочковые нарушения сердечного ритма | 23 | 8.9 | |
| Верифицированная ИБС | 13 | 5.0 | |
| Алкогольная (дилатационная) кардиомиопатия | 8 | 3.1 | |
| Нарушения сердечной проводимости | 3 | 1.2 | |
| Группа 2 (n=70) | Без патологии | ||
У 106 (40.8%) пациентов группы 1 регистрировалась АГ без других симптомов поражения сердечно-сосудистой системы. При этом по результатам СМАД у этих пациентов регистрировались превышения рекомендованных значений среднесуточного АД, среднего дневного и среднего ночного АД (в соответствии с Национальными клиническими рекомендациями ВНОК, 2009 и Рекомендациями Европейского Общества по артериальной гипертензии, 2007) и регистрировались подъемы АД выше 140/90 мм рт. ст. при осмотре в раннем постабстинентном периоде.
У 37 (14.2%) пациентов этой группы во время холтеровского мониторирования были выявлены короткие симптомные или продолжительные пароксизмы фибрилляции/трепетания предсердий, либо пароксизм фибрилляции/трепетания предсердий был документирован при регистрации ЭКГ покоя.
У 23 (8.9%) пациентов этой группы были зарегистрированы пароксизмы симптомной неустойчивой или устойчивой желудочковой тахикардии либо периоды идиовентрикулярного ритма во время суточного мониторирования ЭКГ.
У 13 (5.0%) пациентов этой группы имелась медицинская документация о перенесенном в прошлом остром инфаркте миокарда или проведении коронароангиографии.
Алкогольная кардиомиопатия была диагностирована у 8 (3.1%) пациентов с клиническими проявлениями хронической сердечной недостаточности и признаками дилатационной кардиомиопатии при проведении трансторакальной эхокардиографии.
2. Особенности динамики АГ у пациентов с алкогольной болезнью.
Среди всех симптомов сердечно-сосудистой патологии самым распространенным симптомом была АГ – регистрировалась у 148 пациентов группы 1, причем у 106 пациентов не сопровождалась другими симптомами сердечно-сосудистой патологии (рисунок 2).
Рис. 2. Распространенность АГ среди пациентов с АБ (n=260).

Для пациентов групп 1 и 2 были характерны значимые различия динамики АД во время алкогольного абстинентного синдрома (ААС), в раннем (в течение 1 месяца) и позднем постабстинентном периодах. Для 148 из 190 пациентов группы 1 были характерны умеренные или значительные подъемы АД во все три периода наблюдения. Для пациентов группы 2 во время ААС было характерно нормальное высокое АД или подъемы не превышали 150/100 мм рт. ст. В раннем и позднем ПАП у пациентов группы 2 регистрировалось оптимальное, нормальное или нормальное высокое АД.
При наблюдении пациентов с АГ в течение 36 месяцев было выявлено, что необходимость в постоянной гипотензивной терапии различается среди пациентов с АГ без других симптомов поражения сердечно-сосудистой системы, больных с АГ и симптомными наджелудочковыми пароксизмами и пациентами с АГ и симптомными желудочковыми пароксизмами (см. рисунок 3).
Рис.3. Необходимость приема гипотензивных препаратов у пациентов с АГ.
 * р=0.034; **р=0.025
* р=0.034; **р=0.025 Как видно из представленного рисунка, пациенты с АГ без других симптомов сердечно-сосудистой патологии к 12 месяцам наблюдения нуждались в постоянном приеме гипотензивных препаратов лишь в 52.5% случаев, а к 36 месяцам наблюдения необходимость в гипотензивной терапии у этих больных возникала в 9.09% случаев.
Пациенты с АГ и симптомными пароксизмальными наджелудочковыми нарушениями сердечного ритма демонстрировали наибольшую (72.9%) необходимость гипотензивной терапии к 3 месяцам наблюдения. К 12 месяцам наблюдения в постоянной гипотензивной терапии нуждались 60.6% пациентов, к 36 месяцам наблюдения – 18.2% больных.
Пациенты с АГ и симптомными желудочковыми пароксизмальными нарушениями ритма продемонстрировали «нарастающий» характер артериальной гипертензии: к 12 месяцам динамического наблюдения гипотензивные препараты получали 93.8% пациентов, при этом к 36 месяцам наблюдения необходимость в постоянной гипотензивной терапии сохранялась у 81.25% больных.
2. Особенности динамики нарушений сердечного ритма у пациентов с алкогольной болезнью.
Среди пациентов группы 1 регистрировалась как суправентрикулярные, так и желудочковые нарушения сердечного ритма. Среди всех пациентов с АБ, согласившихся принять участие в наблюдении, симптомные нарушения сердечного ритма регистрировались у 68 больных, что составило 35.8% среди всех пациентов группы 1 (n=190) и 26.2% среди всех пациентов с АБ (n=260).
Структура и распространенность нарушений сердечного ритма среди пациентов с АБ представлены на рисунке 4.
Рис. 4. Структура и распространенность нарушений сердечного ритма среди пациентов с АБ (n=260).

Во время обязательных и дополнительных визитов всем пациентам с нарушениями сердечного ритма производилось суточное мониторирование ЭКГ для контроля эффективности антиаритмической терапии и решения вопроса о необходимости коррекции терапии. Периодически (не реже 1 раза в 2 месяца, перед очередным визитом) производились попытки постепенного снижения доз антиаритмических препаратов с оценкой возможности полного прекращения их приема по результатам контрольного суточного мониторирования ЭКГ. При этом контрольное холтеровское исследование производилось как при каждом снижении дозы, так и при полном прекращении приема препарата.
Необходимость в постоянной антиаритмической терапии у пациентов с симптомными желудочковыми и наджелудочковыми пароксизмальными нарушениями сердечного ритма также была различной (рисунок 5).
Рис. 5. Необходимость в постоянной антиаритмической терапии у пациентов с симптомными желудочковыми и наджелудочковыми нарушениями сердечного ритма в различные сроки наблюдения.

* р=0.006; ** р=0.02; ***р=0.002
Среди больных с симптомными наджелудочковыми нарушениями сердечного ритма наиболее часто встречалась фибрилляция/трепетание предсердий. Клинически все пароксизмы были симпатадреналовыми, кроме того, в период стационарного лечения в наркологическом отделении у 11 из 37 пациентов (29.72%) имелись проявления гипокалиемии.
Через 3 месяца приема антиаритмических препаратов необходимость приема сохранялась у 26 (70.27%) пациентов с симптомными наджелудочковыми нарушениями сердечного ритма. К 12 месяцам наблюдения антиаритмическая терапия проводилась 20 пациентам (60.60%), к 36 месяцам наблюдения -5 больным (15.2%).
Среди пациентов с симптомными желудочковыми нарушениями сердечного ритма к 12 месяцам наблюдения постоянную антиаритмическую терапию получали 15 пациентов (93.75%), к 36 месяцам наблюдения - 13 пациентов (81.25% пациентов, продолживших участие в исследовании).
3. Особенности гипотензивной и антиаритмической терапии у пациентов с алкогольной болезнью.
Для достижения гипотензивного эффекта использовались следующие препараты:
- ингибиторы АПФ (эналаприл 5-10 мг/сут; лизиноприл 2.5-20 мг/сут);
- пролонгированные -адреноблокаторы (бетаксолол 5-20 мг/сут; бисопролол 2.5-10 мг/сут; небиволол 2.5-5 мг/сут);
- дигидропиридиновые блокаторы кальциевых каналов (амлодипин 2.5-10 мг/сут; фелодипин 2.5-10 мг/сут; нифедипин 10-40 мг/сут);
- не дигидропиридиновые блокаторы кальциевых каналов (дилтиазем 60-180 мг/сут; верапамил 40-240 мг/сут)
Последовательная схема подбора гипотензивной монотерапии или комбинации представлена на рисунке 6.
Рис. 6. Варианты гипотензивной терапии у пациентов с алкогольной болезнью.
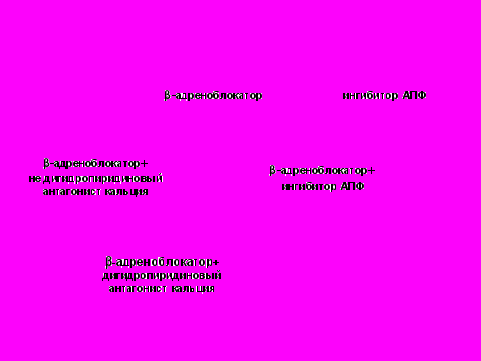
Критериями эффективности гипотензивной терапии было достижение целевых значений АД по результатам контрольного СМАД после каждой смены монотерапии или комбинации: среднесуточное АД 125-130/80 мм рт. ст., среднее дневное – 130-135/85 мм рт. ст., среднее ночное – 120/70 мм рт. ст. (в соответствии с Национальными клиническими рекомендациями ВНОК, 2009 и Рекомендациями Европейского Общества по артериальной гипертензии, 2007).
Для достижения антиаритмического эффекта использовались следующие препараты:
- пролонгированные b-адреноблокаторы (бетаксолол 5-20 мг/сут; бисопролол 2.5-10 мг/сут; небивалол 2.5-5 мг/сут);
- блокаторы кальциевых каналов (не дигидропиридиновые - дилтиазем 60-180 мг/сут; верапамил 40-240 мг/сут);
- амиодарон 200-600 мг/сут.
Последовательная схема подбора антиаритмической монотерапии или комбинации представлена на рисунке 7.
Рис. 7. Варианты антиаритмической терапии у пациентов с алкогольной болезнью.
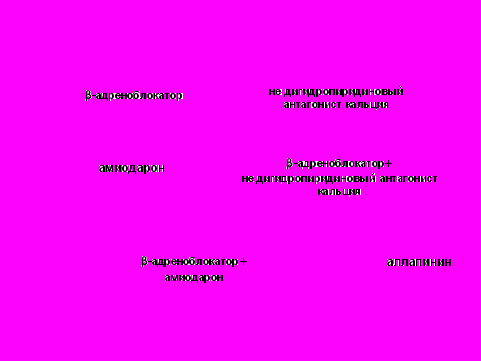
Критериями эффективности антиаритмической терапии было отсутствие пароксизмальных желудочковых и наджелудочковых нарушений ритма, а также отсутствие парной и групповой наджелудочковой и желудочковой экстрасистолии.
Варианты эффективной гипотензивной терапии пациентов с АГ без других симптомов сердечно-сосудистой патологии представлены на рисунке 8. У этих пациентов достоверно чаще использовалась монотерапия -адреноблокаторами (р=0.01), комбинация «антагонист кальция+ -адреноблокатор» использовалась только в первые 9 месяцев наблюдения.
Ни у одного из пациентов этой подгруппы ингибиторы АПФ (эналаприл, лизиноприл) не были эффективными.
Рис.8. Варианты эффективной гипотензивной терапии в подгруппе АГ ( n=106).

* р=0.01
Среди пациентов с симптомными наджелудочковыми нарушениями сердечного ритма с хорошим эффектом использовались 3 варианта терапии (рисунок 9).
Рис.9. Варианты эффективной гипотензивной и антиаритмической терапии у пациентов с симптомными наджелудочковыми нарушениями сердечного ритма и АГ( n=37).
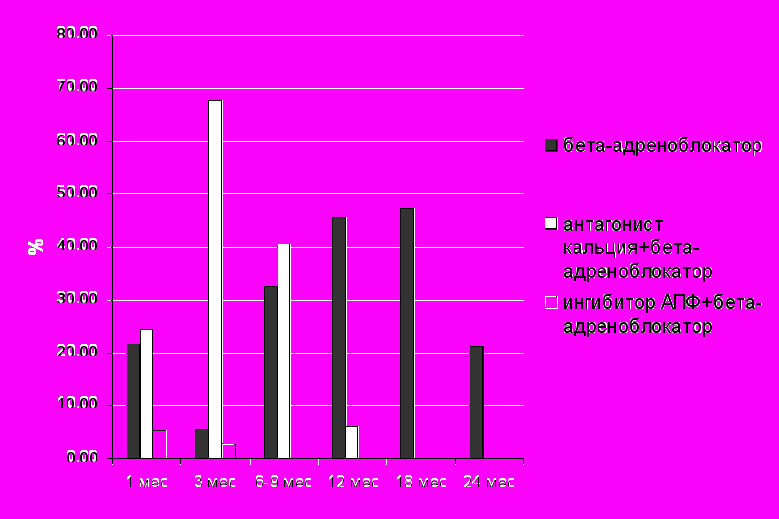
По результатам дисперсионного анализа повторных измерений (р=0.058) была выявлена выраженная клинически значимая тенденция к достоверности следующих результатов: наиболее часто для терапии пациентов подгруппы СВН использовалась монотерапия -адреноблокаторами, причем этого варианта терапии было достаточно как для достижения гипотензивного, так и для достижения антиаритмического эффекта с 12 месяца наблюдения. Наименее востребованной была комбинация «ингибитор АПФ+-адреноблокатор», при этом монотерапия ингибиторами АПФ не была эффективной ни у одного из пациентов.
Среди пациентов с симптомными пароксизмальными желудочковыми нарушениями сердечного ритма (n=23, рисунок 9) на момент включения в исследование можно было выделить 2 категории пациентов:
- пациенты, которые нуждаются только в антиаритмической терапии: 8 больных (34.79%);
- пациенты, которые нуждаются и в антиаритмической, и в гипотензивной терапии: 15 пациентов (65.21%).
Для коррекции желудочковых нарушений сердечного ритма у пациентов, которые не нуждались в гипотензивной терапии (n=8), было достаточным назначения -адреноблокатора пролонгированного действия (небивалол 5-7.5 мг/сут, бисопролол 5-10 мг/сут, бетаксолол 10-20 мг/сут). Во время контрольных суточных регистраций ЭКГ к 3 месяцам наблюдения у всех этих пациентов было отмечено исчезновение эктопической желудочковой активности на фоне указанных суточных доз препаратов. При постепенной отмене терапии к 6 месяцам наблюдения ни один из этих пациентов не нуждался в постоянном приеме антиаритмических препаратов.
Иная картина наблюдалась в динамике у пациентов с желудочковыми нарушениями сердечного ритма и артериальной гипертензией (n=15).
Для коррекции симптомных желудочковых нарушений сердечного ритма (симптомные пароксизмы неустойчивой желудочковой тахикардии) и достижения гипотензивного эффекта 10 пациентам (43.47%) было достаточным назначение -адреноблокаторов. Остальным 5 пациентам (21.74%) была назначена комбинация антагониста кальция и -адреноблокатора.
Через 3 месяца наблюдения необходимость в приеме гипотензивных препаратов сохранялась у 14 пациентов (60.86%). Монотерапия -адреноблокаторами была эффективной у 9 больных (39.13%), для остальных пациентов (5 человек, 21.74%) наиболее эффективным оказался прием антагонистов кальция на фоне приема амиодарона. Ни у одного из пациентов этой подгруппы ингибиторы АПФ не были эффективными.
Через 6-9 мес гипотензивная терапия была показана 15 пациентам (65.21%). На этом этапе наблюдения наиболее эффективной комбинацией для достижения гипотензивного и антиаритмического эффекта был прием антагонистов кальция на фоне приема амиодарона – 12 пациентов, 52.17%. 3 пациентам (13.04%) назначался также -адреноблокатор в комбинации «антагонист кальция+амиодарон+-адреноблокатор» для достижения оптимального гипотензивного эффекта
К концу 1 года наблюдения из исследования выбыли 7 пациентов с пароксизмами устойчивой и неустойчивой желудочковой тахикардии из-за низкой приверженности к лечению. Таким образом, к 12 месяцам наблюдения подгруппа ЖН включала в себя 16 пациентов, из которых необходимость в постоянной гипотензивной терапии сохранялась у 15 пациентов (93.75%). Комбинацию «антагонист кальция+амиодарон» постоянно получали 10 пациентов (62.50%), комбинацию «антагонист кальция+амиодарон+-адреноблокатор» - 3 пациента (18.75%), комбинацию «антагонист кальция+-адреноблокатор» - 2 больных (12.5%). К 24 месяцам наблюдения у 14 больных (87.5%) проводилась терапия гипотензивными и антиаритмическими препаратами. Наиболее часто (12 пациентов, 89.29%) больные принимали комбинацию «антагонист кальция+-адреноблокатор», 2 больных (18.08%) получали комбинацию «антагонист кальция+амиодарон». Сходная картина отмечалась к 36 месяцам наблюдения: в терапии гипотензивными и антиаритмическими препаратами нуждались те же 14 пациентов (87.5%). Их комбинации и дозы препаратов остались прежними.
Рис.10. Варианты эффективной терапии у пациентов с желудочковыми нарушениями сердечного ритма и артериальной гипертензией (подгруппа ЖН, n=23).
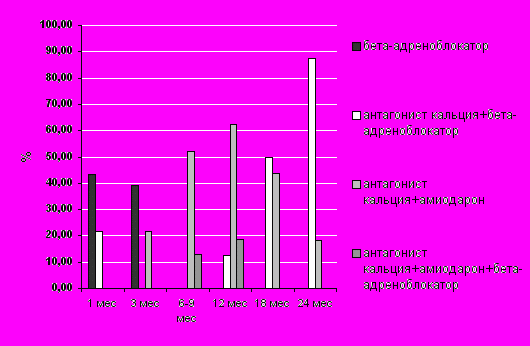
При проведении дисперсионного анализа повторных измерений достоверных различий между используемыми вариантами лечения этой подгруппы получено не было (р=0.196).
4. Варианты осложненного течения кардиальной патологии и сердечно-сосудистая смертность у пациентов с АБ.
Анализ общей и сердечно-сосудистой смертности среди пациентов групп 1 и 2 был произведен с учетом их приверженности к лечению.
В течение 1 года наблюдения из группы 1 (n=190) выбыли 7 больных. Причинами прекращения участия в исследовании были:
- отказ пациентов от продолжения участия в исследовании;
- неявка больных в контрольные сроки без объяснения причин.
У всех этих больных (таблица 4) регистрировались значимые (до 220/120 мм рт. ст.) подъемы АД. При первичном обследовании во время суточного мониторирования ЭКГ были выявлены одиночные (тысячи) и групповые (парные и триплеты) желудочковые экстрасистолы, пароксизмы неустойчивой желудочковой тахикардии (от 5 до 23 в сутки). У 4 пациентов этой подгруппы диагностирована дилатационная кардиомиопатия с явлениями недостаточности кровообращения 2-3 ФК по NYHA и частыми (до 3 раз в неделю) пароксизмами фибрилляции предсердий.
Табл. 4. Смертность и варианты сердечно-сосудистой патологии у не приверженных к лечению пациентов группы 1 (n=7).
| Варианты патологии | Количество, чел | Всего умерло, чел | Смерть во сне |
| АГ | 3 | 7 | 6 |
| Значимые желудочковые нарушения ритма | 7 | ||
| ДКМП | 4 |
Через 24 месяца с момента первичного визита все некомплаентные пациенты умерли, при этом у 6 из них была констатирована смерть во сне, у 1 больного смерть носила насильственный характер.
Остальные 183 пациента группы 1 получали гипотензивную, антиаритмическую и антиангиальную терапию с регулярной периодической коррекцией во время контрольных визитов по мере необходимости. Среди этих пациентов случаев смерти зарегистрировано не было, однако имелись случаи осложненного течения сердечно-сосудистой патологии (таблица 5).
Табл. 5. Варианты осложненного течения сердечно-сосудистой патологии у приверженных к лечению пациентов группы 1.
| Вариант осложнения | n | % в группе |
| Геморрагический инсульт | 5 | 2.6 |
| Ишемический инсульт | 3 | 1.6 |
| Устойчивая пароксизмальная желудочковая тахикардия | 15 | 7.9 |
Статистически значимых достоверных различий распространенности описанных осложнений среди пациентов группы 2 и комплаентных пациентов группы 1 получено не было, однако была выявлена клинически значимая тенденция к более высокой распространенности устойчивой желудочковой тахикардии среди приверженных к лечению пациентов группы 1 (рисунок 11).
Рис. 11. Варианты осложненного течения сердечно-сосудистой патологии у приверженных к терапии пациентов группы 1 (n=183) и пациентов группы 2 (n=70).

5. Анализ генетического полиморфизма системы ингибиторов АПФ (гены АСЕ, AGT, AGTR1, AGTR2), гена синтазы оксида азота (NOS), дофаминовых рецепторов гена DRD2 (рецептор дофамина типа 2) и гена DRD4 (рецептор дофамина типа 4), адренорецепторов ADRA2A (a2A-адренергический рецептор), ADRB2 (b2-адренорецептор) и ADRB1 (b1-адренорецептор).
В связи с общепринятыми правилами генетических популяционных исследований в исследования генетического полиморфизма включаются лица:
- единой этнической принадлежности;
- единого пола;
- не родственные между собой.
Таким образом, среди 260 пациентов с АБ, вошедших в наблюдение, в исследование представленных вариантов генетических полиморфизмов было включено 200 мужчин славянской этнической принадлежности, не родственных между собой.
Для корректного анализа частоты распространенности аллелей и вариантов полиморфизма была сформирована также контрольная группа здоровой возрастной нормы (n=40).
Варианты генетического полиморфизмы были выбраны исходя из основных патофизиологических звеньев кардиотоксического действия алкоголя: гиперсимпатикотония, прямая алкоголь-индуцированная вазоконстрикция и нарушение механизма синтеза NO.
Для поддержания механизмов гиперсимпатикотонии и алкоголь-индуцированной вазоконстрикции был целесообразным анализ генетического полиморфизма тех патофизиологических звеньев, которые лежат в основе высокой симпатической активации:
- адренергических рецепторов: 1-адренергического рецептора (ADRB1 S49G, R389G), 2-адренергического рецептора (ADRB2 C589T, Q27E), 2A-адренергического рецептора (ADRA2A Msp 1, A261G, C68T);
- рецепторов дофамина: D2 рецептор дофамина (DRD2 Taq I, Nco I),
D4 рецептор дофамина (DRD4 48-bр, 120-bр).
Мы также анализировали варианты генетического дефекта NO-синтазы (NOS G298А, G894E), поскольку нарушение механизма синтеза NO является доказанным патофизиологическим звеном кардиотоксического действия алкоголя.
Кроме того, с учетом низкой эффективности ингибиторов АПФ у пациентов с АБ мы предположили возможный генетический дефект ренин-ангиотензин-альдостероновой системы (РААС). Таким образом, был также произведен анализ генетического полиморфизма:
- гена ангиотензин-превращающего фермента (АСЕ I/D);
- гена ангиотензиногена (AGT М174Т, Т235М);
- ген рецептора 1 типа ангиотензина II (AGTR1 А1166С).
Варианты полиморфизма, выбранные для анализа, были наиболее перспективными генами-кандидатами в соответствии с отечественными и зарубежными публикациями на момент начала исследования. Мы анализировали как частоту встречаемости отдельных аллелей, так и вариантов генетического полиморфизма.
Из всех вариантов генетического полиморфизма достоверные (χ2 – 10.403, р=0.034.) межгрупповые различия были выявлены только для инсерционно-делеционного варианта I/D 287bp фрагмента в 16 интроне гена в генетического полиморфизма гена ангиотензин-превращающего фермента (ACE I/D).
В настоящее время считается доказанным, что при наличии D-аллеля имеется более высокий уровень циркулирующего АПФ (от 14 до 50%), а также более высокая активность тканевого фермента, т.е. можно говорить о самом высоком уровне фермента. У носителей I/I генотипа уровень фермента самый низкий, при генотипе I/D отмечается промежуточный уровень АПФ, при генотипе D/D – самый высокий уровень фермента. В настоящее время в литературе встречается все большее количество публикаций, где аллель I называют «протективным», т.е. с АГ ассоциирован аллель D.
Было выявлено, что вариант I/D встречался чаще (76.6%) в группе здоровых лиц по сравнению как с пациентами группы А (53.7%), так и с пациентами группы АК (57.8%). Таким образом, можно сказать, что во всех исследуемых группах превалировал вариант I/D, но в группе здоровых лиц этот вариант генотипа значительно преобладал (76.6%), тогда как среди всех пациентов с АБ встречался примерно в половине наблюдений.
Наиболее «протективный вариант» генотипа (I/I) у здоровых лиц встречался реже (7.8%) по сравнению с пациентами групп А (18.4%) и АК (20.5%): как ни пародоксально, среди пациентов с алкогольной зависимостью, имеющих кардиальную симптоматику, наиболее «протективный вариант» генотипа встречался чаще, чем у здоровых лиц.
Однако наиболее неблагоприятный вариант генотипа D/D встречался в группах А, АК и ЗК в 27.9%, 22.7% и 15.6% соответственно.При этом достоверных различий по частоте встречаемости отдельных аллелей выявлено не было.
Исходя из результатов нашего исследования, мы не можем говорить о четкой ассоциации аллеля D с АГ у пациентов с АБ, поскольку не выявили достоверных различий в распределении отдельных аллелей. Более корректным было бы считать, что для пациентов с АБ и кардиальной симптоматикой характерна достоверно более высокая частота встречаемости неблагоприятного варианта генотипа D/D по сравнению с пациентами с АБ без кардиальной симптоматики и здоровыми лицами контрольной группы (рисунок 12).
Рис. 12. Варианты генетического полиморфизма АСЕ I/D (n=240).
Исследование остальных генов-кандидатов не выявило достоверных различий и клинически значимых тенденций частоты встречаемости как отдельных аллелей, так и вариантов генетических полиморфизмов.
