Практикум по экологическому мониторингу окружающей среды Учебное пособие
| Вид материала | Практикум |
- Г. В. Плеханова (технический университет) М. А. Пашкевич, В. Ф. Шуйский экологический, 1176.09kb.
- В. Н. Масляев охрана окружающей среды учебное пособие, 1544.73kb.
- Черноморец Альберт Евгеньевич доктор юридических наук, профессор Алексеев Алексей Павлович, 1348.21kb.
- 1. 13. Федеральная служба по гидрометеорологии и мониторингу окружающей среды, 60.92kb.
- Мониторинг загрязнения окружающей среды на сети наблюдений гу «Алтайский цгмс», 65.15kb.
- Практикум для вузов Москва владос губарева Л. И., Мизирева О. М., Чурилова Т. М., Практикум, 2037.65kb.
- Учебное пособие санкт-петербург 2 004 удк 669. 2/8; 669. 4 (075. 80) Ббк 34., 990.55kb.
- Учебное пособие Санкт-Петербург 2000 удк 681, 344.56kb.
- Учебное пособие содержит лекции по методологии истории экономики, по развитию экономических, 90.36kb.
- Учебное пособие Миронова Т. Л., Подсолонко Е. А. Менеджмент окружающей среды. Симферополь,, 1405.95kb.
3.5.2Определение растворенного в воде кислорода
электрохимическим методом
Метод основан на измерении тока восстановления О2, диффундирующего к катоду через полупроницаемую мембрану. Скорость диффузии зависит от температуры воды. Мембрана пропускает и другие неполярные газы ( азот, СО2 и др. ). При применении щелочного электролита, восстанавливается только О2. Метод пригоден для анализа любых вод, в том числе мутных и окрашенных.
Аппаратура: прибор «Оксимер»
Материал: вода водоема.
Ход работы. Перед началом работы ознакомиться с инструкцией на прибор «Оксимер» и провести определение содержания кислорода.
Контрольные вопросы
- От каких факторов зависит содержание в воде растворенного кислорода?
- Каково гигиеническое значение определения растворенного в воде кислорода?
- Какими методами определяют содержание растворенного в воде кислорода? На чем основаны эти методы?
- Какие существуют нормативы на содержание в воде растворенного кислорода для водоемов различных категорий водопользования?
Работа №4. Определение микробиологических показателей качества воды
Прямое количественное определение возбудителей всех инфекций для контроля за качеством воды неосуществимо в связи с многообразием их видов и трудоемкостью анализа. Поэтому в практической санитарной микробиологии прибегают к косвенным методам, позволяющим определить потенциальную возможность заражения воды патогенными микроорганизмами.
Санитарно-биологическая оценка качества воды основана на определении двух основных показателей: микробного числа и числа бактерий Coli (группы кишечной палочки).
- Определение микробного числа
Микробное число дает представление об общей обсемененности воды аэробными сапрофитами, которые составляют только часть общего числа микробов в воде. Однако существует прямая зависимость между величиной микробного числа и вероятностью присутствия в воде патогенных микроорганизмов.
Микробное число водопроводной воды не должно превышать 50 колоний бактерий в 1 мл.
Его определяют методом посева на питательную среду – мясопептонный агар ( МПА ). Метод заключается в том, что в 1 мл воды определяют бактерии, которые способны расти на питательном агаре при температуре 370С в течение 24 ч., образуя колонии, видимые при увеличении в 2 – 5 раз. Проведенным таким образом анализом нельзя определить полностью все бактерии в воде, а только те, которые развиваются в условиях анализа. Поэтому, определение дает не абсолютную, а относительную бактериологическую характеристику воды. Этим методом можно сравнивать бактериальную зараженность разных мест водоисточника, а также одного места в разные времена года.
Аппаратура, реактивы: термостат; микроскоп; чашки Петри; питательная среда МПА; дистиллированная вода.
Материал: вода водоема и водопроводная вода.
Ход определения. В чашку Петри пипеткой вносят 1 мл исследуемой питьевой воды
( если исследуют сточную воду, ее разбавляют стерильной водой в несколько раз ), затем заливают пробу 10 – 12 мл остуженного питательного мясопептонного агара (МПА), имеющего температуру приблизительно 450С. Содержимое быстро перемешивают, осторожно наклоняя и вращая чашку по поверхности стола. Необходимо избегать образования пузырьков воздуха, незаметных частей дна чашки, попадания среды на края и крышку чашки. После застывания среды чашку помещают в термостат и выдерживают при температуре 370С в течение 24 часов. За это время в чашке Петри вырастают колонии, которые видны при увеличении в 2 – 5 раз. Обычно вырастает от 30 до 300 колоний.
Для подсчета числа колоний чашку кладут вверх дном на черный фон. Для ускорения подсчета числа колоний Х определяют число колоний в 1см2 (n) и умножают это число на площадь чашки S = π∙r
( r – радиус чашки ):
Х = n∙π∙r2
По полученным данным определяют степень загрязнения воды, пользуясь табл. 9.
Таблица 9
Степень загрязнения воды в зависимости от общего числа бактерий
Характеристика воды | Число бактерий в 1 мл |
| очень чистая чистая умеренно загрязненная загрязненная грязная очень грязная | а · 10 а · 102 а · 103 а · 104 а · 105 а · 106 |
«а» имеет значения от 1 до 9.
4.2. Определение количества бактерий группы Coli
Бактерии группы Coli являются постоянными обитателями кишечника человека и животных; постоянно и в большом числе выделяются во внешнюю среду; дольше, чем патогенные микроорганизмы сохраняют жизнеспособность в этой среде; более устойчивы к действию хлора, чем возбудители большинства инфекций. Поэтому их используют в виде санитарно-показательных микроорганизмов. Кишечная палочка для человека не опасна, но ее присутствие свидетельствует о загрязнении воды выделениями человека и вызывает подозрение о наличии в воде болезнетворных микробов (тифа, холеры, дизентерии и др.).
Определение кишечной палочки основано на ее способности сбраживать сахар. Если питательная среда содержит молочный сахар, то он сбраживается до молочной кислоты, которая разрушает соединение красителя фуксина с сульфитом. В местах роста колоний бактерий Coli получаются окрашенные фуксином красные блестящие бугорки, по числу которых судят о количестве бактерий Coli.
Анализ водопроводной и чистой природной воды проводят после предварительного концентрирования бактерий воды на мембранных фильтрах и выращивания их при
37 ±50С на среде Эндо. Общий вид чашки Петри с выросшими колониями на мембранном фильтре приведен на рис.4. Результаты выражают в виде коли-индекса - числа бактерий в 1 л воды или коли-титра - наименьшего объема воды ( в мл ), содержащего 1 кишечную палочку.
Коли-индекс водопроводной воды не должен превышать 3, а коли-титр 300 мл.
Аппаратура, реактивы: термостат; микроскоп; чашки Петри; питательная среда Эндо; дистиллированная вода.
Материалы: водопроводная вода и вода водоема.
Ход определения. В фильтровальный аппарат (рис.5) помещают стерильный мембранный фильтр и фильтруют 300 – 500 мл воды. Под мембранный фильтр подкладывают простерилизованный кружок из фильтровальной бумаги, смоченный стерильной водой. После окончания фильтрования фильтр снимают обожженным пинцетом с прибора и накладывают на поверхность среды Эндо, помещенной в чашку Петри. Чашку в перевернутом виде помещают в термостат при температуре 370С на 24 часа и затем подсчитывают колонии, окрашенные в красный цвет с металлическим блеском.
Формула для расчета:
Коли-индекс =
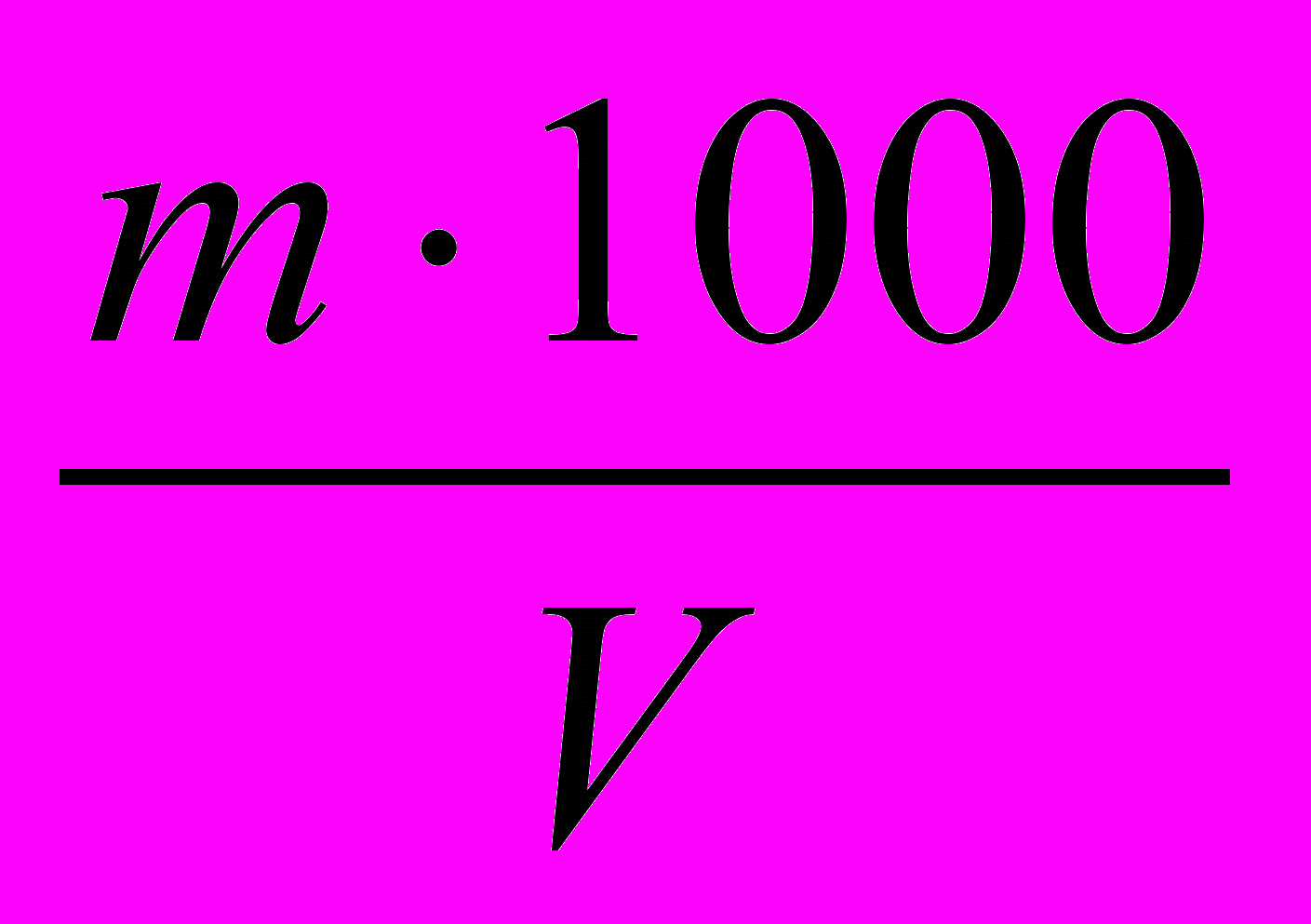 ,
, где m – количество бактерий,V – анализируемый объем воды, л
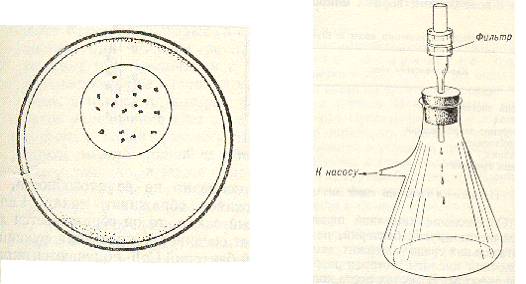
Рис.4. Общий вид чашки Петри Рис.5. Фильтровальный аппарат
с бактериями Coli на мембранном
фильтре
Приготовление питательных сред.
Подготовка мясо-пептонного агара (МПА) для определения общего числа микробов.
1. Приготовление мясной воды. В 1 л дистиллированной воды помещают 500 г мясного фарша (без жира и сухожилий), выдерживают 12 ч на холоде или 1 ч на водяной бане при температуре 50 - 60° С, нагревают до кипения, фильтруют через марлю или вату и доводят объем до 1 л, после чего разливают и стерилизуют в автоклаве при 120 ± 2° С. Так получают мясную воду.
2. Приготовление мясного бульона. К 1 л мясной воды добавляют 10 г пептона и 5 г соли. Нагревают до растворения и устанавливают рН в пределах 7,2 - 7,4, фильтруют, разливают в пробирки и флаконы, после чего стерилизуют в автоклаве при 120 ± 2° С в течение 20 мин.
З. Приготовление мясо-пептонного агара МПА. К 1 л мясного бульона прибавляют 15 г агара, затем нагревают на водяной бане до полного растворения агара, устанавливают рН = 7,2-7,4, фильтруют, разливают в пробирки и флаконы и стерилизуют в автоклаве при 120 ± 2° С в течение 20 мин при 1,1 ат.
Подготовка среды Эндо (фуксинсульфитного агара) для определения коли-индекса.
1. Приготовление сульфитно-спиртового раствора фуксина. Накануне проведения анализа готовят 10%-ный раствор основного фуксина в спирте. К 0,5 мл этого раствора прибавляют по каплям 10%-ный водный раствор сульфита натрия до получения ярко- розовой окраски.
2. Приготовление раствора лактозы. 0,5 г лактозы растворяют в 2 - З мл стерильной воды и нагревают на водяной бане в течение 5 мин.
З. Приготовление среды Эндо (фуксинсульфитного агара). К 100 мл расплавлениого мясо-пептонного агара прибавляют раствор лактозы и сульфитно-спиртовый раствор фуксина. Полученную среду тщательно перемешивают и разливают в чашки Петри.
Контрольные вопросы
Какие показатели определяют безопасность питьевой воды в эпидемиологическом отношении? Опишите методику определения общего количества бактерий в воде.
- Как определяют коли-титр и коли-индекс? Какие факторы влияют на данные показатели качества воды?
- Подсчет числа колоний на среде Эндо показал, что при посеве 1 мл сточной воды без разбавления выросло 3 колонии. Определите коли-индекс и коли-титр данной воды.
- Оцените качество хлорирования воды на водопроводной станции: микробное число 50; коли-индекс – 2; запах – хлорный, 1 балл.
- Оцените качество артезианской воды, предлагаемой для водоснабжения : запах и вкус – 2 балла; мутность – 0,5 мг/дм3; общая жесткость – 2,0 мг-экв/л; микробное число – 80; коли-индекс – 3.
- Для определения каких показателей качества воды используют фуксин- сульфитный агар?
Глава 2. ОЦЕНКА КАЧЕСТВА АТМОСФЕРНОГО ВОЗДУХА
Одним из важнейших объектов окружающей среды является атмосферный воздух. Устойчивость биосферы зависит от его чистоты. Загрязнение воздуха отрицательно влияет на растения, животных, людей, строения, оборудование и различные материалы.
В качестве наиболее распространенных и опасных были выявлены восемь категорий загрязнителей: 1 – взвешенные вещества, которые могут переносить другие загрязнители, растворенные в них или адсорбированные на поверхности частиц;
2 – углеводороды и другие летучие органические соединения; 3 – угарный газ ( СО ); 4 – оксиды азота ( NOx ); 5 – оксиды серы (в основном диоксид SO2 ); 6 – свинец и другие тяжелые металлы; 7 – озон и другие фотохимические окислители; 8 – кислоты (в основном серная и азотная).
Контроль за состоянием атмосферного воздуха включает в себя изучение источников загрязнения, исследование химических и фотохимических превращений загрязняющих веществ, выявление наиболее токсичных веществ, изучение распространения загрязнителей с воздушными потоками, отбор и анализ загрязнителей. Надежность контроля за загрязнением наряду с рассмотренными выше факторами зависит от способа отбора проб. В зависимости от предполагаемого загрязнения воздуха отбор проб может производиться с концентрированием или без него.
Работа №1. Определение запыленности воздуха
Пыль является аэрозолем. Аэрозоли представляют собой частицы вещества (твердые или жидкие) во взвешенном состоянии. Большое количество аэрозолей образуется в результате естественных природных процессов, но немалая их доля имеет антропогенное происхождение. Основной источник антропогенных аэрозолей- процесс горения. Энергетика и транспорт дают 2/3 общего количества антропогенных аэрозолей. Среди прочих источников аэрозолей – металлургические предприятия, производство строительных материалов, химические производства.
Нормативы по содержанию неорганической пыли в воздухе населенных мест: ПДКмр= 0,3мг/м3; ПДКСС = 0,1мг/м3.
Для количественной характеристики запыленности воздуха в настоящее время используется преимущественно весовой метод
( гравиметрия ). Через аналитический фильтр, находящийся в патроне (рис. 6), просасывают определенный объем запыленного воздуха.
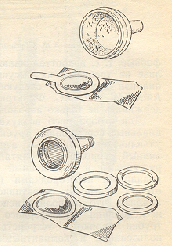
Рис. 6. Патроны для отбора проб пыли на фильтры
Массу всей витающей пыли без разделения на фракции рассчитывают по увеличению массы фильтра. Лучшими являются фильтры из ткани ФПП. Фильтры Петрянова обладают высокой эффективностью и малым аэродинамическим сопротивлением, их ткань обладает водоотталкивающими свойствами. Метод применяется для определения разовых и среднесуточных концентраций пыли в воздухе населенных пунктов и санитарно-защитных зон в диапазоне 0,04 – 10 мг/м3.
Аппаратура, реактивы: улавливающее устройство (фильтродержатель, фильтр из ткани ФПП, аспиратор для отбора проб, стакан-насадка на фильтродержатель); аналитические весы; эксикатор; пинцет; чашки стеклянные диаметром 10 см; барометр; психрометр; анемометр.
Материал: воздух населенного пункта.
Ход работы. Фильтр из ткани ФПП выдерживают в течение 40 – 60 мин. в весовой комнате, взвешивают, помещают в пакет и доставляют на место пробоотбора, где его вкладывают в фильтродержатель, который крепко завинчивают. Перед отбором проб проверяют герметичность фильтродержателя, для чего его входное отверстие закрывают пробкой и включают прибор: при герметичном присоединении расходомер воздуха показывает ноль.
Отбор проб проводят со скоростью 250 – 400 л/мин, чтобы навеска пыли на фильтре была не менее 4 мг. Отбор ведется не более 30 мин. После протягивания воздуха фильтр пинцетом извлекают из держателя, складывают вчетверо запыленной поверхностью внутрь и помещают в тот же пакет, из которого он был взят. В лаборатории фильтр выдерживают в течение 40 – 60 мин. при комнатной температуре и доводят до постоянной массы. Если отбор пробы проводился при относительной влажности, близкой к 100%, то фильтр помещают в стеклянной чашке в эксикатор с плавленым хлористым кальцием на 30 – 50 мин., а затем уже выдерживают при комнатной температуре 40 – 50 мин.
Концентрацию пыли С, мг/м3 вычисляют по формуле:
С =
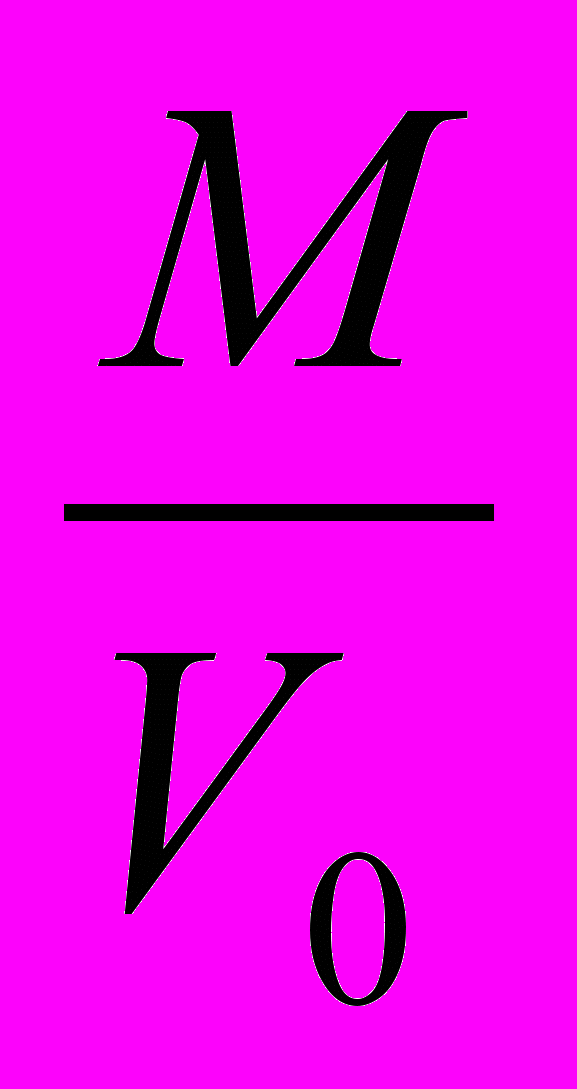 ,
,где М – масса пыли на фильтре, равная разности масс запыленного и чистого фильтра, мг; V0 – объем аспирированного воздуха, приведенный к нормальным условиям, м3.
Под нормальными условиями подразумевается температура 00С и атмосферное давление 1013 гПа ( 760 мм рт. ст. ):
V0 =
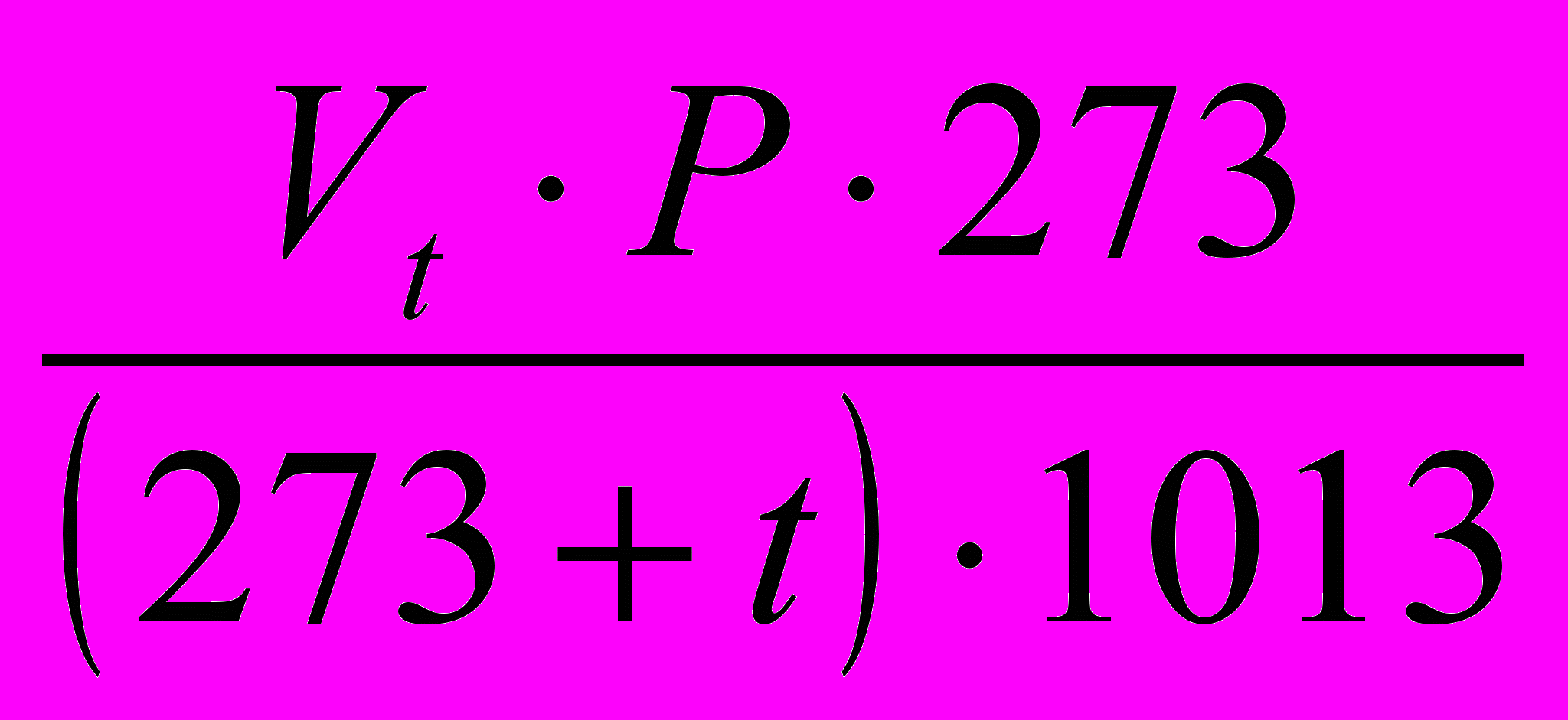 ,
,где Vt – объем аспирированного воздуха при температуре t и атмосферном давлении
Р гПа, м3; 273 – коэффициент расширения газов; 1013 – нормальное давление, гПа.
Контрольные вопросы
- Как производится отбор проб воздуха?
- От чего зависит выбор способа отбора проб воздуха?
- Дайте характеристику фильтрам из ткани ФПП.
- При температуре воздуха 240С, давлении 750 мм рт. ст. отобран воздух для лабораторного исследования в течение 20 мин. со скоростью 25 л/мин. Рассчитайте объем протянутого воздуха и приведите объем воздуха к нормальным условиям.
- Как рассчитывается содержание пыли?
- Отобрано 100 дм3 воздуха. Масса фильтра до отбора – 0,3452 г, после отбора – 1,5848 г. Рассчитайте концентрацию пыли и сравните с ПДК ( 6 мг/м3 ).
- Пропущено 600 дм3 воздуха при температуре 160С, давлении 742 мм рт. ст. Масса задержанной пыли 10 мг. Рассчитайте концентрацию пыли, сопоставьте с гигиеническими нормами.
Работа №2. Определение концентрации диоксида азота в атмосферном воздухе
Азот образует смесь различных оксидов, но лишь NO и NO2 имеют значение как атмосферные загрязнители. Обычно суммарные концентрации NO и NO2 в атмосфере обозначаются как NOx .
Оксиды азота играют основную роль в образовании фотохимического «смога», влияют они и на разрушение озонового слоя, ведут также к образованию кислотных дождей. Загрязнение атмосферы оксидами азота в целом сравнительно невелико. Но в районах с развитой химической промышленностью имеются локальные зоны повышенного содержания NO и NO2 в воздухе.
Монооксид азота NO – бесцветный газ, образующийся в малых количествах в цилиндрах двигателей внутреннего сгорания при взаимодействии О2 с N2 . В дальнейшем он окисляется кислородом до двуокиси азота NО2.
Диоксид азота представляет собой коричнево-бурый газ, ядовитый, с неприятным запахом. При растворении NO2 в воде образуется азотная кислота.
Газообразный NO2 токсичен ( 2 класс опасности ), является также сильным коррозионно-активным агентом.
Предельно допустимая концентрация NO2 максимально разовая составляет 0,085 мг/м3, среднесуточная - 0,04 мг/м3.
Метод определения содержания диоксида азота в воздухе с реактивом Грисса-Илосвая основан на взаимодействии двуокиси азота и сульфаниловой кислоты с образованием диазосоединения, которое, реагируя с α-нафтиламином, дает азокраситель. Последний окрашивает раствор от бледно-розового до красно-фиолетового цвета. По интенсивности окраски раствора определяют количество NO2.
Чувствительность определения 0,1 мкг в анализируемом объеме пробы. Диапазон измеряемых концентраций составляет 0,03 – 0,64 мг/м3 при отборе пробы воздуха 5 л.
Аппаратура, реактивы: улавливающее устройство; аспиратор для отбора проб, поглотительный прибор Рыхтера; аналитические весы; барометр; термометр; фотоколориметр; калий йодистый, х.ч.; натрий азотистокислый, х.ч.; поглотительный раствор: 20 г KI растворяют в 250 г воды. Полученный раствор должен быть бесцветным и храниться в банке из темного стекла. Срок хранения 2 недели; натрий сернистокислый, х.ч., 0,06%-ный раствор. 0,03 г Na2SO3 растворяют в 50 мл воды. Раствор готовят перед анализом; уксусная кислота, х.ч., 12%-ный раствор. 64 мл концентрированной кислоты помещают в мерную посуду на 500мл и доводят до метки водой; сульфаниловая кислота, ч.д.а., 5г сульфаниловой кислоты растворяют в 150мл 12%-ного раствора уксусной кислоты. Хранят раствор в плотно закрытой склянке из темного стекла; α-нафтиламин, ч.д.а. 0,2 г α-нафтиламина растворяют в 20мл воды при нагревании на водяной бане до образования лиловых капель на дне колбы. Раствор осторожно сливают в темную склянку, оставляя осадок в колбе, и приливают к раствору 150 мл 12%-ного раствора уксусной кислоты; составной реактив (реактив Грисса-Илосвая). Перед анализом смешивают растворы α-нафтиламина и сульфаниловой кислоты в отношении 1:1; исходный стандартный раствор: 2 – 3 г азотистокислого натрия растирают и сушат при температуре 50 – 600С в течение 2 часов. Навеску NaNO2 0,15 г растворяют в мерной колбе емкостью 100 мл 1мл полученного раствора соответствует 1000 мкг NO2; раствор, 1мл которого соответствует 10 мкг NO2, готовят разведением стандартного раствора поглотительным раствором в 100 раз; рабочий стандартный раствор. Готовят 10-кратным разбавлением раствора, содержащего 10 мкг/мл NO2 поглотительным раствором. 1 мл рабочего раствора соответствует 1 мкг NO2. Исходный стандартный раствор сохраняется в течение 2 недель в склянке из темного стекла. Рабочий стандартный раствор готовят перед анализом.
Материал: воздух населенного пункта.
Ход работы. Для определения разовой концентрации NO2 исследуемый воздух протягивают через поглотитель Рыхтера (рис.7), наполненный 6 мл поглотительного раствора, со скоростью 0,25 л/мин в течение 20 мин.
Во время отбора пробы следует избегать освещения поглотительного прибора солнечными лучами. Срок хранения отобранных проб не более 2 суток.
Рис.7. Поглотитель Рыхтера
В лаборатории уровень раствора в поглотительном приборе доводят до метки 6 мл дистиллированной водой. Для анализа 5 мл раствора из каждой пробы переносят в пробирку и добавляют по 0,5 мл составного реактива.
Содержимое пробирок тщательно встряхивают и через 20 мин.
( непосредственно перед измерением ) в пробирки приливают по 5 капель 0,06%- ного раствора Na2SO3 и еще раз встряхивают. Оптическую плотность измеряют на фотоколориметре (рис.8) в кюветах толщиной 10 мм при длине волны 540 нм относительно воды. Время от добавления составного реактива до измерения оптической плотности всех проб должно быть одинаковым.
Рис. 8 Прибор КФК-2 ( одноканальный)
Количество NO2 в пробах находят по калибровочному графику. Одновременно проводятся измерения оптической плотности нулевой пробы.
Расчет концентраций диоксида азота в воздухе проводят по формуле:
С =
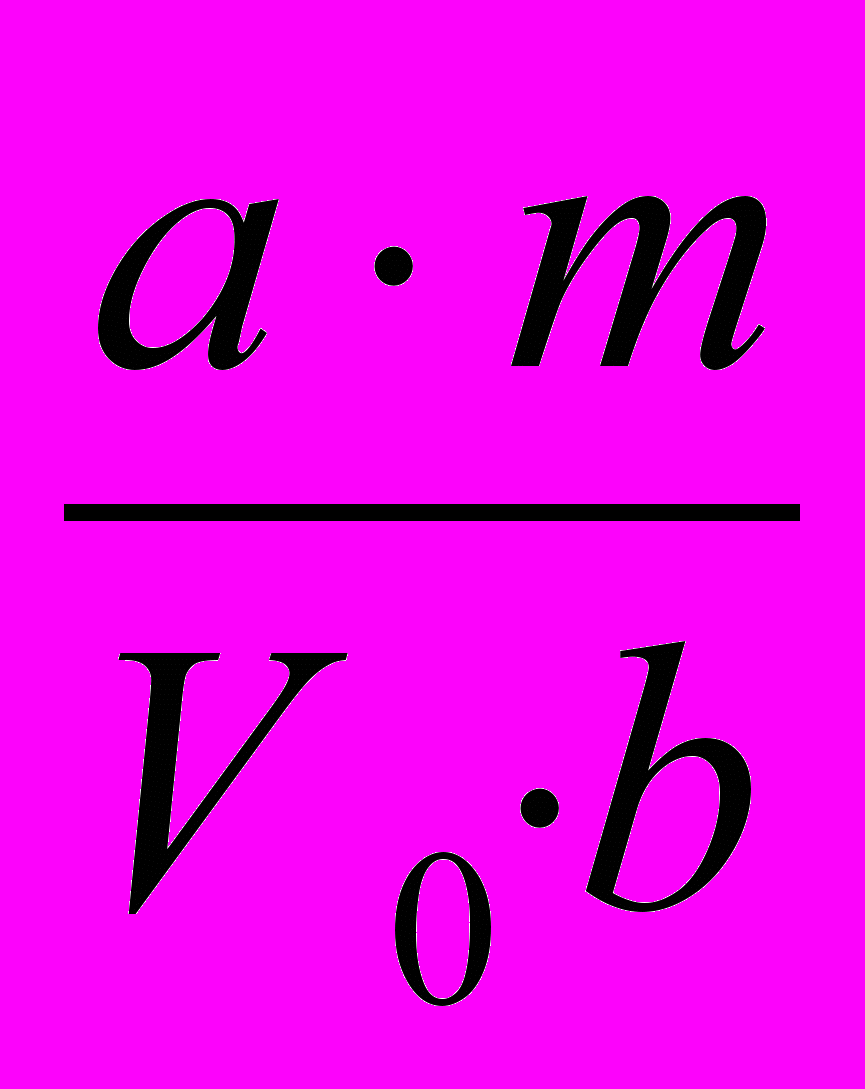 ,
,где
 – общий объем пробы в поглотительном приборе ( 6 мл );
– общий объем пробы в поглотительном приборе ( 6 мл );b – объем пробы для анализа ( 5 мл ); m – количество NO2 в пробе, найденное по калибровочному графику, мкг; V0 – объем протянутого воздуха, приведенный к нормальным условиям, л.
Построение калибровочного графика
В мерные колбы на 50 мл наливают 1, 2, 4, 6, 8, 10, 20 мл рабочего стандартного раствора ( 1 мкг/мл ) и разбавляют до метки поглотительным раствором. Концентрация NO2 в 5 мл стандартного раствора в мерных колбах составляет соответственно 0,1; 0,2; 0,4; 0,6; 0,8; 1,0; 2,0 мкг.
Для приготовления шкалы стандартов отбирают в пробирки по 5 мл каждого стандарта и определяют их оптическую плотность.
Контрольные вопросы
- Какие виды ПДК существуют для воздуха?
- Напишите формулу приведения отобранного объема воздуха к нормальным
( стандартным ) условиям.
- Напишите формулу для расчета концентраций газов в воздухе
( в мг/м3 ).
- В чем заключается принцип метода определения оксидов азота? Какие реактивы применяются в качестве стандартных и поглотительных растворов?
- Как проводится отбор проб воздуха и готовится шкала стандартов для определения оксидов азота?
- Для определения оксидов азота воздух со скоростью 0,2 л /мин в течение 5мин протягивается через 10 см3 поглотительного раствора. При фотометрии 1 см3 пробы обнаружено 0,5 мкг оксида азота. Вычислите концентрацию оксида азота и сопоставьте с ПДК.
7. Для определения ртути через гофрированную трубку протянуто
200 дм3 воздуха при температуре 150С и давлением 746 мм рт.
ст. Общий объем пробы составляет 2 см3. При фотометрии 1 см3
пробы окраска совпала с пробиркой стандартной шкалы,
содержащей 1,0 мкг ртути. Определите концентрацию
ртути и сопоставьте с ПДК.
- Для определения аммиака воздух со скоростью 0,5 л/мин
протягивают в течение 5 мин через 10 см3 поглотительного
раствора. При фотометрии 1 см3 пробы обнаружено 4,0 мкг
аммиака. Определите концентрацию аммиака в воздухе и
сопоставьте с ПДК.
- Наметьте основные пути снижения концентрации токсичных веществ в атмосферном воздухе и воздухе промышленных предприятий.
Работа №3. Определение загрязнения атмосферного воздуха по физико-химическим характеристикам снега
Оценка загрязнения окружающей среды по степени загрязнения снежного покрова
является широко используемым во всем мире приемом проведения мониторинга окружающей среды. Подобные исследования позволяют получать четкую картину экологической обстановки на значительных территориях в течение ряда лет. Такие исследования могут включать оценку степени запыленности воздуха, загрязнения тяжелыми металлами, нитратами, сульфатами, хлоридами, органическими веществами и представляют собой основу для осуществления рекреационных мер по восстановлению экологического благополучия природы, общества, человека.
Аппаратура: фотоэлектроколориметр; рН-метр; аналитические весы; плоскодонные колбы; химические воронки; складчатые фильтры; полиэтиленовые бутыли из под питьевой воды емкостью 1,5 – 2л.
Реактивы: азотнокислое серебро, 10%-ный раствор; трилон Б, 0,05 М; эриохром черный Т; салициловокислый натрий; едкий натр, 10Н раствор; гликолевый реагент; соляная кислота.
Подготовка к работе. Перед началом исследования составляют схему обследуемой территории с указанием выбранных мест отбора снега, основных зданий и сооружений и их назначения. Мест отбора проб снега должно быть не менее 10. Ориентируясь по схеме, отбирают образцы снега в выбранных местах на площадках размером не менее 1 м2. Количество снега должно составлять свыше 600 – 800 г. В качестве емкостей для отбора снега удобно пользоваться полиэтиленовыми бутылями на 1,5 – 2 л из-под питьевой воды, для чего у них отрезают ножницами верхнюю суживающуюся часть
( снег в емкости должен быть плотно утрамбован ). Каждая емкость должна быть пронумерована в соответствии с номерами мест отбора проб снега, номер закреплен на емкости скотчем .
Для таяния снега собранные образцы оставляют при комнатной температуре до следующего занятия. В день сбора образцов снега студенты готовят к следующему занятию складчатые фильтры, плоскодонные колбы и химические воронки. Каждый складчатый фильтр взвешивают на аналитических весах. Вес бумажного фильтра и номер пробы записывают на краю фильтра карандашом. Параллельно нумеруют плоскодонные колбы в соответствии с номерами проб.
3.1. Определение запыленности территории.
Ход работы: После того как снег растаял, его фильтруют через предварительно взвешенный складчатый фильтр, перенося осадок количественно на фильтр (рис.9).
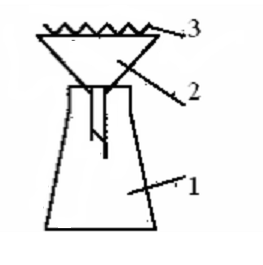
Рис. 9. Прибор для фильтрования талого снега:
1-плоскодонная колба; 2- химическая воронка; 3 – бумажный фильтр
Измеряют объем талого снега каждой пробы. Бумажные фильтры помещают в сушильный шкаф, нагретый до температуры 60 – 800С, или оставляют при комнатной температуре до следующего занятия. После высушивания фильтры взвешивают и определяют массу осадка. Поскольку объем талого снега во всех образцах разный, то, для того чтобы можно было провести сравнительную оценку запыленности территории, каждую величину пересчитывают на 1 л ( кг ) талого снега:
Количество пыли на кг талого снега =

3.2. Определение рН талого снега
В работе используют индикаторную бумагу ( интервал рН = 1 ÷ 14 ) или рН-метр; рН талого снега можно определить во время фильтрования.
3.3. Определение содержания органических примесей
Ход работы. Количество органических примесей можно определить, пока происходит фильтрование талого снега. Это значение оценивают по величине поглощения светового потока органическими веществами при 364 нм , которое происходит в соответствии с законом Бугера-Ламберта-Бера:
D = lgI0/Ic = eCl,
где D – оптическая плотность раствора; I0 – интенсивность света, падающего на раствор; Ic – интенсивность света, прошедшего через раствор; e - молярный коэффициент светопоглощения; С – концентрация растворенного вещества, г-моль/л; l - толщина слоя раствора , см.
Данное исследование проводят при помощи фотоэлектроколориметра КФК-2, принцип работы которого следующий. Колориметр имеет два кюветных отделения: одно - для исследуемого раствора, другое – для растворителя. Первоначально в кюветное отделение для растворителя помещают дистиллированную воду и «зануляют» прибор ( величина поглощения на табло должна быть равна нулю ), благодаря чему при измерении величины поглощения светового потока исследуемым раствором поглощение самой водой автоматически вычитается, а регистрируемое значение соответствует только поглощению органических веществ.
3.4 Качественное определение ионов хлора
Метод основан на осаждении хлорида серебра по реакции:
AgNO3 + Cl - = AgCl¯ + NO3-
В пробирку наливают 5 мл пробы профильтрованного талого снега и добавляют 3 капли 10%-ного раствора азотнокислого серебра. Примерное содержание хлор-иона определяют по внешнему виду осадка:
- опалесцирующий ( слабая муть ) – содержание Cl - 1 – 10 мг/л;
- сильная муть – содержание Cl - 10 – 50 мг/л;
- хлопья, осаждающиеся не сразу – содержание Cl - 50 – 100мг/л;
- белый объемный осадок – содержание Cl - более 100 мг/л.
3.5. Определение общей жесткости в пробах снега
Метод представляет собой комплексонометрическое титрование и основан на вытеснении эриохрома черного Т из комплекса с ионами кальция и магния этилендиаминтетрауксусной кислотой – процесс, сопровождающийся изменением цвета раствора с фиолетового на голубой (рис.10).
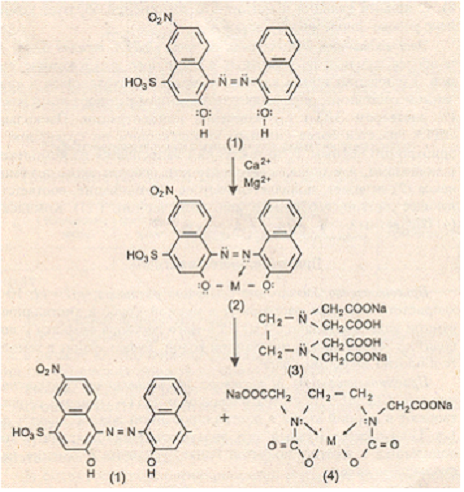
Рис. 10. Схема химических превращений при определении общей жесткости воды
Эриохром черный Т ( 1 ) - представляет собой азоткраситель, обладающий сопряженной системой двойных связей, обеспечивающей окраску данного соединения ( голубой цвет при рН более 8 ). С ионами кальция и магния это соединение образует комплекс розово-фиолетового цвета ( 2 ).
Этилендиаминтетрауксусная кислота ( ЭДТА, трилон Б ) ( 3 ) – наиболее сильный из известных в настоящее время комплексонов. Количество ионов кальция и магния, находящихся в связанном состоянии, определяют титрованием раствора комплекса
( 2 ) раствором ЭДТА ( 3 ) известной концентрации. Поскольку ЭДТА является более сильным комплексоном по сравнению с эриохромом черным Т, то последний вытесняется из комплекса с металлами, и в точке эквивалентности розовая окраска комплекса ( 2 ) исчезает, появляется голубое окрашивание, соответствующее раствору свободного эриохрома черного Т ( 1 ). Комплекс ( 4 ) бесцветный.
Ход работы. Отбирают 10 мл исследуемой пробы в плоскодонную коническую колбу на 100 мл, добавляют 1 – 2 мл аммиачного буфера с рН = 8 и на кончике шпателя краситель эриохром черный Т до получения светло-розового окрашивания и титруют 0,05 М раствором трилона Б до получения голубого цвета раствора. Жесткость воды в
мг-экв/л рассчитывают по формуле:
Жесткость, мг-экв/л =
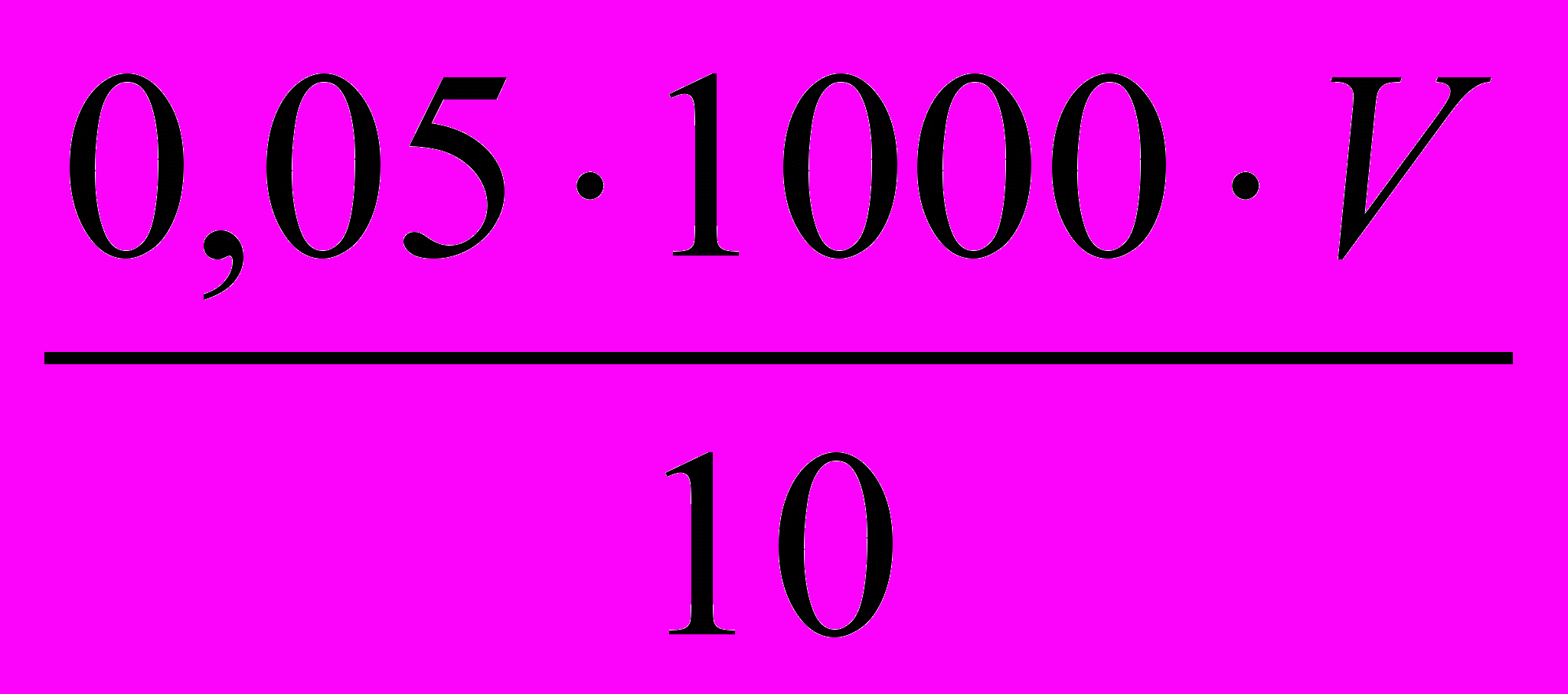 ,
,где 0,05 – молярность трилона Б; V – объем трилона Б, пошедший на титрование, мл;
1000 – коэффициент пересчета в л; 10 – объем пробы воды, взятой на анализ, мл.
3.6. Определение нитратов в пробах снега.
Метод основан на реакции нитратов с с салициловокислым натрием в присутствии серной кислоты с образованием соли нитросалициловой кислоты, окрашенной в желтый цвет.
Ход работы. 10 мл исследуемой воды помещают в фарфоровую чашку. Прибавляют 1 мл раствора салициловокислого натрия и выпаривают досуха. После охлаждения сухой остаток увлажняют 1 мл концентрированной серной кислоты, тщательно растирают его стеклянной палочкой и оставляют на 10 мин. Затем добавляют 5 – 10 мл дистиллированной воды и количественно переносят в мерную колбу вместимостью 50 мл. Прибавляют 7 мл 10 Н раствора едкого натра, доводят объем дистиллированной водой до метки и перемешивают. В течение 10 мин после прибавления едкого натра окраска не изменяется. Сравнение интенсивности окраски исследуемой пробы производят фотометрическим методом, измеряя оптическую плотность раствора
( фиолетовый светофильтр ).
Содержание нитратов определяют по калибровочному графику в мг/л ( в работе желательно пользоваться готовой предварительно полученной стандартной кривой ).
3.7. Определение сульфат-ионов
Метод основан на определении сульфат-иона в виде BaSO4 в солянокислой среде с помощью гликолевого реагента:
BaCl2 + SO
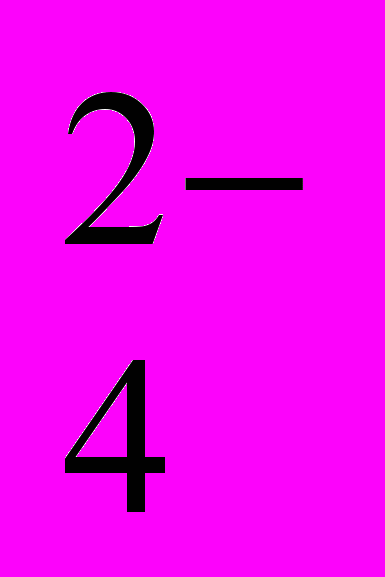 = BaSO4¯ + 2Cl –
= BaSO4¯ + 2Cl –Гликоль, введенный в реакционную смесь при осаждении сульфата бария, стабилизирует образующуюся суспензию BaSO4 и делает возможным турбидиметрическое определение сульфатов.
Ход работы: К 5 мл талого снега после фильтрования добавляют 1 – 2 капли соляной кислоты ( 1 : 1 ), 5 мл гликолевого реагента и тщательно перемешивают. Через 30 мин измеряют оптическую плотность полученного раствора на фотоэлектроколориметре или спектрофотометре в кюветах толщиной 20 мм при l = 364 нм. В качестве раствора сравнения используют исследуемую пробу с добавлением гликолевого реагента, приготовленного без хлорида бария. Содержание сульфатов находят по калибровочной кривой. Оптимальные интервалы концентраций для турбидиметрического определения сульфат-иона находятся в интервале 2 – 25 мг/л.
Все результаты определений записываются в таблицу 10.
Таблица 10
Физико-химические характеристики снега
| № про бы | Объем талого снега, мл | Масса пыли | Величина поглоще- ния орга- нических примесей D364 | Жесткость талого снега, мг-экв/л | Содержа- ние сульфат- ионов, мг/л | Содержа- ние ионов хлора, мг/л | Содержа- ние нитра- тов, мг/л | |
| в про- бе | в л | |||||||
| | | | | | | | | |
В выводах по проделанной работе должно быть отражено:
1. определение наибольшего экологического риска в одной из точек исследования;
2. объяснение, откуда появилось загрязнение в том или ином пункте отбора проб сульфатами, ионами хлора, органическими веществами, ионами кальция и магния, нитратами;
3. выявление наиболее экологически благоприятных зон.
Контрольные вопросы
1. Какие загрязнения снежного покрова следует ожидать в радиусе действия:
- автотранспорта; - теплоэлектростанций; - предприятий черной и цветной металлургии;
- предприятий органического синтеза.
2. Почему надо пересчитывать результаты на 1 л талого снега, почему нельзя сравнивать исходные данные?
3. В чем заключается принцип комплексонометрического определения жесткости воды?
4. Каковы характерные реакции на ионы хлора и сульфат-ионы?
5. На чем основан метод турбидиметрического анализа сульфат-ионов?
6. Объясните изменение цвета раствора при титровании пробы воды раствором ЭДТА.
7. Напишите формулу этилендиаминтетрауксусной кислоты, объясните ее способность образовывать прочные комплексы.
8. Напишите формулу эриохрома черного Т и объясните способность этого соединения образовывать комплексы с металлами.
