Модуль Поверхневі явища. Дисперсні системи. Високомолекулярні речовини та їх розчини Донецьк 2011
| Вид материала | Документы |
- Тема. Будова речовини. Атоми та молекули. Взаємодія молекул. Явище дифузії. Мета, 108.53kb.
- Сучасна колоїдна хімія це велика, самостійна частина хімічної науки, що вивчає дисперсний, 136.55kb.
- Науково-практичної інтернет-конференції економічна політика країн єс 17 жовтня 2011, 3470.85kb.
- Янки, заочеревинного простору, малого тазу, верхніх та нижніх кінцівок методичні вказівки, 1038.09kb.
- Ренція «комплексне використанння природних ресурсів» (12 грудня 2011 року, м. Донецьк,, 2132.33kb.
- З хімії для вступу на перший курс навчання до Вінницького національного технічного, 99.03kb.
- Програма для загальноосвітніх навчальних закладів 7 9 класи пояснювальна записка, 286.52kb.
- Завідувач кафедри М. П. Рагозін затверджено: на засіданні навчально-видавничої ради, 230.44kb.
- Явища природи. Механічні явища. 5 клас. Мета, 60.42kb.
- Назва реферату: Значення м’ясних страв у харчуванні, їх класифікація Розділ, 96.33kb.
Заняття 16.
Поверхневі явища. Когезія. Адгезія. Змочування. Адсорбція. Ізотерми адсорбції.
Актуальність теми
Поверхневими називають явища, які спостерігаються на поверхні поділу фаз гетерогенних систем. Їх можна поділити на дві групи. До першої групи відносяться явища, пов’язані зі зміною форми поверхні поділу (змочування, адгезія). До другої групи – явища, пов’язані зі зміною складу поверхневого шару (адсорбція).
Різноманітні явища, які виникають на межі поділу фаз – змочування, адгезія, адсорбція та інші мають велике значення для фармації. Їх вивчення необхідно для розуміння технології виробництва, очищування, вибору умов зберігання лікарських речовин та лікарської сировини, для вивчення життєво необхідних біохімічних реакцій, в тому числі явищ, які виникають в живих організмах при введенні ліків. Наприклад, на процес перетравлювання жирів впливають солі жовчних кислот, які мають дуже низьке поверхневе натягнення, та є дуже добрими емульгаторами жирів. Жири в вигляді емульсій легко засвоюються.
Цілі навчання
Загальна мета:
ВМІТИ трактувати особливості будови та складу поверхневого шару, адсорбцію на межі поділу фаз, будову молекул поверхнево-активних речовин.
Конкретні цілі:
ВМІТИ:
- Трактувати різноманітність поверхневих явищ.
- Трактувати абсорбційні явища, адсорбцію на межі поділу тверде тіло – газ.
- Інтерпретувати рівняння, характерні для поверхневих явищ та зв'язок між ними.
- Інтерпретувати вплив ПАР на лікарські засоби та їх використання в фармації.
- Розраховувати параметри адсорбції (питому площу поверхні, кількість речовини, що адсорбується, тощо).
Зміст навчання
Теоретичні питання:
- Поверхневі явища та їх значення у фармації. Змочування. Адгезія. Когезія.
- Поверхнева енергія та поверхневий натяг.
- Сорбційні процеси та їх класифікація.
- Адсорбція на межі поділу тверде тіло - газ.
- Поверхнево-активні і поверхнево-інактивні речовини.
- Ізотерма поверхневого натягу розчинів поверхнево-активних речовин (ПАР).
- Емпіричне рівняння адсорбції Фрейндліха, його практичне застосування у фармації.
- Поверхнева активність, її визначення. Правило Дюкло-Траубе.
- Теорія мономолекулярної адсорбції Ленгмюра. Рівняння ізотерми адсорбції Ленгмюра, його виведення і аналіз.
- Будова мономолекулярного шару. Визначення розмірів молекули ПАР.
- Теорія полімолекулярної адсорбції (БЕТ, Поляні).
- Хроматографічний метод аналізу.
- Використання адсорбції та ПАР в фармації.
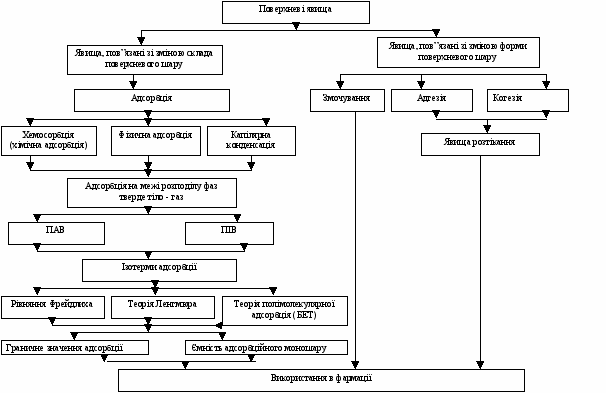
Граф логічної структури теми «Поверхневі явища. Адсорбція. Ізотерми адсорбції»
Джерела інформації
Основна література:
- Фізична і колоїдна хімія / В.І. Кабачний, Л.К. Осипенко, Л.Д. Грицан та ін.; Під ред. В.І.Кабачного. – Харьків: вид-во УукФА „Прапор”, 1999. –с. 220-246.
- Физическая и коллоидная химия/ В.И. Кабачный, л.к. Осипенко, Л.Д. Грицан; Под ред. В.И. Кабачного.- Харьков: изд-во НФаУ, 2005. – с. 202-209; 231-233.
- Фізична та колоїдна хімія. Збірник задач / В.І. Кабачний, Л.К. Осипенко, Л.Д. Грицан та ін.; Під ред. В.І.Кабачного. – Харьків: вид-во НФАУ „Золоті сторінки”, 2001. – с. 124-126.
- Лекції з фізичної та колоїдної хімії.
Додаткова література:
- Физическая и коллоидная химия / М.И. Равич-Щербо, В.В.Новиков.; Под ред. М.И.Равич-Щербо.- Москва: изд-во «Высшая школа», 1964.- с. 178-186.
- Физическая и коллоидная химия / М.И. Равич-Щербо, В.В.Новиков.; Под ред. М.И.Равич-Щербо.- Москва: изд-во «Высшая школа», 1975.- с. 153-168.
- Биофизическая химия / Л.П. Садовничая, В.Г. Хухрянский, А.Я. Цыганенко; Под ред. Л.П. Садовничая.- Киев: изд-во „Высшая школа”, 1986. – с.166-183.
Орієнтовна основа дії
Алгоритм рішення задач з фізичної хімії:
- Вивчити уважно умови завдання: визначити, з якими величинами доведеться проводити обчислення, позначти їх буквами, встановити одиниці їх вимірювання, числові значення, визначити, яку величину потрібно знайти. Записати дані задачі у вигляді коротких умов.
- Якщо в умовах завдання йде мова про взаємодію речовин, записати рівняння реакції (реакцій) і зрівняти його (їх) коефіцієнтами.
- З'ясувати кількісні співвідношення між даними задачі і величиною, що знаходиться. Для цього розділити свої дії на етапи, почавши з питання задачі, з'ясування закономірності, за допомогою якої можна визначити невідому величину на останньому етапі обчислень.
- Якщо у вихідних даних не вистачає будь-яких величин, подумати, як їх можна обчислити, тобто визначити попередні етапи розрахунку. Цих етапів може бути декілька.
- Визначити послідовність всіх етапів вирішення задачі, записати необхідні формули розрахунків.
- Підставити відповідні числові значення величин, перевірити їх розмірності і провести обчислення.
Набір завдань для перевірки досягнення конкретних цілей навчання
Тест 1
Порошки, які містять екстракт красавки та активоване вугілля, мають знижену терапевтичну активність. Яке поверхневе явище впливає на знижену активність?
А. Адсорбція
В. Десорбція
С. Адгезія
D. Когезія
Е. Розтікання
Тест 2
В медичній практиці активоване вугілля призначають при різноманітних отруєннях. Для поглинання надлишку газів в травному тракті він є основним адсорбентом. Як називають процес хімічної взаємодії між молекулами адсорбату та активними центрами адсорбенту?
А. Адсорбція
В. Сольватація
С. Десорбція
D. Возгонка
Е. Хемосорбція
Тест 3
Перед студентами-фармацевтами була поставлена задача розрахувати адсорбцію на твердих адсорбентах виходячи з експериментальних даних. Яке рівняння може бути використано для кількісної характеристики адсорбції на межі поділу “тверде тіло- газ”?
А. Релея
В. Фрейндлиха
С. Гиббса
D. Шишковського
Е. Гельмгольца-Смолуховського
Тест 4
В якості основ для приготування свічок та мазєй, стабілізації емульсій та в якості солюблізаторів використували ПАР, ураховуючи коефіцієнт Траубе. Цей коефіцієнт дорівнює:
А. 1-2
В. 2-3
С. 0-1
D. 3-3,5
Е. 4-4,5
Тест 5
В фармацевтичній лабораторії проводилися дослідження питомої поверхні силікагелю при низькотемпературній адсорбції різноманітних газів. Яка теорія адсорбції допускає утворення полімолекулярних шарів?
А. Теорія Ленгмюра
В. Теорія Арреніуса
С. Теорія БЕТ
D. Теорія Гіббса
Е. Теорія Ребіндера
Тест 6
Провізор-аналітик вибирає адсорбент для проведення адсорбції ПАВ. Який адсорбент найкраще адсорбує ПАВ з водних розчинів?
А. Целюлоза
В. Кварц
С. Бентоніт
D. Активоване вугілля
Е. Силікагель
Тест 7
Поверхнева активність біологічних розчинів нижча, ніж води, тому гідрофобні речовини будуть накопичуватися у стінок судин, тим самим полегшуючи проникливість скрізь мембрану. Таким чином буде утворюватися поверхневий натяг, на який впливає довжина вуглеводневого радикалу. Яким правилом буде описуватися ця залежність?
А. Вант-Гоффа
В. Дюкло-Траубе
С. Антонова
D. Шульце-Гарді
Е. Ребиндера
Тест 8
Площа поверхні 1 г активного вугілля становить 1000м2. Яка кількість аміаку (в м3) може адсорбуватися на поверхні 45 г активного вугілля при 298 К і 1,01∙105 Па? Діаметр молекули аміаку дорівнює 3∙10-10. Приймають, що молекули торкаються одна до одної в площині так, що центри чотирьох сусідніх сфер розміщуються в кутах квадрату.
А. 0,0203 м3
B. 0,011 м3
C. 1,0440 м3
D. 2,055 м3
E. 0,0111 м3
Еталони відповідей до рішення цільових навчальних завдань:
Тест 1-А,Тест 3- В, Тест 6- А,
Тест 8 - A
| Дано: S = 1000м2 m пов= 45 г Т= 298 К р=1,01∙105 Па d = 3∙10-10 | Розв’язання: За задачею молекули торкаються одна до одної в площині так, що центри чотирьох сусідніх сфер розміщуються в кутах квадрату. 1) 4 молекули займають площу (2d)2= 4 d2 кількість молекул в 1 квадраті = площа поверхні діаметр молекули х= 4∙1000/ 4∙(3·10-10)2= 4000/ 4∙9·10-20 = 0,11·1023 молекул |
| V =? |
2) На поверхні 1 г вугілля адсорбується 0,11·1023 молекул, тоді 45 г сілікагелю будуть адсорбувати 45∙0,11·1023= 5∙1023
3) На поверхні 45 г вугілля адсорбується 5∙1023 молекул або 5∙1023/ 6,02∙1023= 0,83 моль
- ρV = nRT V= nRT/ρ
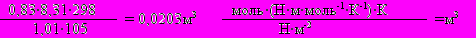
Відповідь: На поверхні асорбується 0,0203 м3.
Короткі методичні вказівки до роботи на практичному занятті
На початку заняття перевіряється підготовленність студентів до заняття шляхом усного опитування, або тестування. Далі студенти студенти працюють самостійно у відповідності до ООД, викладених у методичних вказівках. Рішення ситуаційних задач оформлюється в робочому журналі. Далі проводиться поточний контроль за темою (набори тестів). Потім розглядаються результати самостійної роботи, аналізуються помилки, підводяться підсумки заняття.
