Сафронова дарья александровна репродуктивное здоровье женщин после органосохраняющих операций на яичниках 14. 01. 01 – Акушерство и гинекология автореферат диссертации на соискание ученой степени кандидата медицинских наук Москва – 2011
| Вид материала | Автореферат диссертации |
- Гнойно-септические заболевания послеродового периода: комплексная диагностика, лечение, 659.23kb.
- Каткова надежда юрьевна ведение беременности и родов при плацентарной недостаточности, 651.9kb.
- Акинфиев Сергей Николаевич автореферат диссертации, 1335.17kb.
- L. в экосистемах баренцева моря >03. 02. 04 зоология 03. 02. 08 экология Автореферат, 302.63kb.
- Автореферат диссертации на соискание ученой степени, 267.76kb.
- «Связи с общественностью в условиях чрезвычайных ситуаций» Аннотация к диссертации, 83.66kb.
- Автореферат диссертации на соискание ученой степени кандидата медицинских наук, 321.48kb.
- Автореферат диссертации на соискание ученой степени, 331.91kb.
- Автореферат диссертации на соискание ученой степени, 378.33kb.
- Эволюция лирического героя в поэзии м. Турсун -заде, 1088.86kb.
На правах рукописи
САФРОНОВА
ДАРЬЯ АЛЕКСАНДРОВНА
РЕПРОДУКТИВНОЕ ЗДОРОВЬЕ ЖЕНЩИН ПОСЛЕ ОРГАНОСОХРАНЯЮЩИХ ОПЕРАЦИЙ НА ЯИЧНИКАХ
14.01.01 – Акушерство и гинекология
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
кандидата медицинских наук
Москва – 2011
Работа выполнена в Государственном бюджетном образовательном учреждении высшего профессионального образования «Российский национальный исследовательский медицинский университет имени Н.И. Пирогова Минздравсоцразвития России»
^ Научный руководитель:
доктор медицинских наук,
профессор Соломатина Антонина Андреевна
Официальные оппоненты:
доктор медицинских наук,
профессор ^ Духин Армен Олегович
доктор медицинских наук,
профессор Савченко Татьяна Николаевна
Ведущая организация:
ГУЗ «Московский областной научно-исследовательский институт акушерства и гинекологии» Министерства здравоохранения Московской области
Защита состоится «19» декабря 2011 года в 14.00 на заседании диссертационного совета Д 208.072.12 при ГОУ ВПО РГМУ по адресу: 117997, г. Москва, ул. Островитянова, д. 1.
С диссертацией можно ознакомиться в библиотеке ГОУ ВПО РГМУ по адресу: 117997, г. Москва, ул. Островитянова, д. 1
Автореферат разослан «1» ноября 2011 года
Ученый секретарь диссертационного совета
доктор медицинских наук, профессор Хашукоева Асият Зульчифовна
^ ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность исследования. В последнее десятилетие отмечается рост доброкачественных образований яичников с 6-11 до 19-25% (Гайдуков С.Н., 2006; Шабрина О.В., Адамян Л.В., 2009; Савельева Г.М., Соломатина А.А., 2010; Братчикова О.В., 2011; Lok I.H., Sahota D.S., 2003).
Общепризнанным методом лечения больных репродуктивного возраста с доброкачественными опухолями яичников на современном этапе является лапароскопическая энуклеация образования с максимальным сохранением неизмененной ткани яичника (Радзинский В.Е., 2004; Кулаков В.И., 2005; Манухин И.Б., 2006; Hesseling M., De Wilde R.L., 2004, Chia C.C., Hung S.C. 2007).
Несмотря на ряд работ, показавших преимущество органосохраняющих лапароскопических операций у пациенток с доброкачественными опухолями яичников, исследования по изучению особенностей функционального состояния яичников до оперативного вмешательства, последствий хирургического лечения в зависимости от глубины и тяжести повреждения немногочисленны и противоречивы (Волков Н.И., 2005; Высоцкий М.М., 2006; Зуев В.М., 2006; Muzii L., 2002; Zupi E., 2003)
Оценка фолликулогенеза и снижения фолликулярного запаса как до, так и после оперативного вмешательства остается неизученной проблемой и является чрезвычайно актуальной при планировании семьи на современном этапе. Согласно существующей точке зрения, угасание репродуктивной системы может развиться вследствие снижения фолликулярного пула, нарушения процесса фолликулогенеза, усиления апоптоза и атрезии фолликулов (May-Panloup, 2005; Kligman, 2010).
Работы последних лет значительно расширили представления о репродуктивной функции женщины и позволили сформировать представления об индивидуальном биологическом возрасте яичников - овариальном резерве (Назаренко Т.А., 2007; Боярский К.Ю., 2009). Согласно современным представлениям, выделяют тотальный овариальный резерв, который объединяет в себе фолликулярный запас (количество ооцитов в яичнике) и фолликулогенез (формирование и функционирование доминантного фолликула и желтого тела) [Gleicher N., Weghofer A., 2011].
Большинство исследований основаны на изучении состояния яичников после операции по данным тестов функциональной диагностики, данных гормонального статуса и 2D-УЗИ с применением цветового допплеровского картирования (Соломатина А.А., 2003; Пивоварова О.Ю., 2003; Соловьева Н.Г., 2005; Зуев В.М., 2006; Юсуфбекова У.Ю., 2006).
Рядом зарубежных авторов отмечено преимущество трехмерного ультразвукового исследования в объективной оценке состояния яичника, однако, в отечественной литературе мы не встретили подобных исследований (Raine-Fenning N.J., 2004; Hsien-An P., 2005; Jayaparakasan K., 2007). Отсутствуют работы, в которых оценивается состояние овариального резерва до оперативного вмешательства на яичниках, что, по нашему мнению, может влиять и на характер изменений после операции.
^ Цель исследования
Оптимизировать тактику ведения пациенток с доброкачественными опухолями ячиников, заинтересованных в реализации детородной функции, на основании современных методов оценки морфофункционального состояния яичников до и после оперативного вмешательства.
^ Задачи исследования
- Оценить состояние овариального резерва у пациенток с серозной цистаденомой и зрелой тератомой яичника до оперативного вмешательства.
- Выявить значимость 3Д-УЗИ и гормонального профиля в оценке морфофункционального состояния яичников до и после органосохраняющих операций на яичниках.
- Сравнить влияние кистэктомии и резекции яичников на показатели овариального резерва после оперативного вмешательства с учетом исходного морфофункционального состояния яичников до операции.
- Изучить состояние репродуктивной функции у пациенток после перенесенных операций по поводу доброкачественных опухолей яичников.
^ Научная новизна
Впервые на основании современных методов исследования (3D-УЗИ с энергетической допплерометрией) оценено состояние овариального резерва у пациенток с серозной цистаденомой и зрелой тератомой до и после оперативного вмешательства. Создание контуров вращающегося трехмерного изображения, позволило произвести оценку функционального состояния как яичниковой ткани, прилежащей к образованию, так и интакного яичника.
Впервые выявлено различное состояние овариального резерва у обследованных пациенток, обуславливающее изменение фолликулогенеза. Определена возможность реализации репродуктивной функции в послеоперационном периоде.
^ Практическая значимость
На основании результатов исследования дана характеристика изменений морфофункционального состояния яичников до операции. Внедрение в алгоритм обследования пациенток с доброкачественными опухолями яичников трехмерного ультразвукового сканирования с энергетической допплерометрией позволяет повысить эффективность диагностики нарушений овариальной функции. Впервые научно обоснована необходимость оценки овариального резерва до оперативного вмешательства с целью повышения эффективности лечения после операции. Разработаны и сформулированы рекомендации по ведению пациенток, перенесших резекцию яичника и кистэктомию, что поможет своевременно диагностировать изменения функционального состояния яичников, снизить частоту нарушений фолликулогенеза и репродуктивной функции. Результаты исследования могут быть использованы практическими врачами акушерами-гинекологами, а также служить научно-практической базой для дальнейших исследований и совершенствования лечебно-реабилитационных мероприятий.
^ Положения, выносимые на защиту
- Для объективной оценки функционального состояния яичников до оперативного лечения, наиболее значимым методом диагностики является применение трехмерного ультразвукового сканирования с энергетической допплерометрией, позволяющей определить объем яичниковой ткани, прилежащей к образованию, оценить количество антральных фолликулов и показатели интраовариальной перфузии.
- Определение овариального резерва до оперативного лечения у пациенток с доброкачественными опухолями яичника позволяет прогнозировать нарушения фолликулогенеза в послеоперационном периоде и определяет особенности планирования лечебных мероприятий, направленных на восстановление фертильности.
- Оптимальным методом в аспекте сохранения овариальной функции и репродуктивного здоровья у пациенток с доброкачественными опухолями яичника является кистэктомия без применения дополнительной коагуляции.
^ Внедрение результатов работы в практику
Результаты исследования внедрены в практику гинекологических отделений ГКБ №31 г. Москвы, Центра планирования семьи и репродукции, Центра планирования семьи при городской поликлинике №8. Материалы диссертации используются в педагогическом процессе на кафедре акушерства и гинекологии педиатрического факультета ГБОУ ВПО РНИМУ им. Н.И. Пирогова.
^ Апробация работы
Материалы диссертации доложены на III Международной конференции молодых ученых «Современные вопросы акушерства и гинекологии» (Москва, 2009). Апробация диссертации была проведена на заседании кафедры акушерства, гинекологии и перинатологии педиатрического факультета ГБОУ ВПО РНИМУ им. Н.И.Пирогова от 26 июня 2011 г., протокол №13.
Публикации
По материалам диссертации опубликовано 20 печатных работ, из них - 6 в рецензируемых изданиях, рекомендуемых ВАК РФ.
^ Объем и структура диссертации
Диссертация состоит из введения, 5 глав, выводов, практических рекомендаций и списка литературы. Работа изложена на 163 страницах машинописного текста, содержит 18 таблиц, 21 диаграмму и 9 рисунков. Библиографический указатель включает 70 отечественных и 81 иностранного источника.
^ МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
За период с 2007 по 2010 гг. в гинекологической клинике кафедры акушерства и гинекологии педиатрического факультета ГОУ ВПО РГМУ (зав. кафедрой – академик РАМН, профессор Савельева Г.М.) на базе ГКБ №31 г. Москвы (главный врач – член корр. РАМН, профессор Голухов Г.Н.) нами было изучено репродуктивное здоровье у пациенток, перенесших оперативное вмешательство по поводу доброкачественных опухолей яичников.
Согласно поставленной цели, мы исследовали морфофункциональное состояние яичников у 75 пациенток с серозной цистаденомой яичника, у 65 - со зрелой тератомой до и после органосохраняющих операций и у 30 здоровых женщин. Параллельно оценивали менструальную и репродуктивную функцию. Оперативное вмешательство всем пациенткам выполнялось лапароскопическим доступом по общепринятой методике.
С учетом объема выполненного оперативного вмешательства, обследованные были распределены на 3 группы. В 1 группу вошла 71 пациентка, у которой вылущивание опухоли не сопровождалось удалением яичниковой ткани, что впоследствии было подтверждено гистологически и расценено нами как кистэктомия. Во 2 группу вошли 69 обследованных, у которых, при отсутствии уверенности в полноценном удалении капсулы образования, была произведена экономная резекция яичника. В 3 группу (контрольную) включены 30 здоровых женщин, сопоставимых по возрасту, с регулярным менструальным циклом, имеющих спонтанную овуляцию и не получавших гормональную терапию в течение 1,5 лет. Возраст всех обследованных колебался от 18 до 40 лет, составляя в среднем 27±4,8 лет. При обоих морфологических вариантах образований кистэктомия и резекция были выполнены с одинаковой частотой во всех возрастных периодах.
Помимо общеклинического и гинекологического обследования, нами была произведена инструментальная оценка морфофункционального состояния яичников с использованием 2D-УЗИ и 3D-УЗИ на аппарате VOLUSON-730 Expert (GE Kretz, Zipf, Австрия) по стандартной методике c трансвагинальным датчиком (3,3-10,0 МГц). При помощи программы VOCAL (Virtual Organ Computer-aided AnaLysis) определяли объем яичниковой ткани, прилежащей к образованию, на дооперационном периоде, и объем интактного яичника в ручном режиме (Manual). Подсчет антральных фолликулов выполняли с использованием программы Inversion mode. После выполнения расчетов объема яичника в программе визуализации VOCAL™ на экран выводилась автоматически рассчитанная гистограмма трехмерного изображения (Color Angio) с показателями кровотока: индексом васкуляризации (VI), отражающего процент кровеносных сосудов во всем объеме яичника; индексом кровотока (FI), характеризующего интенсивность перфузии в интраовариальных сосудах.
Оценку фолликулярного запаса производили на 3-5 дни менструального цикла до и после оперативного вмешательства. Фолликулогенез (васкуляризацию доминантного фолликула и жëлтого тела) изучали в послеоперационном периоде с учëтом дня менструального цикла, как в интактном, так и в коллатеральном яичниках.
Для исследования гормонального статуса всем обследованным до операции и через 3, 6, 12 и 24 месяца после оперативного вмешательства проводилось количественное определение концентраций фолликулостимулирющего гормона (ФСГ) и антимюллерова гормона (АМГ) в сыворотке крови на 2-3 день менструального цикла и половых гормонов (эстрадиол, прогестерон) в первую и во вторую фазу менструального цикла методом иммуноферментного анализа.
Статистический анализ данных проводился при помощи пакета компьютерных программ Microsoft Excell с использованием общепринятых статистических методов вычисления средних величин (М), среднеквадратичного отклонения (δ) и средней ошибки (m). Для сравнения средних значений в двух параллельных группах использовали критерий Стьюдента (t). Достоверными считались отличия при p<0,05.
^ Результаты исследования
На основании анализа ультразвуковых показателей, полученных при использовании 3D эхографических исследований, мы распределили пациенток 1 и 2 группы с простой серозной цистаденомой и зрелой тератомой до оперативного лечения по подгруппам с учетом уровня изменения овариального резерва. Показатели овариального резерва в 3 группе соответствовали данным подгруппы А (табл. 1).
Анализируя эхографическую картину у 71 пациентки в 1 группе, нами выявлено, что неизмененный овариальный резерв имел место у 22 наблюдаемых (подгруппа А).
Таблица 1
| Параметры овариального резерва | Подгруппа А | Подгруппа Б | Подгруппа В | |
| Неизмененный | Умеренно сниженный | Низкий | ||
| Количество АФ в яичнике | >6 | 3-6 | <3 | |
| Объем яичника,см³ | >6 | 2-6 | <2 | |
| Показатели кровотока | VI, % | 1,3-2,9 | 0,7-1,2 | <2 |
| FI, 0-100 | 26-34 | 21-26 | >0,7 | |
| ФСГ, МЕ/л | <8 | 8-12 | >12 | |
| АМГ, нг/мл | >2,5 | 1,0-2,5 | 0,9 | |
Следует отметить, что величина опухоли у больных варьировала от 1,7 до 5 см (4,3+0,7), все обследованные находились в возрасте до 35 лет. В подгруппу Б с умеренным снижением овариального резерва вошли 30 (42,2%) пациенток, большинство из которых (21) были старше 35 лет, диаметр опухоли у 9 колебался от 6 до 10 см. В подгруппу В с низким овариальным резервом вошли 19 (26,7%) пациенток, среди которых 15 (70,8%) обследованных находились в позднем репродуктивном периоде (≥40) и у 9 (37,5%) отмечались большие размеры яичникового образования (от 9 до 12 см).
При оценке показателей овариального резерва до оперативного вмешательства у 69 пациенток во 2 группе, установлено, что количество наблюдаемых в подгруппе А (20-28,9%) было сопоставимо с 1 группой. Все обследованные находились в возрасте до 35 лет и величина образования не превышала 5 см. Умеренное снижение овариального резерва (подгруппа Б) имело место у 31 (44,9%) пациентки. При этом 19 из 31 были старше 40 лет, у 12 из 31 средний диаметр опухоли составлял 8,1+ 2,2 см. Низкие показатели (подгруппа В) отмечены у 18 (26%) женщин с величиной образования от 9 до 12 см в сочетании с поздним репродуктивным периодом. Следовательно, возраст выше 35 лет и величина опухоли более 5 см являются факторами, влияющими на состояние овариального резерва до оперативного вмешательства.
Оценка морфофункционального состояния яичников в различные сроки после органосохраняющих операций выявила, что через 1 месяц после оперативного вмешательства объем оперированного яичника в 1,4-1,5 раза был выше как в 1 группе после кистэктомии, так и во 2 группе после резекции яичника. Наибольшее увеличение объема оперированного яичника до 12 см3 наблюдалось у 12 (16,9%) пациенток в 1 группе и у 10 (14,4%) - во 2, у которых образование локализовалось у ворот яичника и энуклеация опухоли сопровождалась повышенной кровоточивостью тканей. Выявленные изменения, вероятно, обусловлены реакцией яичниковой ткани, проявляющейся отеком, в ответ на применение дополнительной коагуляции. На эхограммах визуализировались единичные (2-4) антральные фолликулы, среди неоднородных гетерогенных аваскулярных структур. Мы отметили не только уменьшение числа фолликулов, но и изменение их формы в виде полулунных деформированных гипоэхогенных включений.
Оценивая эхографическую картину яичников через 3 месяца в послеоперационном периоде, отмечено снижение объема оперированного яичника в 1,3 раза у пациенток в 1 группе после кистэктомии и в 1,5 раза - во 2 группе после резекции, в сравнении с исследованием через 1 месяц. Уменьшение объема яичника, по нашему мнению, обусловлено снижением экссудативных процессов и, соответственно, отека оперированного яичника и восстановлением его эхоструктуры с визуализацией фолликулярного аппарата, что позволило нам оценить изучаемые показатели овариального резерва. Таким образом, опираясь на наши данные, возможно заключить, что определение объема яичников, количества антральных фолликулов и показателей кровотока через 1 месяц после оперативного вмешательства не является целесообразным в связи с преходящими изменениями состояния оперированного яичника и исследование необходимо проводить, начиная с 3-го месяца после операции.
Изучая состояние овариального резерва через 3 месяца в послеоперационном периоде, установлено, что показатели фолликулярного запаса в большей степени были снижены после кистэктомии, чем после резекции яичника (табл. 2)
Таблица 2
Показатели овариального резерва у пациенток после оперативного вмешательства на яичниках
| Показатели овариального резерва | Группы обследованных (n=170) | ||
| 1 группа (n=71) | 2 группа (n=69) | 3 группа (n=30) | |
| Количество антральных фолликулов | 5,8+0,5* | 4,9+1,2* | 6,8+0,5 |
| Объем яичника V, см³ | 6,1+0,5* | 5,3+0,5* | 7,3+0,4 |
| Показатели кровотока VI FI | 2,1+0,2* 31,5+1,7 | 1,8+0,5* 25,7+2,9* | 2,6+0,2 33,4+1,7 |
Примечание. *p<0,05 при сравнении с контрольной группой
Следует отметить, что до оперативного вмешательства отмечалось равномерное распределение пациенток по группам в зависимости от уровня снижения овариального резерва. В послеоперационном периоде неизмененные показатели фолликулярного запаса (подгруппа А) имели место в 3 раза чаще в 1 группе - у 21 (29,5%) после кистэктомии, чем во 2-й группе после резекции яичника - у 8 (11,6%). Низкие показатели овариального резерва отмечались в 1,2 раза реже в 1 группе - у 24 (33,8%), чем во второй - у 28 (40,6%) [табл.3].
Как следует из табл.3, после резекции яичника количество больных с измененными параметрами овариального резерва было больше, чем после кистэктомии. Индивидуальный анализ у пациенток, сопоставимых по возрасту и величине образования в дооперационном периоде, выявил, что после кистэктомии ухудшение параметров овариального резерва обусловлено применением дополнительной коагуляции ткани яичника.
Таблица 3
Показатели овариального резерва до и после оперативного вмешательства
| Овариальный резерв | Группы обследованных | ||||
| 1 группа (n=71) | 2 группа (n=69) | ||||
| Абс. | Отн. (%) | Абс. | Отн. (%) | ||
| Нормальный Подгруппа А | До операции | 22 | 30,9 | 20 | 28,9 |
| После операции | 21 | 29,5 | 8 | 11,6 | |
| Средний Подгруппа Б | До операции | 30 | 42,3 | 31 | 44,9 |
| После операции | 26 | 36,6 | 33 | 47,8 | |
| Низкий Подгруппа В | До операции | 19 | 26,8 | 18 | 26,1 |
| После операции | 24 | 33,8 | 28 | 40,6 | |
Анализируя фолликулогенез через 3 месяца после оперативного вмешательства, прослеживается зависимость нарушений процессов формирования доминантного фолликула и желтого тела от уровня снижения овариального резерва. В подгруппе А, с неизмененными показателями овариального резерва до операции, через 3 месяца после операции овуляция имела место в 2 раза чаще, чем в подгруппах Б и В. Овуляторные циклы в оперированном яичнике, несмотря на оперативное вмешательство, были зафиксированы у каждой третьей больной в подгруппе А и только у каждой пятой обследованной в подгруппе Б. В коллатеральном яичнике частота овуляции в подгруппах А и Б составила: 50,3% и 47,5% соответственно. Оценивая фолликулогенез в подгруппе В, нами выявлено формирование доминантного фолликула только в коллатеральном яичнике у каждой второй наблюдаемой, при этом признаки полноценной овуляции (свободная жидкость в дугласовом пространстве, исчезновение доминантного фолликула с визуализацией на его месте гетерогенного образования с нечеткими неровными контурами с формированием желтого тела) не выявлены.
Влияние количества и размеров антральных фолликулов на процесс созревания доминантного фолликула продемонстрировано в исследованиях последних лет (Wallace W.H., 2010). По нашим данным, формирование доминантного фолликула определялось на 4-5 дней раньше у каждой второй обследованной в подгруппе Б и у большинства (72,3%) в подгруппе В. Однако диаметр растущего фолликула накануне овуляции (на 12-й день цикла) не превышал 15,5+0,8 см в сравнении с наблюдаемыми в контрольной группе и у пациенток в подгруппе А (18,5+0,9 см). При 3D энергетической допплерометрии выявлено снижение васкуляризации доминантного фолликула в 1,4 раза, чем в контрольной группе. При наблюдении на протяжении менструального цикла нами установлено наличие запоздалой овуляции и недостаточность перфузии желтого тела у каждой четвертой больной в подгруппе Б. У пациенток в подгруппе В признаки запоздалой овуляции имели место лишь у 4 (16,6%) наблюдаемых. Таким образом, у пациенток из подгруппы Б и В страдает поздняя стадия созревания фолликула, в то время как доминантный фолликул формируется раньше, чем в контрольной группе. Подобное УЗ наблюдение возможно объяснить данными литературны, показавшими, что у женщин со сниженным овариальным резервом имеет место снижение факторов роста IGF-I и IGF-II в фолликулярной жидкости, которые при взаимодействии с гонадотропинами стимулируют фолликул (Klein N.A., Battaglia D.E., 1996; Soules M.R., 2001). Следовательно, так как поздняя стадия фолликулогенеза более гонадотропин-зависимая (Wilshire G.B., 1995; McGee E.A., 2000), то дефицит факторов роста способствует медленному созреванию доминантного фолликула. Существенную роль играет и васкуляризация яичников, при снижении которой уменьшается возможность поступления циркулирующих гонадотропинов (Ernest Hung Y.N., Carina C.W., 2004)
Анализируя эхографическую картину на протяжении менструального цикла, мы выявили, что среди 14 (23,7%) наблюдаемых в подгруппе Б и у 18 (34,6%) обследованных в подгруппе В имел место синдром лютеинизации неовулировавшего фолликула (СЛНФ), что относительно наших наблюдений, возможно обусловлено, изменением процессов созревания фолликула у пациенток с измененным овариальным резервом.
При увеличении длительности наблюдения от 1 года до 2 лет нами отмечено снижение объема яичников, количества антральных фолликулов и показателей кровотока через 24 месяца в подгруппе Б (объем яичника: V=4,7+0,7см³; количество антральных фолликулов: АФ=4,1+1,2; плотность и интенсивность кровотока: VI-0,9+0,5%, FI-25,9+2,9) при сравнении с наблюдением через 12 месяцев (объем яичника: V=5,2+0,7см³; количество антральных фолликулов: АФ=5,3+1,2; плотность и интенсивность кровотока: VI-1,3+0,5%, FI-28,9+2,9). При этом выявлено увеличение процента нарушений фолликулогенеза в 1,3 раза.
Мы, как и другие авторы считаем, что оценка овариального резерва не может быть полноценной без учета показателей гормонов в сыворотке крови (Мишиева Н.Г., Боярский К.Ю., 2005; Singer T., 2009; Gleicher N., Weghofer A., 2011). Определяя концентрацию антимюллерова гормона (АМГ) в послеоперационном периоде, нами установлено, что в 1 группе у пациенток, перенесших кистэктомию, значение этого гормона было выше в 1,4 раза (2,1+0,3 нг/мл), чем во второй группе после резекции яичника (1,6+0,4 нг/мл) [p<0,05]. Концентрация ФСГ у пациенток после оперативного вмешательства во 2-й группе была в 1,8 раза выше, чем в 1 группе. При изучении уровня эстрадиола, нами отмечено, что у пациенток 2 группы среднее значение сывороточной концентрации эстрадиола в раннюю фолликулиновую фазу было выше (278+22,1пмоль/л) в сравнении с наблюдаемыми в первой (232+23,4пмоль/л) и в контрольной группах (193+37,4пмоль/л). Динамика изменений гонадотропных и стероидных гормонов отражена на диаграммах 1-4.
Проведенные биохимические исследования как до, так и после оперативного вмешательства продемонстрировали наибольшую зависимость между снижением овариального резерва и уровнем АМГ. Согласно результатам наших исследований, у пациенток в подгруппе А с неизмененным овариальным резервом уровень АМГ соответствовал контрольной группе (2,1+0,3 нг/мл). В подгруппе Б с умеренным снижением овариального резерва концентрация АМГ варьировала от 1 до 2,5 нг/мл. У обследованных в подгруппе В этот параметр зафиксирован ниже среднего уровня (от 0,5 до 0,9 нг/мл).
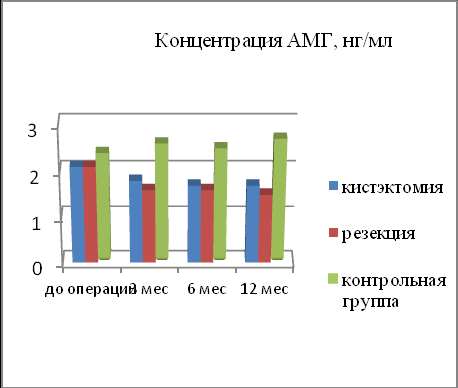
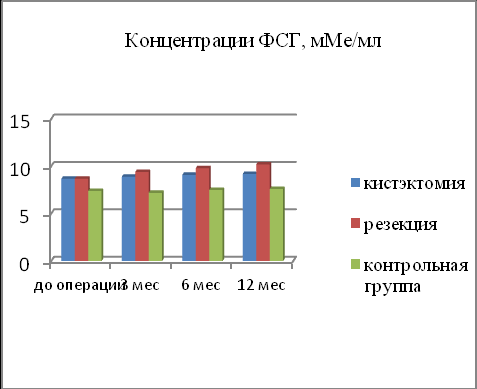
| Диаграмма 1. Концентрация АМГ у пациенток после операций на яичниках, нг/мл. | Диаграмма 2. Концентрация ФСГ у пациенток после операций на яичниках, мМе/мл. |
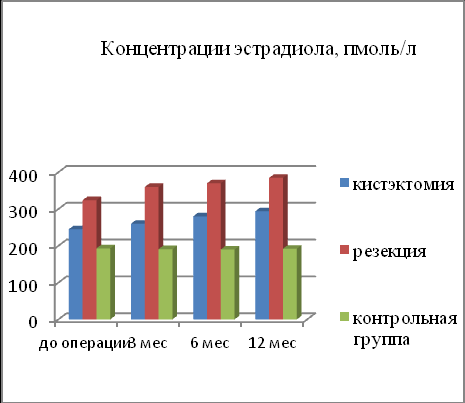
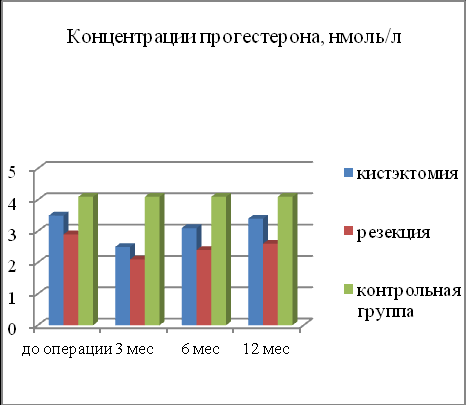
| Диаграмма 3. Концентрация эстрадиола у пациенток после операций на яичниках, пмоль/л. | Диаграмма 4. Концентрация прогестерона у пациенток после операций на яичниках, нмоль/л. |
При изучении базального уровня ФСГ на 3-4 день менструального цикла, установлено, что у пациенток в подгруппе А уровень гормона у большинства наблюдаемых (85,7%) не превышал 8,1 МЕ/мл и соответствовал данным контрольной группы (7,6+0,51МЕ/мл). Среди пациенток подгруппы Б отмечалось увеличение среднего уровня ФСГ (9,3+0,6 МЕ/мл). В подгруппе В имело место наибольшее повышение концентрации ФСГ (12,1+0,61МЕ/мл). Несмотря на измененные показатели овариального резерва, уровень ФСГ соответствовал контрольной группе у 10 из 66 наблюдаемых в подгруппе Б, и у 6 из 36 обследованных в подгруппе В.
При анализе показателей эстрадиола у пациенток в подгруппе А среднее значение сывороточной концентрации эстрадиола было ниже (193+37,4пмоль/л), в сравнении с пациенткми в подгруппе Б (245+28,4пмоль/л) и подгруппе В (324+32,1пмоль/л). При этом, повышенный уровень эстрадиола среди больных с умеренным снижением овариального резерва имел место только у каждой третьей больной, с низким овариальным резервом – у каждой второй.
Эхографические признаки синдрома лютеинизации неовулирующего фолликула (СЛНФ) сопровождались снижением предовуляторной концентрации эстрадиола и прогестерона во вторую фазу менструального цикла.
У всех пациенток со сниженными показателями перфузии жëлтого тела отмечались низкие концентрации уровня прогестерона (2,9+0,3нмоль/л) в сравнении с контрольной группой (p<0,05). Соответственно, учитывая тот факт, что количество пациенток с недостаточной перфузией желтого тела во 2 группе было больше, чем в первой, средняя концентрация прогестерона во второй группе после резекции яичника была ниже.
Второй этап работы был посвящен оценке состояния менструальной и репродуктивной функции у пациенток после органосохраняющих операций на яичниках.
При изучении менструальной функции отмечено, что после оперативного вмешательства количество больных с измененным менструальным циклом увеличилось в 1,4 раза. При детальном анализе менструальной функции в зависимости от объëма оперативного вмешательства установлено, что во 2 группе количество женщин с нормальным менструальным циклом было меньше в 1,3 раза, чем в 1 группе после кистэктомии. Нами выявлено, что у большинства наблюдаемых в подгруппе А менструальный цикл был сохранен, длительность его составила 28-30 дней и лишь у 3 (7,9%) имело место нарушение в виде олигоменореи. В то же время среди обследованных подгруппы Б изменения отмечались у каждой второй. У всех наблюдаемых подгруппы В менструальный цикл был нарушен: у 22 ( 61,1%) - укорочение менструального цикла, у 9 (25%) - нарушение по типу олигоменореи и у 4 (11,1%) - ациклические кровотечения.
Полученные результаты позволили нам прийти к заключению, что такой клинический признак, как укорочение менструального цикла, может явиться симптомом снижения функциональной активности репродуктивной системы женщин. Мы, как и другие авторы считаем, что продолжительность менструального цикла снижается у женщин в зависимости от возраста и фолликулярного запаса (Марченко Л.А., Александрова Н.В., 2005; Мишиева Н.Г., 2008; Santoro N., 1996; Weinstein M., Gorrindo T., Riley A., 2003).
Известно, что исследование тотального овариального резерва позволяет предположить наступление беременности, ее течение и исход (Мишиева Н.Г., Корсак В.С., 2008). Определение овариального резерва является тестом, оценивающим достаточность как овариального пула, так и качество ооцитов, что находит отражение в реализации детородной функции (Bukman A., 2001; Alper M.M., 2009).
При изучении репродуктивной функции через 2 года после оперативного вмешательства, нами выявлено, что у пациенток в 1 группе после кистэктомии по поводу доброкачественных опухолей яичника количество беременностей составило 17 (22,6%), а после резекции в 1,5 раза меньше - 11 (16,9%). Следует отметить, что 24 (32%) пациентки в 1 группе и 28 (43,1%) - во второй предохранялись от беременности. Следовательно, из 88 наблюдаемых, перенесших органосохраняющие операции на яичниках и планирующих реализацию репродуктивной функции, беременность наступила через 2 года только у каждой второй.
Опираясь на выделенные нами варианты состояния овариального резерва на основании УЗ критериев и биохимических параметров, мы провели анализ показателей репродуктивной функции в зависимости от степени снижения овариального резерва и объема операции (табл. 4).
Согласно результатам наших исследований наибольшая частота наступления беременности после оперативного вмешательства выявлена у пациенток в подгруппе А - 23 (79,3%).
Течение беременности среди самопроизвольных гестаций, ее исходы у обследованных с неизмененными показателями овариального резерва и эмбриональные потери (2) были сопоставимы контрольной группе (р>0,05).
Таблица 4
Исходы беременностей у пациенток 1 и 2 группы после органосохраняющих операций на яичниках
| Характеристика репродуктивной функции | Группы обследованных (n=140) | |||||||
| 1 группа (n=71) | 2 группа (n=69) | |||||||
| А N=21 | Б N=26 | В N=24 | А N=8 | Б N=33 | В N=28 | |||
| Роды | своевременные | Абс. Отн(%) | 7 33,3 | 0 | 0 | 3 37,5 | 1 3,03 | 0 |
| преждевременные | Абс. Отн(%) | 3 14,2 | 3 11,5 | 0 | 1 12,5 | 3 9,09 | 0 | |
| Кесарево сечение | Абс. Отн(%) | 1 4,7 | 3* 11,5 | 0 | 1 12,5 | 1 3,03 | 0 | |
Артифициальные аборты | Абс. Отн(%) | 4 19,04 | 2 7,69 | 1 4,2 | 1 12,5 | 1 3,03 | 1 3,5 | |
Самопроизвольные аборты | Абс. Отн(%) | 1 4,7 | 1 3,8 | 1 4,2 | 1 12,5 | 3* 9,09 | 2* 7,1 | |
Неразвивающаяся беременность | Абс. Отн(%) | 0 | 4* 15,3 | 1 4,2 | 0 | 3* 9,09 | 2* 7,1 | |
Всего беременностей | Абс. Отн(%) | 16 76,1 | 13 50,0 | 3 12,5 | 7 87,5 | 12 36,3 | 5 17,8 | |
Примечание. *p<0,05 при сравнении с контрольной группой
Бесплодие встречалось у 4 (10,5%) наблюдаемых. Анализируя причины бесплодия, нами установлено, что у 2 имел место трубно-перитонеальный и у 2 - мужской факторы, из них 3 произведена стимуляция овуляции и применение вспомогательных репродуктивных технологий (ВРТ) с последующим наступлением беременности.
Оценивая детородную функцию у обследованных в подгруппе Б, нами выявлено, что частота наступления беременности была ниже в 1,6 раза, чем в подгруппе А и составила - 25 (42,3%).
Сопоставляя результаты репродуктивных потерь, отмечен более высокий процент таких осложнений, как неразвивающаяся беременность - у 7 (31,8%) и самопроизвольное прерывание беременности - у 5 (20%) в подгруппе Б.
При изучении течения беременности, наступившей самопроизвольно у пациенток, заслуживает внимания высокая частота угрозы прерывания беременности в подгруппе Б - 12 (44,4%) в сравнении с наблюдаемыми в подгруппе А - 3 (13,04%). При гормональном обследовании было выявлено снижение уровня прогестерона, что, по нашему мнению, явилось следствием нарушенного фолликулогенеза в виде недостаточной перфузии желтого тела, которая встречалась в 2 раза чаще у пациенток с умеренным снижением овариального резерва.
При анализе течения II триместра беременности, обращает на себя внимание развитие плацентарной недостаточности в 4 раза чаще у 7 из 14 беременных в подгруппе Б. Высокая частота позднего гестоза у обследованных в подгруппе Б, по-видимому, объясняет у них же и более высокую частоту недостаточности плацентарного комплекса 9 (69,2%).
Анализируя течение и исходы родов у обследованных женщин, мы получили закономерные результаты. Нами выявлено, что частота преждевременных родов в подгруппе Б имела значительный удельный вес и составила 7 (25,9%). Каждая вторая пациентка подгруппы Б (6 из 14) была родоразрешена путем операции кесарево сечение в экстренном порядке. Мы связываем наличие большей частоты экстренных оперативных родоразрешений у пациенток с умеренным снижением овариального резерва с тем, что течение беременности у данных больных, по-видимому, осложнялось развитием плацентарной недостаточности.
Число инфертильных женщин после оперативного вмешательства у наблюдаемых в подгруппе Б было в 2,2 раза больше, чем в подгруппе А и составило 16 (24,2%). В отличие от пациенток с неизмененным овариальным резервом, среди причин бесплодия у обследованных в подгруппе Б преобладали эндокринный фактор у 4 (25%) и бесплодие неясного генеза - у 3 (18,7%). Процент трубно-перитонеального и мужского факторов не отличался от наблюдаемых в подгруппе А с неизмененным овариальным резервом. По нашему мнению, наличие эндокринного бесплодия обусловлено изменением процессов фолликулогенеза у большинства пациенток в подгруппе Б.
В наших исследованиях программа ВРТ была реализована у 8 из 16 наблюдаемых в подгруппе Б. При этом наступление беременности имело место только у 5 (62,5%) и ее течение осложнялось: неразвивающейся беременностью у 1 больной, плацентарной недостаточностью (1), нарушением гемостаза (гиперкоагуляция) - у 2 пациенток.
Освещая вопрос репродуктивной функции у пациенток в подгруппе В с низким овариальным резервом, нами зафиксировано наступление беременности у 8 (15,3%) наблюдаемых, заинтересованных в реализации репродуктивной функции. При этом, артифициальный аборт был произведен у 2 пациенток. Ни одну из наступивших беременностей не удалось сохранить: неразвивающаяся беременность имела место у 3, самопроизвольный выкидыш - у 3.
Количество инфертильных пациенток в подгруппе В было в 4,5 раза выше, чем в подгруппе А и в 2,2 раза выше, чем в подгруппе Б. При ретроспективном исследовании этиологии бесплодия у женщин с низким овариальным резервом, обращает на себя внимание наибольшая частота пациенток с неустановленным фактором - у 6 (35,3%) и эндокринным бесплодием - у 5 (29,4%), в то время как трубно-перитонеальный 1 (5,8%), мужской 2 (11,8%) и сочетанные факторы 3 (17,6%) имели место в значительно меньшем проценте наблюдений, чем в подгруппе А и Б.
Сопоставляя полученные результаты исследования с данными ультразвукового и биохимического профиля, мы выявили, что у большинства наблюдаемых с бесплодием неясного генеза имел место синдром лютеинизации неовулировавшего фолликула (СЛНФ).
При анализе исходов ВРТ у 10 из 17 наблюдаемых с бесплодием и низким овариальным резервом, нами выявлено наступление беременности только у 3. При этом, у 1 пациентки имела место неразвивающаяся беременность и у 2 - самопроизвольное прерывание беременности. У остальных пациенток (7 из 10) попытки ЭКО были безуспешны.
Таким образом, своевременная диагностика таких изменений фолликулогенеза, как недостаточность лютеиновой фазы цикла и СЛНФ, которые были выявлены у большинства наблюдаемых в подгруппах Б и В с измененным овариальным резервом позволит предупредить нарушения менструальной функции и осложнения последующих гестаций.
ВЫВОДЫ
- Изменения морфофункционального состояния яичников у женщин до оперативного вмешательства зависит от возраста пациенток, размеров и локализации опухоли. Более выраженное снижение овариального резерва отмечено у пациенток старше 35 лет, с величиной опухоли более 6 см и при расположении яичникового образования у ворот яичника.
- На фоне использования биохимических маркеров в оценке овариального резерва (АМГ, ФСГ, эстрадиол), наиболее значимым инструментальным методом является 3D-УЗИ с определением объема яичников, количества антральных фолликулов, показателей интраовариального кровотока.
- Сравнительная оценка органосохраняющих операций с учетом состояния овариального резерва до операции, свидетельствует о более негативных последствиях после резекции яичника по отношению к кистэктомии.
- Характер изменения овариального резерва влияет на репродуктивную функцию пациенток:
- при неизмененном овариальном резерве достоверных различий в реализации репродуктивного потенциала в сравнении с женщинами в популяции нет;
- при умеренном снижении овариального резерва в 2 раза чаще встречаются такие осложнения, как угроза прерывания беременности, развитие плацентарной недостаточности;
- при низком овариальном резерве отмечается наибольший процент бесплодия (53,8%).
^ ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
- Оперативное вмешательство у пациенток репродуктивного периода с доброкачественными опухолями яичника предпочтительно проводить c максимальным сохранением яичниковой ткани, что достигается в большей степени при кистэктомии, чем при резекции.
- С целью определения параметров овариального резерва на дооперационном этапе целесообразно применение 3D-УЗИ с трехмерной допплерометрией, которая позволяет более точно оценить объем яичниковой ткани, прилежащей к образованию, визуализировать фолликулы при помощи создаваемых вручную контуров вращающегося трехмерного эхографического изображения и выявить изменения плотности и интенсивности интраовариальной перфузии.
- Определяя морфофункциональное состояние яичников до оперативного вмешательство необходимо учитывать уровень снижения овариального резерва, выделяя:
- неизмененный овариальный резерв [объëм яичника V=7,1+0,7см³; количество антральных фолликулов АФ=6,8+0,5; интенсивность и скорость кровотока:VI-2,1+0,2; FI-31,8+1,7]
- умеренно сниженный овариальный резерв [объем яичника: V=5,1+0,7см³; количество антральных фолликулов: АФ=4,8+1,2; плотность и интенсивность кровотока: VI-1,8+0,5%, FI-29,9+2,9]
- низкий овариальный резерв [объëм яичника V=2,7+0,7см³; количество антральных фолликулов АФ=2,8+0,5; интенсивность и скорость кровотока не регистрировались].
4. С целью раннего выявления нарушений фолликулогенеза, необходимо проведение ультразвукового исследования и определение гормонального профиля на протяжении менструального цикла, начиная с 3 месяца после операции, так как в течение первых трех месяцев в оперированном яичнике отмечаются преходящие изменения, обусловленные отеком в области оперативного вмешательства.
5. При наличии умеренного снижения овариального резерва беременных пациенток необходимо относить в группу повышенного риска по развитию невынашивания беременности и плацентарной недостаточности. Пациенткам с бесплодием и с умеренным снижением овариального резерва после оперативного лечения целесообразно рекомендовать программу ВРТ через 3 месяца после оперативного вмешательства во избежание потери овариального резерва с течением времени.
6. При низком овариальном резерве пациентку необходимо предупредить о возможности бесплодия и наступления беременности только при использовании ВРТ.
^ СПИСОК РАБОТ, ОПУБЛИКОВАННЫХ ПО ТЕМЕ ДИССЕРТАЦИИ
- Манюхина И.А., Кузнецов М.В., Сафронова Д.А. Репродуктивное здоровье женщин после воспалительных заболеваний органов малого таза //Вестник Российского государственного медицинского университета. - 2008. - №3(62). - С. 42-46.
- Сафронова Д.А., Тварадзе И.Э., Манюхина И.А., Демидов О.В. Репродуктивное здоровье пациенток после органосохраняющих и радикальных методов лечения пациенток с трубной беременностью //Вестник Российского государственного медицинского университета. - 2008. - №3(62). - С. 57-59.
- Соломатина А.А., Сафронова Д.А., Л.Н. Демина Л.Н. Репродуктивное здоровье женщин после органосохраняющих и радикальных операций на яичниках //Тезисы докладов международного конгресса «Технологии 21 века в гинекологии». – Москва, 2008. - С. 107-109.
- Братчикова О.В., Сафронова Д.А., Сорокин Ю.А. Трехмерная визуализация в диагностике эпителиальных опухолей яичников //III международная конференция молодых ученых «Современные вопросы акушерства, гинекологии и перинатологии». Лечебное дело, специальный выпуск. – Москва, 2009. - С. 8-13.
- Сафронова Д.А., Братчикова О.В., Сорокин Ю.А. Овариальный резерв у пациенток после органосохраняющих операций на яичниках //III международная конференция молодых ученых «Современные вопросы акушерства, гинекологии и перинатологии». Лечебное дело, специальный выпуск. – Москва, 2009. - С. 44-48.
- Соломатина А.А., Сафронова Д.А., Братчикова О.В. Возможности трехмерной эхографии в оценке морфофункционального состояния яичников у пациенток, перенесших органосохраняющие операции на яичниках //Актуальнi проблеми сучасноi медицини. – Киев, 2009. - Том №2. - Выпуск 4. - C. 87-92.
- Соломатина А.А., Сафронова Д.А., Братчикова О.В. Значение трехмерного ультразвукового сканирования в оценке овариального резерва у пациенток, перенесших органосохраняющие операции на яичниках //Вопросы гинекологии, акушерства и перинатологии. - 2009. - Т. 8. - N6. - С. 52-56.
- Соломатина А.А., Братчикова О.В., Сафронова Д.А. Трехмерная эхография в диагностике серозных опухолей и рака яичников //Вопросы гинекологии, акушерства и перинатологии. – 2009. – Т.8. – N.6. – C. 40-45.
- Соломатина А.А., Сафронова Д.А., Братчикова О.В., Соломатин Д.В., Саргсян Н.С. Овариальный резерв у пациенток, перенесших органосохраняющие операции на яичниках. Значение трехмерного ультразвукового исследования //Материалы Х Всероссийского научного форума «Мать и дитя». – Москва, 2009. - С. 411-412.
- Соломатина А.А., Сафронова Д.А., Братчикова О.В. Преимущества трехмерного ультразвукового исследования в оценке овариального резерва у пациенток, перенесших операции на яичниках //Тезисы докладов ХХII Международного конгресса с курсом эндоскопии «Новые технологии в диагностике и лечении гинекологических заболеваний». – Москва, 2009. – С. 13.
- Савельева Г.М., Соломатина А.А., Сафронова Д.А. Функциональное состояние яичников до и после операций по поводу доброкачественных образований яичников //Материалы ХI Всероссийского научного форума «Мать и дитя». – Москва, 2010. - С. 493.
- Сафронова Д.А., Братчикова О.В., Соломатин Д.В., Тюменцева М.Ю. Значение трехмерной энергетической допплерометрии в оценке овариального резерва у пациенток, перенесших резекцию яичника //Вестник Российского государственного медицинского университета. - 2010. - №2. - С. 285-286.
- Сафронова Д.А., Братчикова О.В., Соломатин Д.В., Смирнова А.А., Науменко А.А. Состояние интраовариального кровотока у пациенток, перенесших кистэктомию по поводу доброкачественных опухолей яичников //Вестник Российского государственного медицинского университета. – 2010. - №1 (специальный выпуск). – С. 40-41
- Соломатина А.А., Сафронова Д.А., Братчикова О.В. Восстановление яичников после органосохраняющих операций по поводу доброкачественных опухолей: УЗ-оценка в краткосрочном периоде после операции //Материалы ХI Всероссийского научного форума «Мать и дитя». – Москва, 2010. - С. 515.
- Соломатина А.А., Сафронова Д.А., Братчикова О.В., Соломатин Д.В., Смирнова А.А. Значение 3D-УЗИ в оценке морфофункционального состояния яичников у пациенток, перенесших оперативное вмешательство по поводу эндометриоза яичников //Тезисы докладов IV международного конгресса по репродуктивной медицине. - Москва, 2010. – С. 41.
- Solomatina A.A., Safronova D.A., Bratchikova O.V. Ovarian restore after laparoscopic enucleation of ovarian cysts: 3D-Ultrasonography short-term postsurgical follow-up //5-th Congress of the world Association of Reproductive Medicine. Reproductive BioMedicine Online. – Moscow, 2010. - C. 48.
- Сафронова Д.А., Братчикова О.В., Кавтеладзе Е.В. Овариальный резерв и репродуктивная функция у пациенток после лапароскопической кистэктомии по поводу доброкачественных опухолей яичников //Вестник Российского государственного медицинского университета. - 2011. - N.2 - С. 124-127.
- Соломатина А.А., Кавтеладзе Е.В., Сафронова Д.А. Возможности 3D-УЗИ в диагностике эндометриоидных образований яичников //Материалы ХII Всероссийского научного форума «Мать и дитя». – Москва, 2011. - С. 420-421.
- Соломатина А.А., Сафронова Д.А., Коновалова А.В., Братчикова О.В., Балицкий С.П. Овариальный резерв у пациенток с различными видами трубно-пернитонеального бесплодия //Тезисы докладов ХХIV Международного конгресса с курсом эндоскопии «Новые технологии в диагностике и лечении гинекологических заболеваний».– Москва, 2010. – С. 167-168.
- Solomatina A.A., Kavteladze E.V., Safronova D.A., Bratchikova O.V. Three-dimentional evaluation of ovarian reserve in patient with endometriomas before and after lapariscopic excision //11-th World Congress on Endometriosis. - France, 2011. – P. 242.
- Solomatina A.A., Kavteladze E.V., Safronova D.A., Aghaeva S.V. The new possibilities of differential diagnosis of endometriomas // Deutcsch-Russischer Kongress fur Gynakologie und Geburtshilfe. -Berlin, 2011. – N. 16.
