Пограничные эпителиальные опухоли яичников: клиническое течение и проблемы морфологической диагностики
| Вид материала | Документы |
- "опухоли яичников", 207.85kb.
- Синдром гиперстимуляции яичников в программе экстракорпорального оплодотворения. Клиническое, 882.52kb.
- Дополнительные вопросы и список литературы для подготовки к квалификационному экзамену, 346.64kb.
- Г. Г. Автандилов Российская медицинская академия последиплом, 32.45kb.
- Макарищев Алексей Яковлевич клиническое значение сосудистого эндотелиального фактора, 770.69kb.
- Эпителиальные опухоли, 166.88kb.
- Рабочий план практических занятий по акушерству и гинекологии для студентов IV курса, 24.92kb.
- Лекция, одобренная nams, 33.27kb.
- Классификации инфекционных заболеваний, 40.03kb.
- Влияние электромагнитного излучения миллиметрового диапазона на течение острого инфаркта, 37.45kb.
ПОГРАНИЧНЫЕ ЭПИТЕЛИАЛЬНЫЕ ОПУХОЛИ ЯИЧНИКОВ: КЛИНИЧЕСКОЕ ТЕЧЕНИЕ И ПРОБЛЕМЫ МОРФОЛОГИЧЕСКОЙ ДИАГНОСТИКИ
Е.Н. Шлома1, М.В.Фридман2, С.Е. Шелкович2, Ю.Е. Демидчик1
1 Белорусский государственный медицинский университет
2 Минский городской клинический онкологический диспансер
Пограничные эпителиальные опухоли яичников, называемые также карциномами с низким потенциалом злокачественности, характеризуются интракистозным ростом сосочковых структур, отсутствием инвазии стромы яичника и благоприятным клиническим течением. Как правило, эти новообразования выявляются у женщин репродуктивного возраста, а потому представляют собой не только медицинскую проблему, но в определенной мере имеют и социальное значение.
Известно, что клиническая диагностика пограничных опухолей затруднена из-за отсутствия патогномоничных симптомов, а результаты ультрасонографии не всегда позволяют их дифференцировать не только с доброкачественными новообразованиями, но и с типичными злокачественными карциномами. Широко распространенный в настоящее время способ идентификации рака яичников, основанный на определении маркерного гликопротеина СА-125, применительно к пограничным карциномам не может считаться строго специфичным. По этой причине диагноз пограничной опухоли может быть достоверно установлен только по итогам послеоперационного морфологического исследования.
К сожалению, большинство операций по поводу новообразований с низким потенциалом злокачественности выполняется в неспециализированных учреждениях, где, зачастую, нет возможности для проведения экспресс-диагностики, от результата которой должен зависеть выбор соответствующего объема операции.
Так, в исследовании R.Fauvet с соавт. [13] при ретроспективном анализе 360 случаев хирургического лечения пограничных опухолей яичников отмечается, что срочное гистологическое исследование проведено только в 41,6% случаев, а адекватное хирургическое стадирование выполнено лишь у 37 (10,3%) пациенток.
В большинстве случаев (50-80%) карциномы яичников низкой степени злокачественности выявляются в начальных стадиях заболевания [1, 13, 14]. Поэтому у трети больных, у которых заболевание диагностируется в возрасте до 40 лет при Iа стадии процесса и желании женщины сохранить фертильность, возможно выполнение органосохраняющего лечения [16, 17]. Пятилетняя выживаемость при I стадии, по данным различных авторов, составляет 95-100% [2, 8, 10, 13, 15].
Согласно морфологической классификации, выделяют следующие гистологические типы низкозлокачественных карцином: серозные, муцинозные, эндометриоидные, светлоклеточные, опухоли Бреннера и смешанные [1, 6]. Наиболее частый гистологический вариант – это серозные опухоли, которые составляют более 50% всех пограничных новообразований [7, 8]. Муцинозные и эндометриоидные – встречаются реже, согласно данным литературы, в 14-30% и 2,3-7% случаях соответственно [6, 8]. Двусторонний процесс чаще выявляется при серозных опухолях (20-40%), реже при муцинозных (5-10%) [1, 10].
Заметим, что морфологическая диагностика эпителиальных опухолей яичников традиционно относится к одному из наиболее сложных и ответственных процессов. Все еще остаются спорными вопросы верификации карцином как таковых (например, критерии дифференциации между пограничными неоплазмами низкого потенциала злокачественности и истинным раком), определение внутривидовых различий новообразований (принадлежность к группе серозных, муцинозных или эндометриоидных опухолей), а также способы доказательства первичности или метастатического характера процесса.
Возникает парадоксальная ситуация, когда, несмотря на огромную клиническую значимость опухолей яичников и распространенность их в популяции, большую заинтересованность в улучшении результатов диагностики и лечения и внедрение самых современных методов обследования, точность морфологических заключений по-прежнему во многом определяется размерами образования и его макроскопическим видом.
В качестве примера приведем ситуацию, когда у пациентки обнаруживается гормонально-неактивное пальпируемое двустороннее образование, опухолевые клетки в асцитической жидкости отсутствуют, патологических изменений со стороны органов желудочно-кишечного тракта не отмечено. При лапаротомии видны изменения в серозной оболочке толстого и тонкого кишечника, брюшине малого таза и большом сальнике – узловатые мягко-эластичные серовато-красные образования размером до 10 мм. В то же время капсула 20-30-сантиметровых яичников, с бугристой поверхностью, гладкая. При экспресс-биопсии большего по размеру измененного органа определяются множественные гладкостенные кисты, содержащие в просвете густое, тягучее, светлое содержимое.
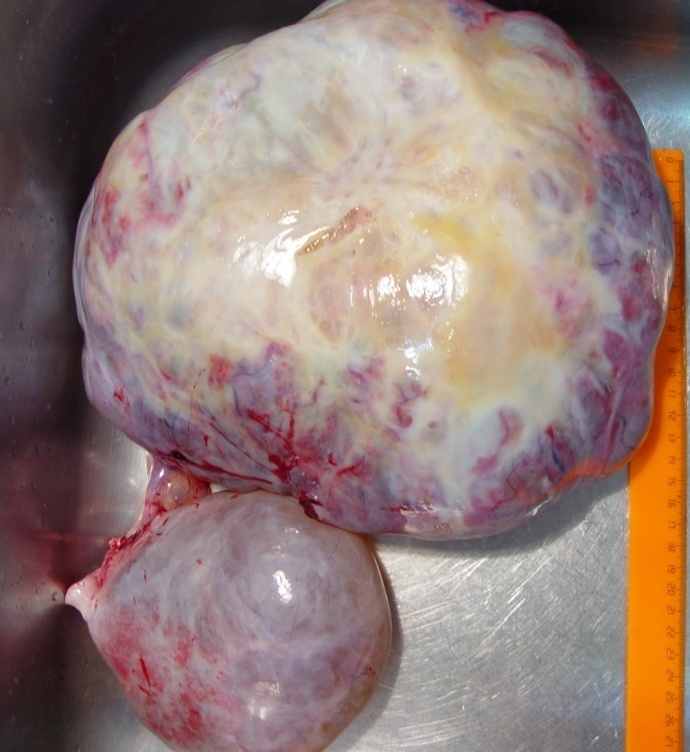
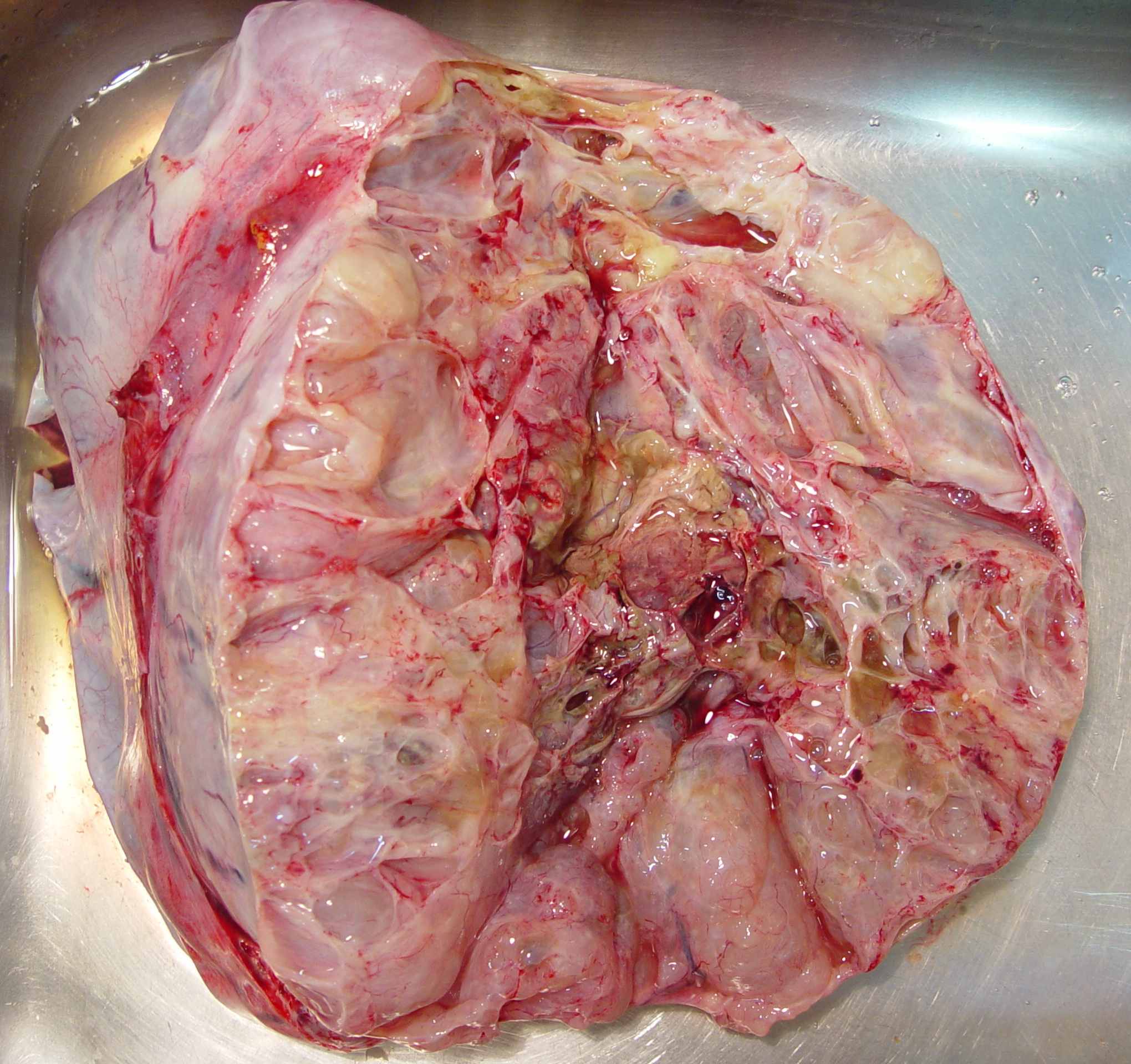
Интересы больной требуют от патологоанатома определить злокачественный потенциал новообразования, что не всегда просто и при рутинном исследовании, но совершенно невозможно, когда отсутствуют макроскопические признаки малигнизации – солидный рост, обширные участки распада и прорастание капсулы яичника. В рассматриваемой ситуации закономерно возникает вопрос, сколько тканевых блоков будет достаточно, чтобы в 20-30-сантиметровой опухоли (рисунок 1а-в) отыскать участки малигнизации (если, конечно, они в ней имеются). При этом следует помнить, что наличие опухолевых клеток в смывах из брюшины или в асцитической жидкости, а также видимые невооруженным глазом опухолевидные узлы в сальнике могут отражать процесс обсеменения из разорвавшихся кистозных камер, но не истинное метастазирование. Очевидно, что рекомендуемое некоторыми исследователями выборочно-серийный (через 1 см) тотальный забор материала неосуществим в условиях общей прозектуры, поэтому и доказательность диагноза пограничной кистомы или истинной аденокарциномы во многом будет зависеть от вероятностного фактора.
Следующая проблема возникает при определении принадлежности первичного новообразования яичника к тому или иному варианту, выделяемому в зависимости от эпителиальной выстилки кист или железистых ходов. Светооптическое разнообразие структур и опухолевых клеток долгое время питало признанное в настоящий момент ложным представление о гистогенетическом полиморфизме эпителиальных неоплазм яичника. Так, выделяли опухоли из дистопированного эпителия трубно-маточного (цилиоэпителиальная, или серозная группа, а также эндометриоидный вариант) и цервикального (псевдомуцинозная, или муцинозная группа) типов и новообразования из эмбриональных остатков первичной почки (опухоли Бреннера, или переходноклеточные и мезонефромы, или светлоклеточные неоплазмы). Хотя уже более тридцати лет считается доказанным, что все эпителиальные новообразования яичника происходят из метаплазированного мезотелия, тем не менее, и в ранних, и в более поздних классификациях составители сохраняют светооптическую детализацию.
Заметим при этом, что предсказательная и прогностическая значимость описанных вариантов строения эпителиальных опухолей яичника никем пока не выявлена. В то же время, практическая целесообразность такого подразделения не вызывает сомнений – каждая группа имеет свои особенности морфогенеза и дифференциальной диагностики аденом и карцином. В некоторых случаях можно вести речь о стадийности канцерогенеза, в других же существование переходных форм от доброкачественных к злокачественным нозологическим единицам не доказано (например, в группе светлоклеточных опухолей).
Определение внутривидовой принадлежности эпителиальной опухоли яичника важно и для формулирования критериев злокачественности. Например, одно- и многокамерные кисты со светло-серозным жидким содержимым и наличием на внутренней поверхности плотных зерен или бляшек определенно указывает на грубососочковую серозную цистаденому, которая обладает нулевым потенциалом к малигнизации. Для диагностики пограничной серозной цистаденомы патологоанатому требуется обнаружить мягкие ворсинчатые выросты, а в них - стратификацию эпителия, выстилающего сосочки, вместе с плеоморфизмом ядер, клеток и их митотической активностью. Если доминируют папиллярные структуры, выстланные многорядным эпителием, где утрачивается полярность и присутствует выраженная цитологическая атипия, а в субэпителиальной строме наблюдается мононуклеарная инфильтрация, то единственным мерилом, позволяющим провести дифференциальную диагностику с карциномой, становится обнаружение инвазивного роста.
Кистомы яичника губчатого строения со стекающей с поверхности разреза вязкой полупрозрачной массой (муцинозные опухоли) оцениваются по другим критериям. Даже без явных сосочков, эпителиальных напластований и образования аркад, атипичные изменения в опухолевых клетках, выстилающих кисты (полиморфизм, гиперхроматоз или укрупнение ядрышка, большое количество митозов, исчезновение секретирующих муцин клеточных элементов), уже достаточны для диагностики муцинозного рака (рисунок 1г-е). Следует подчеркнуть, что гистологическая детализация возможна только в случаях высоко дифференцированных новообразований. По мере нарастания катаплазии, которая проявляется преобладанием участков солидного и солидно-альвеолярного строения (рисунок 2), слабым или, наоборот, чрезмерным развитием стромы, клеточной атипией, определить принадлежность неоплазмы к той или иной группе не представляется возможным даже с использованием средств иммунофенотипирования [19]. То же относится и к оценке изменений, возникших в связи с химиотерапией, что проявляется обилием псаммомных телец, появлением опухолевых клеток с обильной светлой или эозинофильной цитоплазмой. Именно поэтому столь важно определить фенотип опухоли до начала специфического лечения.
Наконец, остаются вопросы точности морфологической диагностики в случаях первично-множественного опухолевого процесса и при дифференциальной диагностике метастатической и органоспецифической карциномы. В метастазе структура первичной опухоли может быть резко изменена либо наблюдается светооптическое сходство с какой-то разновидностью рака яичника. Ориентируются в таких случаях на преимущественную локализацию процесса – при метастатической природе наблюдается поражение периваскулярных и периневральных пространств, а также эмболия сосудов. Для первичных карцином яичников характерны остатки кист. Но если опухоль низкой степени дифференцировки и субтотально замещает орган (диффузные солидно-скиррозные разрастания), то разобраться в нозологической принадлежности карциномы исключительно сложно. В спорных ситуациях клинико-лабораторные данные играют важную роль, но не стоит их и переоценивать.
Сегодня в арсенале морфолога имеются высокоспецифические моноклональные антитела, результат применения которых (с поправкой на информацию, полученную при анализе клинической информации и макроскопического вида объектов), в подавляющем большинстве случаев, позволяет добиться верификации процесса. Например, при использовании панели маркеров с включением низкомолекулярного цитокератина 7 типа, СА125, WT1, ER, p53 и p16 есть возможность уточнить серозный фенотип и исключить новообразования другого (имитирующего) фенотипа [20]. А коэкспрессия виментина и цитокератина в сочетании с обнаружением эстрогеновой и прогестероновой активности в опухолевых клетках позволит говорить об эндометриоидной опухоли. Наконец, для муцинозных новообразований будет характерна продукция карцино-эмбрионального и эпителиального мембранного антигенов.
За период с 2002 по 2005 гг. в Минском городском клиническом онкологическом диспансере наблюдали 585 больных злокачественными эпителиальными, неэпителиальными и пограничными опухолями яичников I-IV стадий. Истиные карциномы диагностированы у 463 (79,2%) больных, неэпителиальные злокачественные новообразования – в 51 (8,7%) наблюдении, а пограничные опухоли яичников выявлены в 71 (12,1%) случае.
Возраст пациенток с новообразованиями яичников низкой степени злокачественности варьировал от 20,9 до 84,9 лет, составив в среднем 44,7±1,8 года. При оценке степени распространения опухоли по классификации FIGO, в значительном числе наблюдений диагностированы начальные стадии заболевания. Так, IA стадия имела место в 37 (52,1%) случаях, IB – в 4 (5,6%), IС – в 24 (33,8%), IIA – в одном наблюдении (1,4%) (таблица 1.). У двух пациенток установлена III стадия: у одной – выявлены микрометастазы в большом сальнике, у второй больной – асцит, диссеминаты в малом тазу, метастазы в большом сальнике (таблица 1).
Преобладающим гистологическим вариантом был серозный тип, установленный в 46 (64,8%) случаях. Пограничная муцинозная опухоль выявлена у 24 (33,8%) больных, эндометриоидная – у одной (1,4%).
Согласно данным литературы, каких-либо специфических клинических проявлений для пограничных новообразований яичников не существует. Так и по нашим данным, симптомы заболевания не были патогномоничными. При профилактическом осмотре опухоль яичников была диагностирована только у 26 (36,6%) пациенток, остальные обратились с жалобами. Боли или дискомфорт в нижних отделах брюшной полости наблюдали у 34 (47,9%) больных, увеличение живота – в 19 (26,8%) случаях, мено-метроррагии – у трех (4,2%) и общая слабость – у трех (4,2%) пациенток.
Специальное лечение начиналось в среднем через 9,4 месяца от момента появления жалоб. У 5 (7%) пациенток хирургическое лечение выполнено по экстренным показаниям в связи с клинической картиной “острого живота”. В 38% случаев (27 больных) пограничные опухоли яичников выявлены при плановых хирургических вмешательствах в гинекологических отделениях общей лечебной сети. Такие пациентки поступали с предварительным диагнозом миомы матки либо кисты яичника.
Сопутствующие заболевания диагностированы у 45 (63,4%) больных. Чаще всего встречались болезни сердечно-сосудистой системы (ИБС, артериальная гипертензия) и желудочно-кишечного тракта (гастрит, холецистит, язвенная болезнь желудка или 12-перстной кишки), реже – заболевания органов дыхания и периферических вен (таблица 2).
Обращает на себя внимание, что более половины больных (n=39; 54,9%) имели в анамнезе заболевания репродуктивной системы. Чаще всего наблюдались: миома матки, эрозии шейки матки, хронический аднексит. Хирургическое лечение по поводу доброкачественных кист яичников в прошлом выполнено 6 (8,5%) пациенткам. Первично-множественный рак установлен в 4 случаях: у одной больной выявлен синхронный рак эндометрия, у трех пациенток – в анамнезе проведено хирургическое лечение по поводу злокачественных новообразований шейки матки, кожи, легкого.
Согласно алгоритмам диагностики и лечения больных злокачественными новообразованиями [18], в объем диагностических мероприятий при опухолях яичников входят: лабораторные исследования, определение опухолевых маркеров (СА-125, больным до 30 лет β-хорионического гонадотропина, АФП), гинекологическое исследование, УЗИ органов брюшной полости и малого таза, обследование органов ЖКТ с целью исключения метастатического характера поражения яичников.
В нашем исследовании изменения в общем анализе крови отмечены у 14 (19,7%) пациенток в виде: анемии, лейкоцитоза, ускоренной СОЭ. Отклонения в биохимическом анализе крови зарегистрированы в единичных случаях. Гипопротеинемия, как результат общего воздействия опухоли на организм, была выявлена у двух (2,8%) больных с I стадией заболевания, при этом диагностированы опухоли больших размеров (20-46 см в наибольшем измерении). Белковое голодание организма связано с феноменом “субстратных ловушек”. Разрастаясь, опухоль потребляет продукты необходимые для жизнедеятельности организма (аминокислоты, глюкозу, липиды и т.д.), приводя в конечном итоге к кахексии больного. Повышение уровня мочевины до 10,5 ммоль/л выявлено у двух (2,8%) больных. Высокий уровень мочевины, при нормальных показателях креатинина может свидетельствовать о распаде опухолевых масс. Несмотря на приспособленность опухоли к гипоксии, при больших размерах новообразования наступает некроз клеток, что проявляется синдромом эндогенной интоксикации, обусловленной всасыванием большого количества продуктов тканевого распада. Вероятнее этим обусловлены высокие показатели мочевины у данных пациенток.
Основную роль в патогенезе тромботических осложнений, а также ДВС-синдрома у онкологических больных играют изменения системы гемостаза, вызываемые опухолью. Активация системы гемостаза обусловлена поступлением в кровоток из опухолевых клеток высокоактивного тканевого тромбопластина, который служит инициатором процесса свертывания крови. Как известно, I стадия ДВС-синдрома характеризуется нарастанием гиперкоагуляции и повышением внутрисосудистой агрегации тромбоцитов. Для данной стадии характерно укорочение АЧТВ, нормальный, но чаще повышенный уровень фибриногена. Гиперкоагуляция по результатам АЧТВ выявлена в 6 (8,5%) наблюдениях. Гиперфибриногенемия отмечена у 26 (36,6%) больных.
Наиболее известным маркером для идентификации злокачественных серозных и эндометриоидных опухолей яичников считается СА-125. Данный гликопротеин не является истинным опухолевым маркером, т.к. может синтезироваться и нормальными, и злокачественными клетками эпителиального происхождения. Повышение уровня СА-125 может наблюдаться при эпителиальных опухолях негинекологической локализации, различных воспалительных заболеваниях органов брюшной полости, циррозе печени, беременности и эндометриозе [13] . Следует отметить, что исходный уровень СА-125 до начала лечения определялся только у 9 (12,7%) пациенток и был повышен у трех из них.
Согласно данным УЗИ и ревизии органов брюшной полости размер опухоли варьировал от 4 до 50 см в наибольшем измерении, составляя в среднем около 10 см.
Всем больным на первом этапе проведено хирургическое лечение. Стандартная операция (экстирпация матки с придатками, резекция большого сальника) выполнена в 46 (64,8%) наблюдениях, в том числе у 42 (51,1%) пациенток с I стадией и у 4 (5,6%) со II и III стадией. Органосохраняющие вмешательства (односторонняя аднексэктомия и резекция второго яичника, удаление большого сальника) произведены 19 (26,8%) молодым пациенткам с IA стадией заболевания. В остальных случаях выполнялись следующие операции: двусторонняя аднексэктомия, резекция большого сальника (n=5; 7%); надвлагалищная ампутация матки с придатками и резекция большого сальника (n=1; 1,4%).
У 38 (53,5%) пациенток хирургическое лечение дополнено курсами полихимиотерапии (от 3 до 6, в среднем 4 курса) с использованием стандартных препаратов I линии: CP (цисплатин 75-100 мг/м2 + циклофосфамид 750-1000 мг/м2) или СС (карбоплатин 300-350 мг/м2 + циклофосфамид 750-100 мг/м2).
За время наблюдения умерло две пациентки, одна от ИБС, вторая от основного заболевания. Наблюдаемая 5-летняя выживаемость составила 94,6%.
ВЫВОДЫ
- Пограничные опухоли яичников встречаются преимущественно у пациенток молодого возраста, обычно диагностируются в I стадии, характеризуются отсутствием специфической симптоматики, часто выявляемой гиперфибриногенемией и гематологическими признаками эндогенной интоксикации.
- У больных с низкозлокачественными карциномами яичников I стадии допустимый объем оперативного вмешательства заключается в выполнении аднексэктомии с резекцией сальника, контрольной биопсией париетальной брюшины и второго яичника.
- Первичная морфологическая диагностика при подозрении к опухоли яичника должна включать обязательный этап интраоперационного исследования. Тщательное описание изменений, видимых невооруженным взглядом до фиксации в формалине, акцентуация на поиске зон сосочкового и солидного строения, обращение внимания на состояние капсулы яичника способствует выбору адекватного материала как для экспресс-биопсии, так и для базового гистологического исследования. При обнаружении обширных зон с макроскопической картиной, позволяющей заподозрить пограничную опухоль или рак, рекомендуется оставлять эти полоски ткани в архиве (можно фиксировать в 10% растворе формалина) для возможностей дополнительного взятия материала из подозрительных участков. Наконец, в диагностике обязательно следует учитывать, что определение злокачественного потенциала опухоли производится только на основании особенностей ее строения и роста в яичнике без учета клинических проявлений (в том числе, диссеминации в сальнике или других проявлениях агрессивных свойств).
ЛИТЕРАТУРА
- Новикова, Е.Г. Пограничные опухоли яичников/Е.Г.Новикова,
Г.Ю. Батталова. – М.: ООО «Медицинское информационное агентство», 2007. – 152 с.
- Батталова, Г.Ю. Отдаленные результаты органосохраняющих операций пограничных опухолей яичников у женщин детородного возраста /
Г.Ю. Батталова // Акушерство и гинекологогия. – 2005. – №2. – С. 57 – 60.
- Gershenson, D. Is Micropapillary Serous Carcinoma for Real? / D. Gershenson // Cancer. – 2002. – Vol. 95, № 4. – P. 677 – 680.
- Scollo, P. Borderline ovarian tumors. Case report and review of literature / P.Scollo, M.R.Pagano // Europ. J. Gynecol. Oncol. – 1995. – 16 (3). – P. 232 – 237.
- Батталова, Г.Ю. Особенности репродуктивной функции женщин после лечения по поводу пограничной опухоли яичника / Г.Ю.Батталова // Российский вестник акушера-гинеколога. – 2004. – Том 4, №4. – С. 51 – 54.
- Батталова, Г.Ю. Современные представления о пограничных опухолях яичников / Г.Ю. Батталова, Е.Г.Новикова // Вопросы онкологии. – 2005. – Том 51, №2. – С. 173 – 181.
- Онкогинекология: Руководство для врачей / Под ред. З.Ш.Гилязутдиновой и М.К.Михайлова. – 2-е изд. – М: МЕДпресс-информ, 2002. – 384 с.
- Опухоли женской репродуктивной системы / В. В.Баринов [и др.]; под общ. ред. М. И.Давыдова, В. П.Летягина, В. В.Кузнецова. – М.: ООО «Медицинское информационное агентство», 2007. – 376 с.
- Батталова, Г.Ю. Причины обращения к врачу больных с опухолями яичников / Г.Ю. Батталова, Г.Ш. Ямалетдинова // III съезд онкологов и радиологов СНГ: материалы съезда, Минск, 25-28 мая 2004 г.: в 2 ч. / МЗ РБ, Ассоциация директоров центров и институтов онкологии, радиологии и рентгенологии СНГ, НАН Беларуси, Гос. Ком. по науке и технологиям РБ, ГУ НИИ ОиМР им. Н.Н. Александрова. – Минск, 2004. – Ч. II. – С. 186 – 187.
- Эхография и доплерометрия при пограничных опухолях яичников /
В.Н. Демидов [и др.] // Ультразвуковая диагностика в акушерстве, гинекологии и педиатрии. – 2000. – Том 8, №4. – С. 289 – 296.
- Винокуров, В.Л. Рак яичников: закономерности метастазирования и выбор адекватного лечения больных / В.Л. Винокуров. – СПб.: ФОЛИАНТ, 2004. – 336с.
- Eagle, K. Tumor Markers in Ovarian Malignancies / K. Eagle, J.A. Ledermann // The Oncologist. – 1997. – N2. – P. 324 – 329.
- Restaging Surgery for Women with Borderline Ovarian Tumors / Raffaele Fauvet [et al] // Cancer. – 2004. – Vol. 100, № 6. – P. 1145 – 1151.
- Olejek A. Guzy jajnika o granicznej złośliwości // Międzynarodowy Kongres Rak Jajnika: Kraków, 18-21 czerwca 2008 / Uniwersytet Jagielloński Wzdział Lekarski. – Kraków, 2008. – S. 13 – 14.
- Survival among Women with Borderline Ovarian Tumors and Ovarian Carcinoma / Mark E. Sherman [et al] // Cancer. – 2004. – Vol. 100, № 5. – P. 1045 – 1052.
- Recurrence After Cystectomy for Borderline Ovarian Tumors: Results of a French Multicenter Study / Christophe Poncelet [et al] // Annals of Surgical Oncology. – 2006. – Vol. 13, № 4. – P. 565 – 571.
- Conservative treatment of borderline ovarian tumors / HD Tazelaar [et al] // Obstet Gynecol – 1985. – № 66. – P. 417 – 422.
- Алгоритмы диагностики и лечения больных злокачественными новообразованиями: утв. Министерством здравоохранения РБ 09.02.07. – Минск, 2007. – 512 с.
- Miller K, Price JH, Dobbs SP, et al. An immunohistochemical and morphological analysis of post-chemotherapy ovarian carcinoma. J Clin Pathol 2008. 61;652-657.
- McCluggage WG. My approach to and thoughts on the typing of ovarian carcinomas. J Clin Pathol 2008;61; 152-163.
Таблица 1. – Характеристика клинических наблюдений
| Признак | Количество больных | ||
| Возраст: | Средний менее 35 лет 36-50 лет 51-65 лет 66 лет и более | 44,7±1,79 21 (29,6%) 23 (32,4%) 21 (29,6%) 6 (8,5%) | |
| ^ Распространение опухоли (FIGO): | Стадия IA Стадия IB Стадия IС Стадия I Стадия IIA Стадия IIB Стадия IIIA Стадия IIIB | 37 (52,1%) 4 (5,6%) 24 (33,8%) 2 (2,8%) 1 (1,4%) 1 (1,4%) 1 (1,4%) 1 (1,4%) | |
Таблица 2. – Сопутствующие заболевания
| Заболевание | Число больных | |
| ^ Сердечно-сосудистые заболевания: | ||
| | ИБС Артериальная гипертензия | 20 (28,2%) 19 (26,8%) |
| ^ Хронические заболевания желудочно-кишечного тракта: | ||
| Холецистит, ЖКБ или холецистопанкреатит Гастрит Язвенная болезнь 12-перстной кишки или желудка | 6 (8,5%) 19 (26,8%) 3 (4,2%) | |
| ^ Болезни органов дыхания (хронический бронхит, бронхиальная астма) | 4 (5,6%) | |
| Заболевания периферических вен (варикозное расширение, тромбофлебиты и др.) | 6 (8,5%) | |
| ^ Хронические урологические заболевания (пиелонефрит, нефролитиаз, цистит, ХПН др.) | 4 (5,6%) | |
| Заболевания репродуктивной системы | ||
| Эрозии шейки матки Хронический аднексит Кисты яичников Миома матки Полипы цевикального канала/эндометрия | 10 (14,1%) 9 (12,7%) 6 (8,5%) 18 (25,4%) 3 (4,2%) | |
Рисунок 1.
 а | 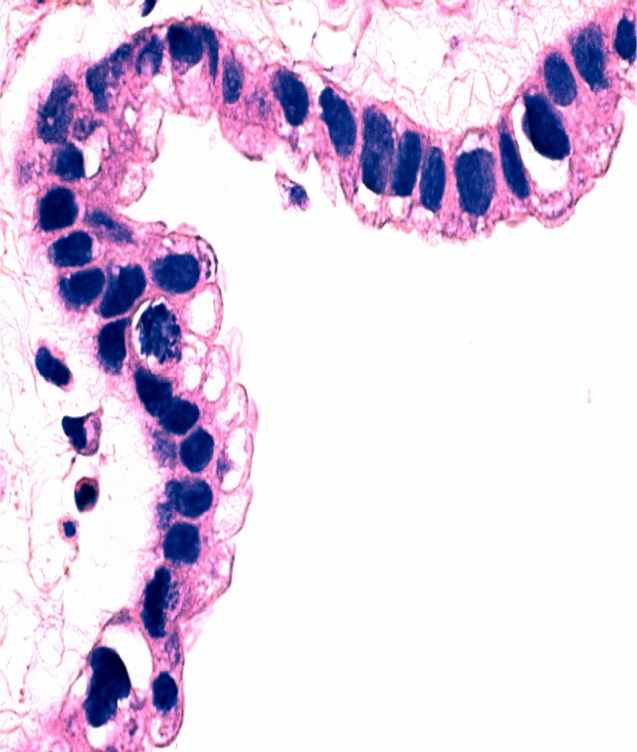 г |
 б | 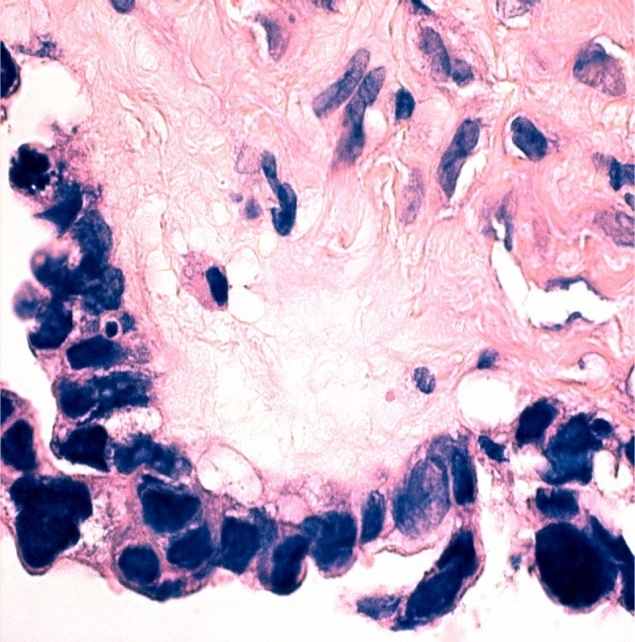 д |
 в | 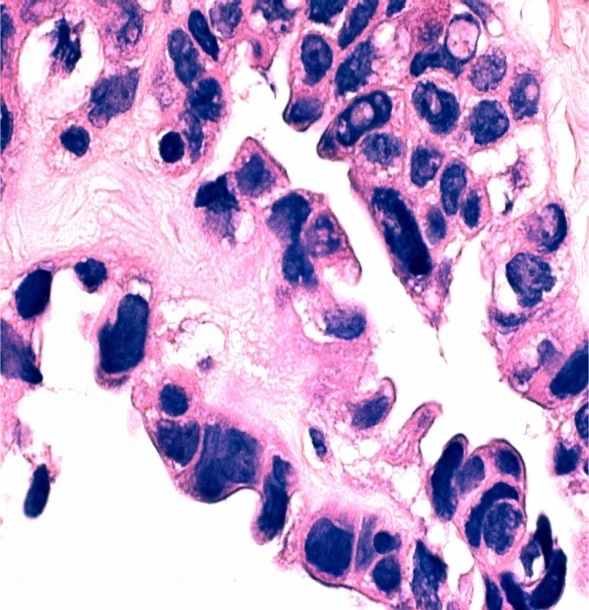 е |
Рисунок 2.
 а | 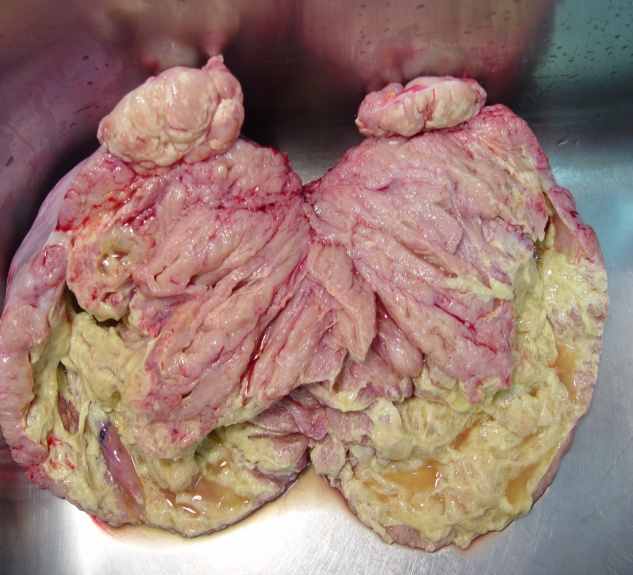 б |
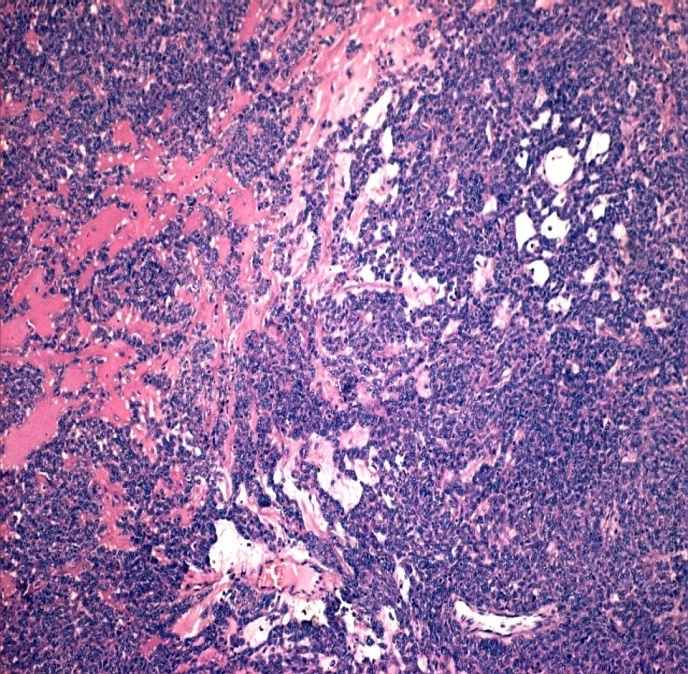 в | 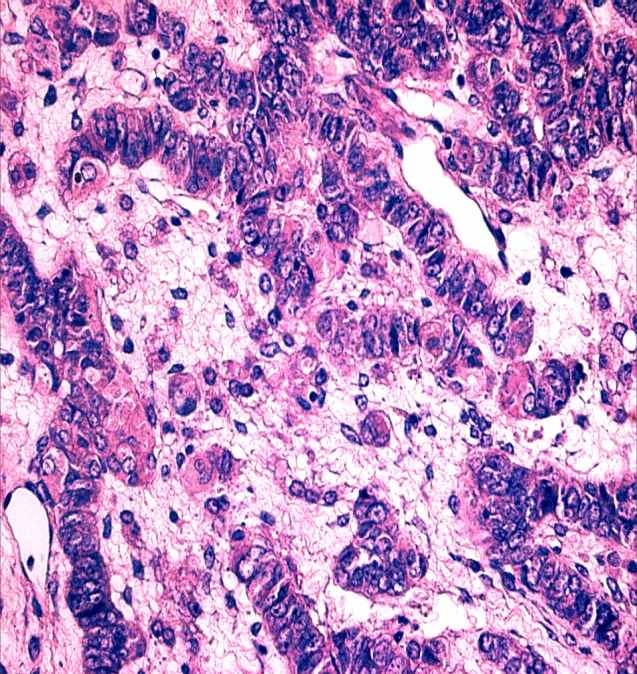 г |
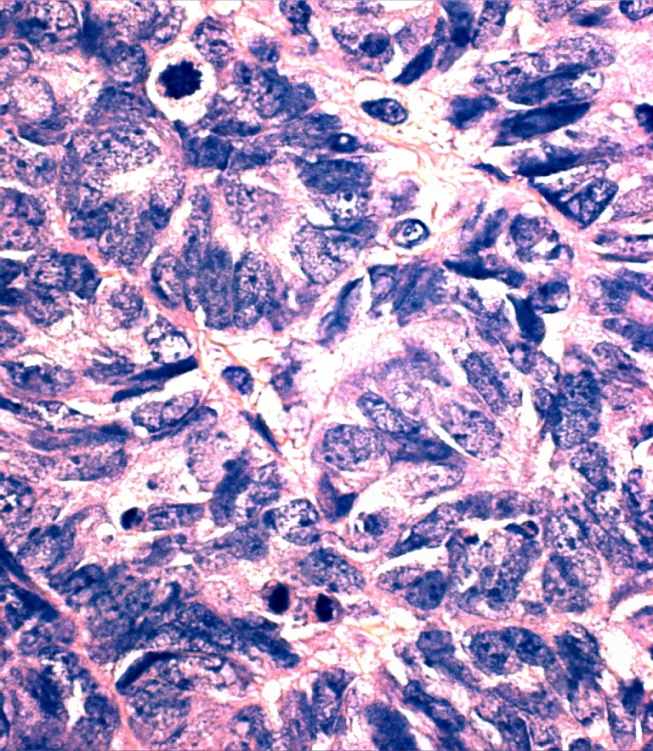 д | 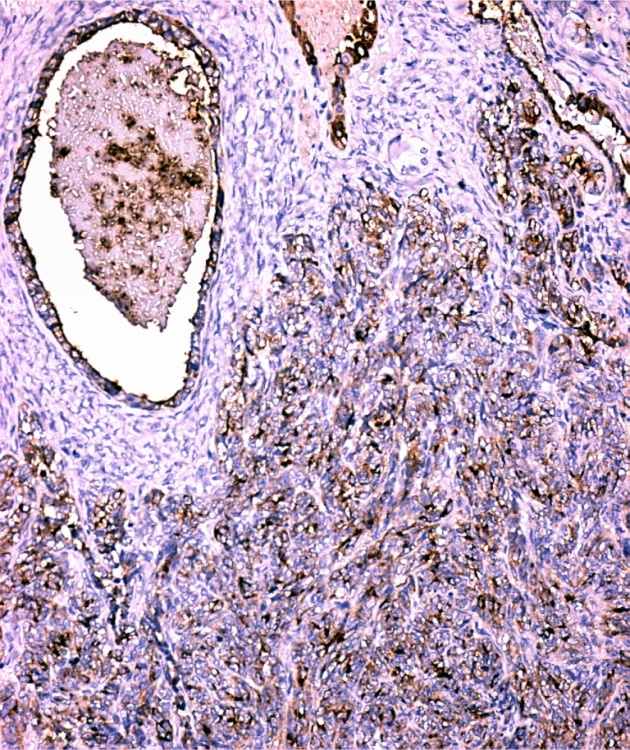 е |
Подписи к рисункам:
Рис.1.
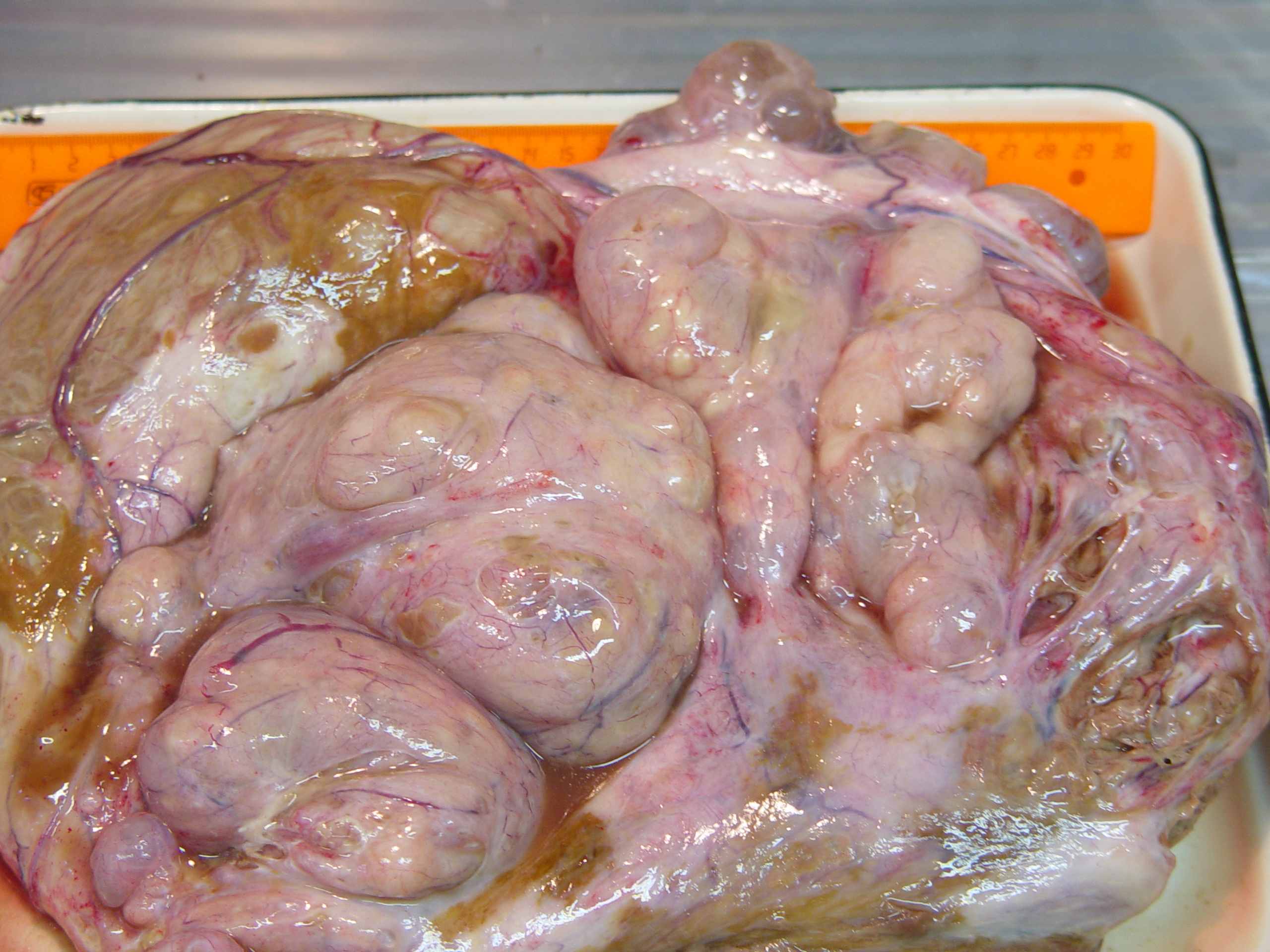
Неинвазивный муцинозный рак яичников: а-в – макроскопический вид (а – на гладкой (непапиллярной) поверхности капсулы видны белесоватые перламутрового вида очаги; б – на разрезе многокамерные гладкостенные кисты с желеобразным содержимым; в - в опухолях больших размерах вследствие повышенного давления и атрофии наблюдается разрыв перегородок, и опухолевая ткань сохраняется в виде желтоватых очагов неправильной формы); г-е – исчезновение секретирующих слизь клеток, выраженный цитологический полиморфизм, образование уродливых гиперхромных ядер и клеточных элементов с внутриядерными включениями, обилие атипических митозов, очаговая папиллоидная гиперплазия. Окраска гематоксилин и эозин, ув. х1000.
Рис.2.
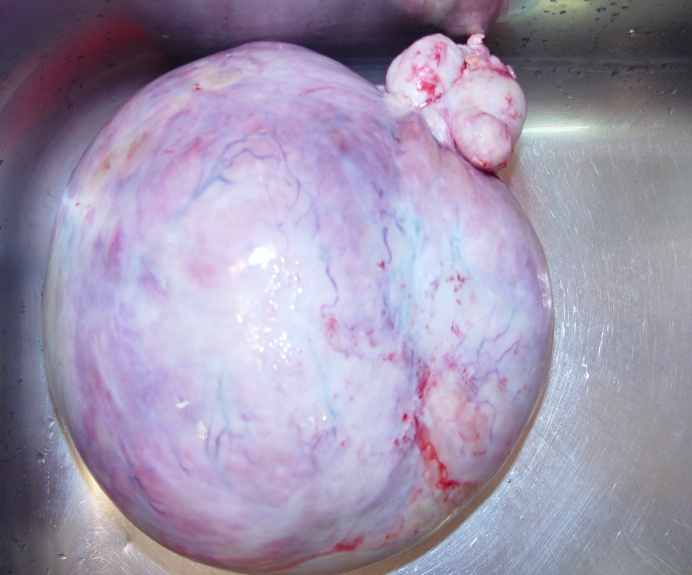
Плохо дифференцированный рак яичников: а – макроскопический вид, прорастание капсулы органа, б – на разрезе видны солидные массы с обширными зонами распада; в,г – крупные участки солидно-инсулярного и трабекулярного строения имитируют архитектонику опухолей из стромы полового тяжа (в – структуры, напоминающие тельца Call-Exner, г – анастомозирующие трабекулярные тяжи и скопления в интерстиции одно- и двуядерных клеток с эозинофильной цитоплазмой копируют формирующуюся половую строму, что характерно для умеренно дифференцированной арренобластомы, или опухоли из клеток Сертоли и Лейдига 2 типа); д – в отличие от опухолей из стромы полового тяжа, клеточный состав неоплазмы у данной пациентки представлен крупными элементами со сдвигом ядерно-цитоплазматического отношения в сторону гипохромного ядра с несколькими мелкими ядрышками, отмечается множество патологических митозов; е – положительный результат окраски с антителами, маркирующими эпителиальное происхождение новообразования (в предоставленном наблюдении – эпителиальный мембранный антиген), как в остатках эндометриоидной цистаденофибромы, так и в солидно-трабекулярных разрастаниях карциномы, свидетельствует в пользу плохо дифференцированного рака. Окраска гематоксилин и эозин (в,г,д). Увеличение х100 (в), х200 (е), х400 (г), х1000 (д).
