Химия структура
| Вид материала | Документы |
- Рабочая программа дисциплины (модуля) «математический анализ», 424.74kb.
- Рабочая программа дисциплины (модуля) «Уравнения математической физики», 266.58kb.
- Рабочая программа дисциплины (модуля) «Линейная алгебра и аналитическая геометрия», 275.82kb.
- Алкилиденанилины: структура и реакционная способность в гидрировании 02. 00. 03 органическая, 495.9kb.
- Утверждаю, 65.11kb.
- Программа «аналитическая химия» по направлению подготовки 020100 «Химия», 31.74kb.
- Химия Химия — наука о веществах, их превращениях и тех явлениях, которыми эти превращения, 890.58kb.
- Рабочая программа по дисциплине «Спектральные методы анализа» для специальности 020101, 175.88kb.
- Управление персоналом вопросы для подготовки к экзамену, 23.69kb.
- «Неорганическая химия», 1345.55kb.
ХИМИЯ
Структура:
1. Фотохимические преобразования.
2. Фотоэффект и радиационная теория катализа А.Эйнштейна.
3. Не является ли кинетическая энергия молекул лишь проявлением поглощенных ФОТОНОВ?
4. «Плененное» излучение.
5. Формы проявления фотона.
6. Механизм взаимодействия фотонов с молекулой (атомом).
7. Эффект нагревания и химическая реакция.
8. Резонансные частоты фотоэффекта.
9. Энергия активации.
10. О митогенетическом излучении и сохранении мощности.
Как меры химии связаны с мерами LT?
Теперь, мы можем говорить о ХИМИИ, которая должна принять «эстафетную палочку» от физики.
Известно, что в химии существуют следующие меры:

Рассмотрим теперь физико-химический фундамент для объяснения явлений неустойчивого равновесия.
Речь пойдет о фотохимических преобразованиях, о фотонике, основой которой является фотон — световой квант.
1. Фотохимические преобразования
 | Известно, что первый шаг в этом направлении сделал в 1905 г. А. Эйнштейн. Однако введенное им понятие квантов энергии было встречено с недоверием ведущими физиками того времени. В работе М. Д. Клейна, опубликованной в «Эйнштейновском сборнике» за 1966 год под названием «Первая работа Эйнштейна по квантам», сказано: «Даже в 1913 г. Макс Планк мог включить следующее замечание в письмо, в котором он предлагал избрать Эйнштейна членом Прусской академии наук и всячески превозносил его труды и дарования: “То, что он иногда бьет мимо цели в своих соображениях, как, например, в связи с гипотезой световых квантов, не может быть поставлено ему в минус”». |
| Альбе́рт Эйнште́йн Albert Einstein (1879—1955) |
Более того, именно Эйнштейн и был тем человеком, который связал фотоэффект с химической реакцией. Так появилась радиационная теория катализа. Теория фотоэффекта получила свое подтверждение только в 1916 году после работ Милликена. Таким образом, в момент становления квантовой статистики многие положения радиационной теории катализа казались весьма спорными.
2. Фотоэффект и радиационная теория катализа А. Эйнштейна
Радиационная теория катализа встретилась с ОДНИМ противоречием — скорости химических реакций оказались ВЫШЕ, чем требовалось от теории, которая действовала в то время. Вычисляя плотность лучистой энергии в сфере химической реакции, приходили к выводу, что такая плотность фотонов в сфере реакции НЕДОСТАТОЧНА для наблюдаемых скоростей реакции.
Теория была «опровергнута» «экспериментально». Опровержение выглядело так. Определяем энергию активации для некоторой химической реакции. Делим полученное выражение на число молекул и вычисляем энергию активации отдельной молекулы. Считаем, что для каждой молекулы требуется излучение с частотой или длиной волны, равной энергии активации. Частота излучения, полученная этим вычислением, оказалась фотохимически неактивной. На таком опровержении и закончилась история радиационной теории катализа.
В настоящее время, когда мы знаем, что резонансная частота должна задаваться с точностью до 1010, а точность вычисления энергии активации не превосходит 5%, мы понимаем, что никакой проверки «экспериментально» не могло производиться вообще!
Если для вакуума скорость света зависит ТОЛЬКО от длины волны и частоты:
c = l ,
где c — скорость света, l — длина волны, — частота; то с учетом показателя преломления n — либо длина волны, либо частота имеет своим сомножителем этот показатель преломления.
c = n l .
Чтобы получить плотность энергии, согласованную со скоростью реакции, достаточно, чтобы показатель преломления имел значение порядка 102.
Поскольку речь идет о РЕЗОНАНСНОМ поглощении, то есть поглощении света, совпадающего с собственной частотой, то на собственных частотах, как известно, показатель преломления стремится к бесконечности (формально из математической формулы), а реально может заметно превосходить величину 102. Таким образом, как теоретически (плотность излучения), так и «экспериментально» — радиационная теория катализа Эйнштейна — выдержала испытание временем.
В настоящее время нет ни одного явления в кинетической теории газов, которое не следовало бы из моделей молекул с квантованием кинетической энергии.
3. Не является ли кинетическая энергия молекул
лишь проявлением поглощенных ФОТОНОВ?
Простой мысленный эксперимент подтверждает эту гипотезу. Если закрыть Землю оболочкой, которая изолирует ее от действия лучистой энергии Солнца, и охладить Землю до абсолютного нуля температур, то вся газовая оболочка нашей планеты превратится в твердое тело с лужицами гелия. Естественно, что в этом мысленном эксперименте мы пренебрегаем теплотой, которая идет из глубинных слоев земного шара.
Этот эксперимент снимает мысленный штамп, связанный со статистическим описанием газа атмосферы как «бильярдных шаров, находящихся в состоянии хаотического беспорядочного движения». При абсолютном нуле этого хаотического беспорядочного движения молекул не наблюдается, то есть такое движение не является СОБСТВЕННЫМ СВОЙСТВОМ молекул. Однако достаточно убрать преграду к доступу солнечного света, и довольно быстро восстановится наблюдаемая нами атмосфера, где над каждым квадратным сантиметром поверхности находится столб, весом в килограмм.
4. «Плененное» излучение
Это позволяет сделать следующий вывод: кинетическая энергия молекул есть ничто иное, как энергия фотонов, поглощенная атмосферой и другими веществами поверхности планеты. Теперь существует термин для этого излучения — «плененное излучение».
Именно признание факта, что кинетическая энергия молекул НЕ ЕСТЬ собственное свойство молекул, а есть результат поглощенных фотонов — позволяет рассматривать кинетическую энергию молекул как энергию «плененного излучения» — этот термин введен в теории лазеров по отношению к накапливаемому излучению.
5. Формы проявления фотона
Во всех квантово-энергетических процессах участвует ФОТОН. Однако он может проявляться в различных формах:
1. В форме электромагнитного излучения в свободном пространстве (в вакууме) с той или иной длиной волны или с той или иной частотой.
2. В форме теплоты, когда эти фотоны претерпели эффект превращения в ТЕПЛОТУ, но только после поглощения их тем или иным ВЕЩЕСТВОМ.
3. В форме химической потенциальной энергии, когда эти фотоны вызвали фотоэффект или фотодиссоциацию. В последнем случае реизлучение уже не следует закону Стефана—Больцмана.
4. В форме кинетической энергии молекул и атомов.
6. Механизм взаимодействия фотонов с молекулой (атомом)
Все эти формы образуются в результате химических взаимодействий на микроуровне. По этой причине требуется рассмотреть механизм взаимодействия фотонов с молекулой (атомом) и ответить на вопросы:
1) Почему некоторые фотоны поглощаются, а некоторые — е поглощаются?
2) Почему некоторые из поглощаемых фотонов приводят к химической реакции, а некоторые фотоны дают только возбуждение молекул и теряются, передаваясь другим молекулам при ударах второго рода или излучаясь в виде люминесценции?
Эти вопросы тесно связаны с фундаментальным вопросом, который был сформулирован ранее: « Куда девается лучистая энергия и как она начинает вновь функционировать?»
Сформулированные выше вопросы являются естественным продолжением поиска решения проблемы на атомно-молекулярном уровне.
Ответ на первый вопрос довольно прост — каждая молекула поглощает те и только те фотоны, которые соответствуют спектру поглощения этой молекулы.
Ответ на второй вопрос сравнительно прост для атомарных спектров благородных газов, где он проявляется в чистом виде.
7. Эффект нагревания и химическая реакция
Если резонансный фотон не достигает энергии фотоионизации, то мы имеем дело с физическим процессом, который является эффектом НАГРЕВАНИЯ. Энергия поглощенного фотона будет обнаруживаться как КИНЕТИЧЕСКАЯ ЭНЕРГИЯ молекулы.
Если резонансный фотон соответствует частоте фотоэффекта, то наблюдается ХИМИЧЕСКИЙ процесс, так как из электрохимии известно, что процессы потери или приобретения электронов являются ХИМИЧЕСКИМИ РЕАКЦИЯМИ. Энергия поглощенного фотона будет обнаруживаться как ПОТЕНЦИАЛЬНАЯ ЭНЕРГИЯ молекулы.
8. Резонансные частоты фотоэффекта
Для многоатомных газов спектр поглощения, связанный с поглощением света и переходом электрона в возбужденное состояние, дополняется переходами не только электронов, но вращательными и колебательными спектрами этой молекулы. Однако и в этом случае, хотя число спектральных линий резко возрастает, имеет место поглощение фотона только тех частот, которые соответствуют спектру (резонансным частотам) той же самой молекулы. Здесь химическая реакция может быть связана не только с чистым фотоэффектом по отношению к электрону, но с фотодиссоциацией молекул.
С другой стороны, среди всех возможных актов поглощения фотонов молекулами газов из ОСНОВНОГО СОСТОЯНИЯ мы выделим только одну частоту, которую будем называть «ЧАСТОТА ФОТОЭФФЕКТА». Именно эту частоту, которая вызывает фотоэффект, молодой Альберт Эйнштейн еще в 1905 году посчитал важнейшей фотохимической константой.
Совершенно очевидно, что имеется кардинальное различие между поглощением фотона с частотой МЕНЬШЕЙ, чем частота фотоэффекта, и частотой, превосходящей эту частоту.
Если частота меньше, то мы имеем ФИЗИЧЕСКИЙ эффект НАГРЕВАНИЯ; если частота превосходит этот порог, то мы имеем дело с ХИМИЧЕСКОЙ РЕАКЦИЕЙ.
Может быть, эта константа и разделяет диссипативные и антидиссипативные процессы и образует физико-химический фундамент для объяснения явлений неустойчивого равновесия, связанного с критической ситуацией первого рода?
9. Энергия активации
В нашем описании отсутствует понятие «ЭНЕРГИЯ АКТИВАЦИИ»; роль этой величины играет энергия первого фотона, обладающего «ЧАСТОТОЙ ФОТОЭФФЕКТА». В экзотермических реакциях энергия этого фотона МЕНЬШЕ, чем энергия выделившихся фотонов. В эндотермических реакциях энергия первого фотона БОЛЬШЕ, чем энергия выделившихся фотонов. Из этого следует, что эндотермические реакции предполагают использование дальнего ультрафиолета, которого сейчас на поверхности планеты практически нет. По утверждению В. И. Вернадского, вся атмосфера Земли — биогенного происхождения. Это означает, что в отсутствии Жизни этот ультрафиолет доходил до поверхности планеты и мог обеспечить протекание реакций синтеза органических веществ из неорганических.
Нетрудно убедиться в том, что понятию «экзотермическая реакция» соответствует понятие «диссипативный процесс», а понятию «эндотермическая реакция» — понятие «антидиссипативный процесс» (рис. 1).
Действительно, энергия активации — это энергия с определенной частотой, т. е.
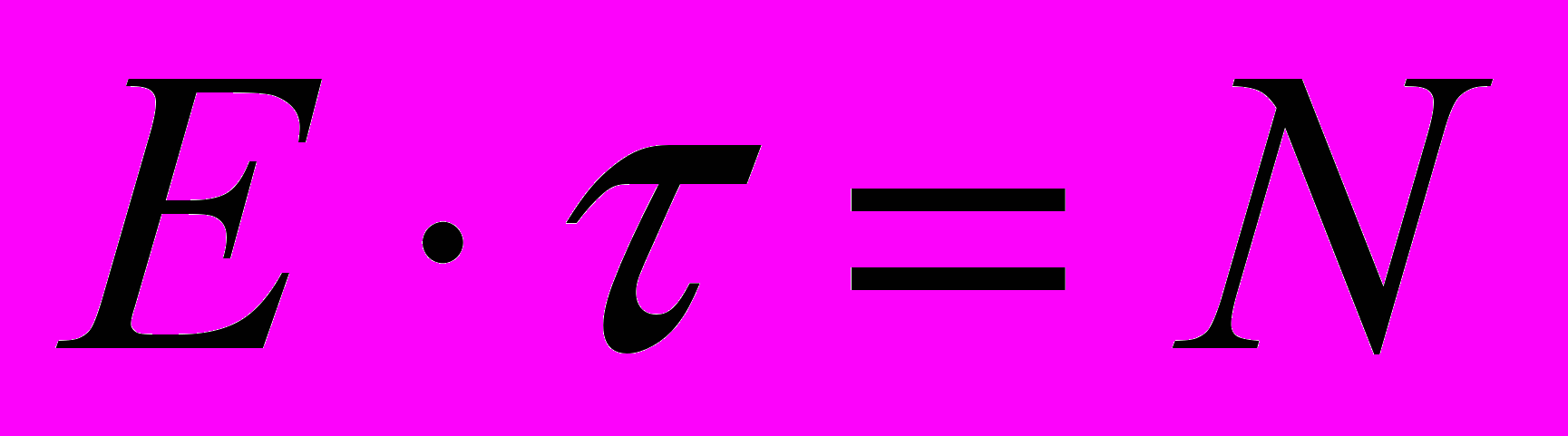 , где — частота [L0 T1], а E — энергия [L5 T4].
, где — частота [L0 T1], а E — энергия [L5 T4].Следовательно, энергия активации — это энергия в единицу времени, имеющая размерность мощности [L5 T].
Из закона сохранения мощности следуют условия протекания экзотермических и эндотермических реакций:
1. Если полная мощность N (энергия первого фотона) меньше мощности потерь (выделенной энергии) G , т. е.
N – G < 0,
имеет место диссипативный процесс рассеяния свободной энергии фотона, который и соответствует типу экзотермической реакции.
2. Если полная мощность N больше мощности потерь G , т.е .
N – G > 0,
имеет место антидиссипативный процесс накопления свободной энергии фотона, который соответствует типу эндотермической реакции.
3. Если полная мощность оказывается равной мощности потерь, имеет место критическая ситуация первого рода.
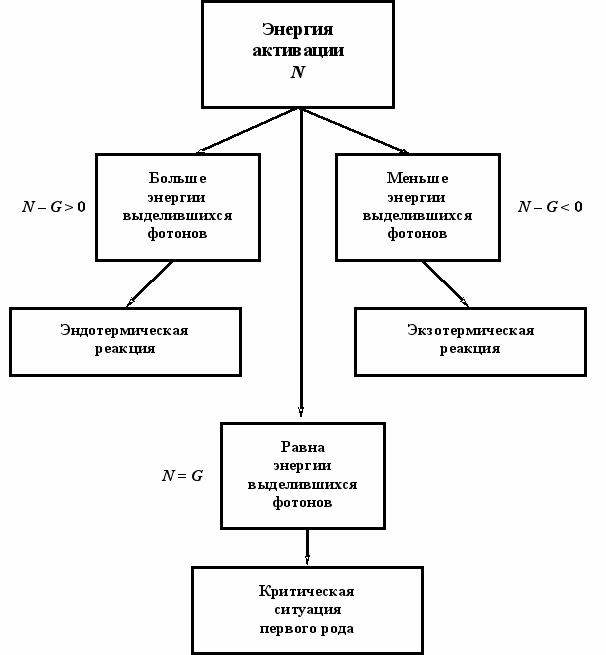
Рис. 1
10. О митогенетическом излучении и сохранении мощности
В свое время было много дискуссий, связанных с митогенетическим излучением А. Г. Гурвича. В собственных публикациях А. Г. Гурвича считается, что это открытие сделано в 1924 году. В Собрании сочинений академика П. П. Лазарева это открытие отнесено им к 1923 году. В сочинениях П. П. Лазарева этому излучению отводится весьма заметная роль и приведены экспериментальные данные Г. М. Франка, получавшего спектры митогенетического излучения с использованием биологических детекторов.
Если использовать уравнения химических реакций с участием фотонов, то нет никакого сомнения, что такое хемилюминесцентное излучение должно сопровождать ВСЕ химические реакции, образующие понятие «ОБМЕНА ВЕЩЕСТВ» в любом живом организме.
Для поддержания этого процесса всегда нужно расходовать мощность. Принцип сохранения МОЩНОСТИ является тем малоизвестным фактом, который тесно связан с теорией биологического поля всех живых организмов. ВСЕ живые организмы нуждаются просто для своего сохранения, т. е. нормального обмена веществ, в постоянном притоке ЭНЕРГИИ. Этот ПОТОК ЭНЕРГИИ и есть МОЩНОСТЬ. Но только ли живые организмы и технологические процессы связаны с потоком энергии или мощностью? Рассмотрим простой факт СУЩЕСТВОВАНИЯ поля температур вокруг Солнца. Это поле температур измеряется и вычисляется из величины мощности, падающей на единицу поверхности (по закону Стефана—Больцмана). Само Солнце на ПОДДЕРЖАНИЕ этого поля температур расходует до 4-х миллионов тонн массы, которую уносит в каждую секунду электромагнитное излучение. Часть этого потока падает на поверхность нашей планеты. Величина мощности, которая непрерывно падает на нашу планету, составляет 1014 кВт. Часть этого потока, перехватывается фотосинтезом растений и служит источником мощности, поддерживающим существование всей биосферы, т. е. всей совокупности всех форм ЖИЗНИ нашей планеты.
Таким образом, мы переходим к явлениям живой природы.
Заключение
В разделе «Химия» мы продолжили обсуждение проблемы измерения диссипативных и антидиссипативных процессов и рассмотрели только три вопроса:
- Как меры химии связаны с мерами LT?
- Как на химическом уровне объясняются явления неустойчивого равновесия?
- Как установить мостик между химическими реакциями, диссипативными и интидиссипативными процессами?
В результате рассмотрения этих вопросов мы пришли к определенным выводам.
Выводы
- Меры химии — масса атома, число структурных элементов в единице массы и объема, заряд электрона, валентность элемента, энергия элемента, энтальпия молярная — могут быть выражены в пространственно-временных единицах LT-размерности.
- Во всех квантово-энергетических процессах участвует фотон. Он может проявляться в различных формах:
1. электромагнитное излучение (свободное пространство);
2. теплота (после поглощения фотона веществом);
3. потенциальная энергия (фотоэффект);
4. кинетическая энергия («плененное» излучение).
- Если частота фотона меньше частоты фотоэффекта, то наблюдается эффект нагревания. Если частота фотона больше частоты фотоэффекта, то наблюдается химическая реакция.
- Если энергия активации первого фотона с частотой фотоэффекта, т. е. его полная мощность, меньше мощности потерь (выделенного потока энергии), то имеет место фотохимическая экзотермическая реакция — имеет место процесс диссипации.
- Если энергия активации первого фотона с частотой фотоэффекта, т. е. его полная мощность, больше мощности потерь, то имеет место фотохимическая эндотермическая реакция — доминирует антидиссипативный процесс.
- Если полная мощность оказывается равной мощности потерь, имеет место неустойчивое равновесие, определенное в разделе «Физика» как критическая ситуация первого рода.
- Реакции синтеза органических веществ из неорганических могут рассматриваться как разрешение критической ситуации первого рода — сменой типа фотохимической реакции.
