Отдаленные результаты применения моноклональных анти-ige антител в комплексной терапии тяжелой неконтролируемой атопической бронхиальной астмы 14. 01. 25 пульмонология
| Вид материала | Автореферат |
- Лабораторные методы исследования в диагностике аллергий, 15.05kb.
- Обоснование целесообразности применения метода компьютерной электроакупунктуры в комплексной, 353.98kb.
- На правах рукописи, 611.91kb.
- Эффективность галотерапии в комплексе реабилитации при атопическом дерматите у детей, 61.6kb.
- Клинико-иммунологическая характеристика обострений бронхиальной астмы 14. 00. 43 пульмонология, 423.16kb.
- Взрослых, 178.64kb.
- А. Г. Логвиненко, С. И. Логвиненко, И. А. Логвиненко, 58.39kb.
- Морфофункциональные аспекты сопряженности бронхиальной астмы и гастроэзофагеального, 146.61kb.
- Принципы терапии аллергических заболеваний, 781.38kb.
- Применение нутрицевтиков при комплексном санаторном лечении бронхиальной астмы и атопического, 248.85kb.
На правах рукописи
Сучкова Юлия Борисовна
ОТДАЛЕННЫЕ РЕЗУЛЬТАТЫ ПРИМЕНЕНИЯ МОНОКЛОНАЛЬНЫХ АНТИ-IgE АНТИТЕЛ В КОМПЛЕКСНОЙ ТЕРАПИИ ТЯЖЕЛОЙ НЕКОНТРОЛИРУЕМОЙ АТОПИЧЕСКОЙ
БРОНХИАЛЬНОЙ АСТМЫ
14.01.25 – пульмонология
АВТОРЕФЕРАТ
диссертации на соискание ученой степени
кандидата медицинских наук
Москва – 2010
Работа выполнена в Федеральном государственном учреждении «Научно-исследовательский институт пульмонологии» Федерального медико-биологического агентства России
Научный руководитель:
Доктор медицинских наук Осипова Галина Леонидовна
Официальные оппоненты:
Доктор медицинских наук, профессор Абросимов Владимир Николаевич
Рязанский государственный медицинский университет им. академика Павлова
Доктор медицинских наук, профессор Ненашева Наталия Михайловна
Российская медицинская академия последипломного образования
Ведущая организация: Московская Медицинская Академия
им. И.М. Сеченова Росздрава.
Защита состоится «______»________________2010г. в _____ часов на заседании диссертационного совета Д.208.053.01 при ФГУ «НИИ пульмонологии» ФМБА России (105077, г. Москва, 11-я Парковая, 32)
С диссертацией можно ознакомиться в библиотеке ФГУ «НИИ пульмонологии» ФМБА России (105077, г. Москва, ул.11-я Парковая, 32)
Автореферат разослан «______»_________________2010г.
Ученый секретарь диссертационного совета,
доктор медицинских наук Анаев Эльдар Хусеевич
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность проблемы
Многочисленные эпидемиологические исследования свидетельствуют о широкой распространенности и неуклонном росте бронхиальной астмы (БА). В настоящее время в мире насчитывается около 300 млн. больных этим заболеванием, а в России число пациентов с БА составляет 55 млн. человек (GINA, 2006; Woolcock A.J. et al., 1997; Ненашева Н.М., 2008).
Основной целью лечения БА является достижение и поддержание оптимального контроля заболевания (Weel C. et al., 2008; Черняк Б.А., Воржева И.И., 2008), под которым подразумевается отсутствие или минимальная частота возникновения симптомов, отсутствие ограничений активности и обострений БА, нормальные значения объема форсированного выдоха за 1 секунду (ОФВ1) и пиковой скорости выдоха. Однако, несмотря на наличие эффективных методов терапии БА, полный контроль заболевания поддерживается только у 5,3 – 42% больных (Bateman E. et al., 2004; Rabe K. et al., 2000), а неконтролируемое течение БА встречается у 51% больных (Partridge M.R. et al., 2006; Белевский А.С., Вознесенский Н.А., 2005). В России недостаточный контроль заболевания также является актуальной проблемой, и наибольший процент больных с неконтролируемым течением БА наблюдается в группе с тяжелым течением заболевания, который составляет 78,4% (Чучалин А.Г., 2004).
Среди больных БА от 40 до 67% имеют атопическую форму заболевания (Novak N. et al., 2003; Pearce N et al., 1999), центральную роль в развитии которой играет иммуноглобулин Е (IgE) (Oettgen H.C. et al., 2001). В связи с этим при лечении атопической БА большое значение приобретают лекарственные препараты, мишенью действия которых является IgE.
Первым препаратом этой группы, разрешенным к применению в клинической практике, является омализумаб, моноклональные анти-IgE антитела (АТ) (Kuhn R. et al., 2007), которые, связываясь с циркулирующим IgE и препятствуя его последующему взаимодействию с высокоаффинными рецепторами на тучных клетках и базофилах, предотвращают развитие ответа ранней фазы аллергического воспаления. Показано также уменьшение выраженности ответа поздней фазы аллергического воспаления под влиянием терапии моноклональными анти-IgE АТ (Djukanojvic R. et al., 2004). Проведенные в мире контролируемые исследования свидетельствуют об эффективности и безопасности анти-IgE терапии в лечении аллергических заболеваний, сопровождающихся повышением уровня IgE, включая тяжелую неконтролируемую атопическую БА (Maykut R.J. et al., 2008, Mossop E.P. et al., 2009).
В России в настоящее время отсутствуют данные по применению моноклональных анти-IgE АТ в силу сравнительно недавнего внедрения этого метода лечения в отечественное здравоохранение, а также ощущается необходимость в систематизации данных по их применению. Из-за достаточно высокой стоимости такого лечения длительное непрерывное назначение анти-IgE терапии может быть сопряжено с определенными экономическими трудностями. Терапия моноклональными анти-IgE АТ также связана с необходимостью как в регулярных визитах пациента в клинику (каждые 2 или 4 недели) для инъекций препарата, так и в последующем врачебном наблюдении в течение 2 часов после инъекции.
Исходя из вышесказанного, необходимым представляется изучение эффективности и безопасности длительного применения моноклональных анти-IgЕ АТ у больных тяжелой неконтролируемой атопической БА, а также разработка оптимальной схемы их назначения, предусматривающей ее прерывность, которая, тем не менее, обеспечит достижение и поддержание оптимального контроля БА в течение всего периода лечения.
Цель исследования:
Оценить эффективность и безопасность применения моноклональных анти-IgE антител в комплексной терапии тяжелой неконтролируемой атопической бронхиальной астмы и разработать схему их дискретного применения.
Задачи исследования:
- Провести ретроспективный анализ применения моноклональных анти-IgE антител в России (включая оценку клинической симптоматики, частоты внеплановых визитов к врачу, обострений и госпитализаций, динамики показателей ФВД, объема получаемой терапии) у пациентов с тяжелой неконтролируемой атопической бронхиальной астмой.
- Изучить динамику клинико-иммунологических показателей при использовании моноклональных анти-IgE антител.
- Оценить изменения уровня контроля бронхиальной астмы на фоне применения моноклональных анти-IgE антител в ближайшем и отдаленном периодах наблюдения.
- Изучить влияние анти-IgE терапии на динамику показателей качества жизни пациентов в ближайшем и отдаленном периодах наблюдения.
- Оценить длительность сохраняющейся эффективности анти-IgE терапии после отмены препарата.
Научная новизна:
Впервые:
- в России проведена оценка многолетнего клинического опыта, подтвердившая эффективность и безопасность применения моноклональных анти-IgE антител у больных тяжелой неконтролируемой атопической бронхиальной астмой.
- проведен анализ длительного применения моноклональных анти-IgE антител у больных тяжелой неконтролируемой атопической бронхиальной астмой.
- разработана схема дискретного применения моноклональных анти-IgE антител у больных тяжелой неконтролируемой атопической бронхиальной астмой и доказана ее эффективность.
Практическая значимость:
- Доказана эффективность в достижении контроля заболевания и безопасность применения моноклональных анти-IgE антител в комплексной терапии тяжелой неконтролируемой атопической бронхиальной астмы, что диктует необходимость внедрения их в клиническую практику.
- Показано, что анти-IgE терапия может осуществляться в дискретном режиме.
Внедрение в практику здравоохранения
Разработанная схема курсового лечения моноклональными анти-IgE антителами внедрена в лечебную практику аллергологического отделения и аллергокабинета ГКБ № 57.
Основные положения диссертации, выносимые на защиту:
- Применение моноклональных анти-IgE антител в комплексной терапии тяжелой неконтролируемой атопической бронхиальной астмы повышает эффективность проводимого лечения и позволяет достичь контролируемого течения заболевания у 47,8% больных в течение первого года лечения и у 61,5% больных при дальнейшем длительном их применении, что значительно повышает качество жизни больных.
- Моноклональные анти-IgE антитела при длительном применении не вызывали побочных эффектов, которые требовали их отмены и приводили к ухудшению состояния больных.
- Моноклональные анти-IgE антитела в комплексной терапии тяжелой неконтролируемой атопической бронхиальной астмы могут применяться дискретно, возможный перерыв между курсами лечения не должен превышать 2 месяцев, более длительное прерывание анти-IgE терапии приводит к статистически значимому ухудшению клинических показателей и качества жизни больных.
Апробация работы
Основные положения диссертационной работы доложены и обсуждены на: IV Международной Конференции по иммунотерапии (г. Москва, 2008), итоговых научных сессиях ФГУ «НИИ пульмонологии» ФМБА России (г. Москва, 2008, 2009), XIX Национальном Конгрессе по болезням органов дыхания (г. Москва, 2009), совместной конференции ФГУ «НИИ пульмонологии» ФМБА России и кафедры госпитальной терапии педиатрического факультета ГОУ ВПО РГМУ Росздрава (г. Москва, 2010).
Публикации по теме диссертации
По теме диссертации опубликовано 6 печатных работ, в том числе 1 статья в журнале, входящем в перечень ведущих рецензируемых научных журналов и изданий, рекомендованных ВАК.
Объем и структура диссертации
Диссертация изложена на 151 странице машинописного текста и состоит их введения, обзора литературы, описания материалов и методов исследования, результатов собственных исследований, обсуждения полученных результатов, выводов и практических рекомендаций. Библиографический указатель включает 223 источника, в том числе 45 отечественных и 188 зарубежных авторов. Диссертация иллюстрирована 28 таблицами, 23 рисунками.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
В исследовании проводился анализ данных по применению моноклональных анти-IgE АТ за период с 1998 по 2009 г. Исследование проводилось на базе ФГУ НИИ пульмонологии ФМБА России и аллергокабинета КДО ГКБ № 57.
Проведенное исследование состояло из трех этапов.
На I этапе был проведен ретроспективный анализ эффективности и безопасности лечения моноклональными анти-IgE АТ на основании архивных данных пациентов, получавших лечение с 1998 по 2005 г. Всего было проанализировано 27 амбулаторных карт пациентов с атопической БА тяжелого неконтролируемого течения, которым в 1998-1999 гг. впервые было назначено лечение моноклональными анти-IgE АТ. Исследуемые показатели оценивались в исходной точке до начала терапии, а также на 16 неделе и на 32 и 44 неделях лечения.
На II этапе была проведена оценка отдаленных результатов моноклональными анти-IgE АТ, в него были включены 13 больных с атопической БА, получавших анти-IgE терапию с 1998 по 2005 г. Перерыв в лечении моноклональными анти-IgE АТ составлял 1,5 года, во время него больные продолжали получать базисную терапию. Нами были проанализированы клинико-функциональные показатели и показатели качества жизни (КЖ) после перерыва в лечении, а также их динамика на фоне возобновления анти-IgE терапии на 16 неделе и на 32 и 44 неделях лечения. Описываемый этап исследования проводился в 2007-2008 гг.
На III этапе в исследование было включено 46 пациентов с верифицированным диагнозом атопическая БА тяжелого неконтролируемого течения, обследованных в ФГУ НИИ пульмонологии ФМБА России и не получавших ранее лечение моноклональными анти-IgE АТ. Больные были разделены на 2 группы: первая группа (n=23) получала анти-IgE терапию в дополнение к стандартной базисной терапии, вторая группа (сравнения) (n=23) получала только стандартную базисную терапию. Исследуемые показатели измерялись как до начала терапии, так и на 16 неделе и на 32 и 44 неделях лечения. Для определения длительности сохраняющегося эффекта анти-IgE терапии исследуемые показатели были оценены в динамике на фоне ее прерывания. Пациенты находились под наблюдением с 2008 по 2009 г. Характеристика изучаемых групп больных представлена в таблице 1.
Дизайн исследования.
I этап: Открытое ретроспективное исследование.
II этап: Открытое проспективное исследование.
III этап: Открытое сравнительное проспективное исследование.
Таблица 1. Характеристика изучаемых групп больных
| Этапы | Группы | Число больных | Возраст (лет) | Мужчин | Женщин | Длительность заболевания (годы) |
| Этап I 1998 г. | Моноклональные анти-IgE АТ | 13 | 51,9±9,7 | 4 | 9 | 9,2±1,8 |
| Группа сравнения | 14 | 48,9±7,7 | 3 | 11 | 7,2±2,8 | |
| Этап II 2007 г. | Моноклональные анти-IgE АТ | 13 | 59,3±8,8 | 4 | 9 | 20,07±9,55 |
| Этап III 2008 г. | Моноклональные анти-IgE АТ | 23 | 42,91±10,9 | 6 | 17 | 15,05±7,28 |
| Группа сравнения | 23 | 49,8±13,2 | 5 | 18 | 14,7±11,15 |
Критерии включения в исследование:
- Возраст пациентов от 18 до 70 лет.
- Пациенты с верифицированным диагнозом атопическая БА тяжелого неконтролируемого течения с подтвержденной аллергией к бытовым и эпидермальным аллергенам.
- Уровень общего IgE в пределах от 30 до 700 МЕ\мл.
- Полученное согласие пациента на участие в исследовании.
- Отсутствие в анамнезе тяжелых анафилактических и анафилактоидных реакций.
- Отсутствие активного заболевания легких, кроме БА.
- Отсутствие других, кроме атопии, причин повышения уровня IgE.
- Отсутствие сопутствующей паразитарной инвазии.
- Отсутствие АСИТ на момент включения в исследование.
Критерии исключения из исследования:
- Наличие курения в анамнезе или на момент включения в исследование.
- Наличие у пациента тяжелой сопутствующей патологии (онкологические, гематологические, сердечно-сосудистые заболевания, патология эндокринной системы и др.).
- Беременные женщины, кормящие грудью, или женщины детородного возраста, не применяющие методов контрацепции.
- Наличие сведений о злоупотреблении пациентом лекарственными средствами или алкоголем.
- Невозможность пациента выполнить условия протокола исследования, в том числе смена пациентом места жительства.
- Отказ пациента от участия в исследовании.
Методы исследования
Верификация диагноза БА и оценка эффективности и безопасности проводимого лечения осуществлялась с помощью следующих основных методов исследования:
- Клиническое обследование и сбор аллергологического анамнеза. У всех больных проводилась оценка частоты возникновения дневных и ночных симптомов заболевания, частоты обострений БА, частоты внеплановых визитов к врачу и госпитализаций, потребности в ингаляциях β2-агонистов короткого действия, суточных доз ингаляционных глюкокортикостероидов (ИГКС) в пересчете на беклометазона дипропионат (БД) и системных глюкокортикостероидов (СГКС). Попытки уменьшения доз ИГКС предпринимались через 12 недель терапии, снижение проводилось постепенно каждые 2 недели, вначале до 1500 мкг в сутки, если текущая доза была более 1750 мкг в сутки, и на 250 мкг, если текущая доза составляла менее 1750 мкг в сутки. Все больные заполняли тест по контролю над астмой (АСТтм).
Оценка контроля БА осуществлялась согласно критериям GINA пересмотра 2006 г.
- Лабораторно-инструментальные методы обследования (исследование показателей ФВД, определение уровня общего IgE в сыворотке крови, определение аллергенспецифической гиперчувствительности, включая постановку и оценку аллергологических кожных проб, а также определение уровня специфических IgE АТ в сыворотке крови, исследование показателей иммунного статуса).
- Исследование КЖ больных с использованием валидизированного опросника по качеству жизни больных БА (Asthma Quality of Life Questionnaire) (AQLQ).
Характеристика моноклональных анти-IgE антител, дозирование и способ введения
В исследовании мы применяли омализумаб (Ксолар, Новартис Фарма АГ, Швейцария), регистрационный номер ЛСР-000082. Препарат представляет собой лиофилизированный порошок белого цвета, не содержащий консервантов. В одном флаконе содержится 75 или 150 мг действующего вещества, в качестве растворителя используется вода для инъекций. Препарат вводился подкожно в область дельтовидной мышцы в дозе 150-375 мг каждые 2 или 4 недели. Расчет дозы и частоты инъекций препарата производился индивидуально на основании исходной концентрации IgE (МЕ/мл), измеренной до начала лечения, а также массы тела пациента (кг) с помощью таблицы по дозированию. На II этапе исследования в связи с тем, что перерыв в лечении составлял более 1 года (1,5 года), необходимые дозы моноклональных анти-IgE АТ рассчитывались после повторного измерения уровня общего сывороточного IgE и массы тела больного.
Статистическая обработка полученных данных проводилась с помощью пакета прикладных программ Statistica 6.0. Анализ соответствия вида распределения признака закону нормального распределения проводился с использованием критерия Шапиро-Уилка. Признаки, имеющие нормальное распределение, анализировались при помощи параметрических методов статистики, для анализа признаков, распределение которых было отличным от нормального использовались непараметрические критерии. Для оценки статистической значимости различий при сравнении двух несвязанных между собой групп использовался критерий Стьюдента и непараметрический критерий Манна-Уитни. При анализе повторных измерений использовался парный критерий Стьюдента и непараметрический критерий Вилкоксона. Различия считались статистически значимыми при р<0,05. Данные представлены в виде ±s ; Me(25%-75%), где – выборочное среднее, s – выборочное стандартное отклонение, Ме – медиана, 25%-75% - интерквартильный размах (значения 25-го и 75-го процентилей соответственно).
РЕЗУЛЬТАТЫ СОБСТВЕННЫХ ИССЛЕДОВАНИЙ И ИХ ОБСУЖДЕНИЕ
I этап. Ретроспективный анализ эффективности и безопасности лечения моноклональными анти-IgE антителами
При проведении анализа архивного материала было выявлено, что все пациенты на момент назначения анти-IgE терапии отвечали всем критериям включения в исследование. Среднее значение общего сывороточного IgE в исследуемой группе больных составило 284,1±20 МЕ/мл. Исходные значения изучаемых клинико-функциональных показателей до назначения анти-IgE терапии представлены в таблице 2.
Таблица 2. Исходные значения клинико-функциональных показателей у больных, получавших лечение моноклональными анти-IgE АТ и больных группы сравнения (ретроспективный анализ)
| Показатели | Группы больных | |
| Моноклональные анти-IgE АТ | Группа сравнения | |
| Частота обострений БА в год | 5,1±0,44 | 5,1±0,4 |
| Частота госпитализаций в год | 2,0±0,17 | 2,6±0,3 |
| Частота внеплановых визитов к врачу в год | 12,2±0,3 | 13,6±0,8 |
| Частота ингаляций β2-агонистов короткого действия в сутки | 8,0±0,64 | 8,1±0,64 |
| Доза ИГКС (БД, мкг/сут) | 1749,0±43,2 | 2015,7±101,3 |
| Доза СГКС (преднизолон, мг/сут) | 6,8±0,6 | 6,3±1,4 |
| ОФВ1, % от должного | 62,6±0,4 | 62,8±0,4 |
В группе больных, получавших анти-IgE терапию, выявлено статистически значимое снижение частоты ингаляций β2-агонистов короткого действия - до 7,0±0,48 на 16 неделе лечения и 5,2±0,3 (р<0,01) на 32 неделе терапии. В группе сравнения статистически значимых различий данного показателя на протяжении всего периода наблюдения выявлено не было, средние значения составили 7,0±0,48 на 16 неделе и 7,3±0,32 на 32 неделе наблюдения.
Проведенный ретроспективный анализ показал статистически значимое уменьшение в 5 раз количества обострений БА за год (1,0±0,1 (р<0,05)), больные не госпитализировались в течение всего периода наблюдения, отмечено также снижение в 1,7 раза внеплановой обращаемости в поликлинику (7,25±0,2 (р<0,01)) на фоне лечения моноклональными анти-IgE АТ. В группе сравнения эти показатели оставались высокими – 4,25±0,3, 2,2±0,2 и 13,1±0,8 соответственно, различия по сравнению с исходными данными были статистически незначимы (рис. 1 и 2).
Анализ изменений суточных доз ИГКС показал, что к концу 32 недели лечения в группе больных, получавших моноклональные анти-IgE АТ, дозы ИГКС были снижены в 3,5 раза и составляли 499,9±64 мкг/сут (р<0,05) в пересчете на БД. 4 больных из этой группы прекратили принимать ИГКС. В группе сравнения суточные дозы ИГКС оставались высокими и среднее их значение составляло 1936±101,8 мкг/сут. Статистически значимых различий по сравнению с исходными данными выявлено не было, отмены ИГКС не удалось добиться ни у одного больного.
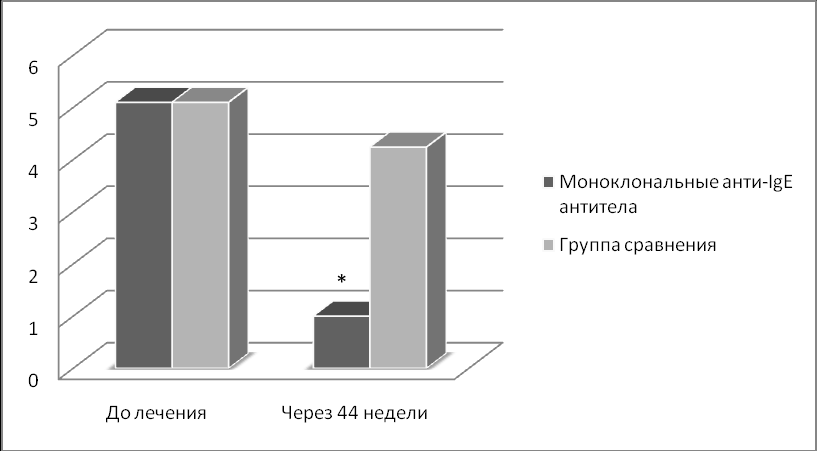
* р<0,05 в сравнении с исходным значением
Рисунок 1. Динамика частоты обострений в год (ретроспективный анализ).
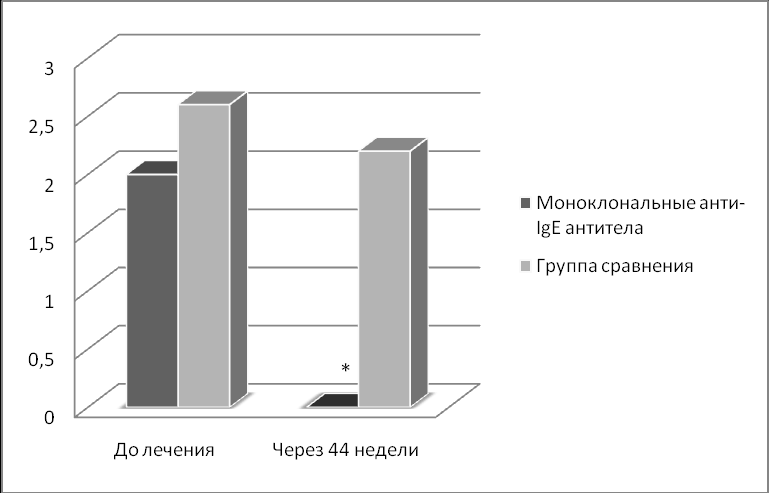
* р<0,01 в сравнении с исходным значением
Рисунок 2. Динамика частоты госпитализаций в год (ретроспективный анализ).
В группе больных, получавших лечение моноклональными анти-IgE АТ, к концу периода наблюдения СГКС прекратили принимать 3-е больных из 3-х получавших. В группе сравнения только у 1 больного удалось снизить суточную дозу преднизолона с 10 мг до 7,5 мг, среднее значение принимаемых СГКС составило 6,8±0,9 мг в сутки, статистически значимых различий указанного показателя в сравнении с исходным значением не выявлено.
Статистически значимое улучшение ФВД было получено в группе больных, получавших моноклональные анти-IgE АТ: показатель ОФВ1 составил 63,5±0,69% на 16 неделе и 81,4±0,43% (р<0,01) на 32 неделе лечения. В группе сравнения среднее значение ОФВ1 было равным 62,8±0,4% на 16 неделе и 65,6±0,24 % на 32 неделе наблюдения соответственно. Различия указанных показателей в сравнении с исходными были статистически незначимыми.
При оценке динамики КЖ больных на фоне лечения моноклональными анти-IgE АТ нами было получено статистически значимое его улучшение по всем пяти изучаемым критериям (таблица 3). В группе сравнения значимых изменениях в изучаемых критериях КЖ выявлено не было.
Анализ архивных данных показал хорошую переносимость проводимой терапии, побочных явлений выявлено не было, связанных с применением моноклональных анти-IgE АТ выявлено не было.
Ретроспективный анализ показал значительную эффективность терапии моноклональными анти-IgE АТ в достижении контроля атопической БА тяжелого течения и улучшении КЖ больных, а также отсутствие серьезных побочных эффектов. Однако полученных данных было недостаточно для оценки долговременного контроля БА при длительной анти-IgE терапии.
Таблица 3. Динамика критериев КЖ по опроснику AQLQ в группе больных, получавших моноклональные анти-IgE АТ
| Критерии | Периоды наблюдения | ||
| До начала лечения | 16 недель | 32 недели | |
| Общее КЖ, баллы | 2,8±0,06 | 4,2±0,04 * | 4,7±0,07 ** |
| Симптомы, баллы | 3,7±0,06 | 4,3±0,3 * | 4,9±0,1 ** |
| Ограничение активности, баллы | 3,6±0,1 | 4,1±0,02 | 4,8±0,1 ** |
| Эмоциональная сфера, баллы | 2,8±0,05 | 4,7±0,1* | 4,8±0,06 |
| Влияние окружающей среды, баллы | 2,8±0,1 | 3,8±0,04 * | 4,4±0,09 ** |
* - р<0,05 по сравнению с исходными данными;
** - р<0,05 по сравнению с результатами, полученными через 16 недель терапии.
II этап. Оценка отдаленных результатов применения моноклональных анти-IgE антител
Для оценки отдаленных результатов проводимого лечения в 2007 г. был спланирован и проведен II этап исследования, в который была набрана группа из 13 больных получавших лечение моноклональными анти-IgE АТ с 1998-1999 по 2005 г. В таблице 4 показано, что после перерыва в лечении, который был равным 1,5 годам, в исследуемой группе больных было отмечено ухудшение клинической симптоматики, что выражалось в увеличении количества обострений и госпитализаций и снижении показателя ОФВ1. У больных отмечалось увеличение суточной дозы ИГКС, однако повторного назначения СГКС для базисной терапии БА не было ни у одного больного. Следует отметить, что, хотя отмена анти-IgE терапии вызвала ухудшение клинической симптоматики, показателей функциональных тестов и КЖ пациентов, показатели, полученные через 1,5 года после отмены препарата, были значимо лучше, чем исходные показатели той же группы больных до назначения анти-IgE терапии в 1998 г. Среднее значение общего сывороточного IgE в исследуемой группе больных составило 113,22±43,68 МЕ/мл.
На фоне возобновления лечения у больных отмечалась положительная динамика изучаемых клинико-функциональных показателей: статистически значимо уменьшилось количество дневных и ночных симптомов, снизилась частота обострений (р=0,005), больные не госпитализировались в течение всего периода наблюдения. Отмечено статистически значимое снижение частоты ингаляций β2-агонистов короткого действия (р=0,007) и средней суточной дозы ИГКС (р=0,043), больным не требовалось лечение СГКС (таблица 4).
Таблица 4. Клинико-функциональные показатели через 1,5 года после прерывания лечения моноклональными анти-IgE АТ и их динамика во время возобновления анти-IgE терапии (II этап исследования)
| Показатели | Периоды наблюдения | ||
| Исходные показатели (2007г) | 16 недель | 32 недели | |
| Частота дневных симптомов в неделю | 2,07±0,49; 2 (2-2) | 1,15±0,37; 1(1-1) *(р<0,05) | 0,92±0,64; 1(1-1) |
| Частота ночных симптомов в неделю | 0,53±0,51; 2 (1-3) | 0; 0 *(р<0,05) | 0,07±0,27; 0 |
| Частота ингаляций β2-агонистов короткого в сутки | 2,23±0,72; 2(2-2) | 1,38±0,5; 1(1-2) *(р=0,007) | 1,15±0,8; 1(1-2) |
| ОФВ1, % от должного | 63,6±20,04; 63,8(48,5-75,1) | 65,6±23,6 60,9(47,9-85,1) | 68,1±23,9; 71,6(47,2-85,8) |
| Частота внеплановых визитов к врачу в год | 1,77±1,09; 2(1-2) | - | 0,46±0,66; 0(0;1) *(р=0,002) |
| Частота обострений БА в год | 2,3±1,31; 2(1-3) | - | 0,53±0,77; 0(0;1) *(р=0,005) |
| Частота госпитализаций в год | 0,07±0,27; 0 | - | 0 *(р<0,001) |
| Суточная доза ИГКС, мкг | 1038,5±477; 1000(1000-1000) | 826,9±449,3; 1000(500-1000) | 653,8±462,5;500(500-500) **(р=0,043) |
* - статистически значимые различия по сравнению с исходными данными;
** - статистически значимые различия по сравнению с результатами, полученными через 16 недель терапии.
Статистически значимого улучшения показателя ОФВ1 на фоне возобновления лечения отмечено не было. Однако у некоторых больных наблюдалась тенденция к увеличению показателей ФВД. Снижения показателя ОФВ1 у длительно болеющих больных тяжелой неконтролируемой атопической БА не было выявлено.
Уровни контроля согласно критериям, рекомендованным GINA 2006 г., в изучаемой группе больных после 1,5 лет перерыва в анти-IgE терапии были распределены следующим образом: частично контролируемое течение БА отмечено у 12 больных (92,3%), полностью контролируемое течение БА – у 1 больного (7,69%). Через 16 недель лечения полный контроль над симптомами БА был достигнут у 6 больных (46,15%), частично контролируемым течение заболевания было у 7 больных (53,84%). К 32 неделе контролируемое течение БА отмечено у 8 больных (61,5%), частично контролируемое - у 5 больных (38,46%).
Среднее значение результатов теста АСТтм в изучаемой группе больных составило 18,38±2,8; 19(13-22) баллов на момент возобновления лечения. На фоне лечения отмечено статистически значимое улучшение результатов проводимого теста по контролю над астмой (21,7±2,1; 21(20-22) (р=0,001) на 16 неделе и 21,8±1,52; 22(21-23) (р=0,017) на 32 неделе терапии).
На момент начала II этапа исследования в изучаемой группе больных среднее значение баллов опросника AQLQ составляло: симптомы – 3,97±0,89; 3,8(3,4-4,5) балла, ограничение активности - 4,58±0,84; 4,4(3,9-5,3) балла, эмоциональная сфера - 4,06±1,2; 4,2(3,5-5,0) балла, влияние окружающей среды - 4,14±1,2; 4(3,4-4,7) балла, общее КЖ - 4,08±0,8; 3,9(3,4-4,6) балла. При оценке динамики КЖ больных на фоне анти-IgE терапии на 32 неделе лечения нами было получено статистически значимое его улучшение по критериям общего КЖ, симптоматики заболевания, активности и эмоциональной сферы. Статистически значимых изменений по критерию влияния окружающей среды получено не было. Однако отмечена тенденция к увеличению этого показателя (таблица 5).
Таблица 5. Динамика критериев КЖ у больных, получавших терапию моноклональными анти-IgE АТ на II этапе исследования
| Критерии КЖ | Периоды наблюдения | ||
| Исходно (2007г) | 16 недель | 32 недели | |
| Общее КЖ, баллы | 4,08±0,8; 3,9(3,4-4,6) | 4,71±0,94; 4,68(3,9-5,4) *(р=0,002) | 5,09±0,83; 4,8(4,4-5,8) **(р=0,0014) |
| Симптомы, баллы | 3,97±0,89; 3,8(3,4-4,5) | 4,56±0,98; 4,75(3,8-5,25) *(р=0,036) | 5,03±0,9; 5(4,4-5,5) **(р=0,0028) |
| Ограничение активности, баллы | 4,58±0,84; 4,4(3,9-5,3) | 4,82±1,05; 4,5(4,3-5,7) | 5,2±0,97; 5,1(4,7-6,0) **(р=0,0029) |
| Эмоциональная сфера, баллы | 4,06±1,2; 4,2(3,5-5,0) | 5,0±1,07; 5,4(3,6-5,8) *(р=0,006) | 5,35±0,9; 5,4(5,0-6,2) **(р=0,049) |
| Влияние окружающей среды, баллы | 4,14±1,2; 4(3,4-4,7) | 4,45±1,2; 4,5(3,5-5,5) | 4,62±1,23; 4(3,5-5,75) |
* - статистически значимые различия по сравнению с исходными данными;
** - статистически значимые различия по сравнению с результатами, полученными через 16 недель терапии.
Проведенный II этап исследования показал высокую эффективность длительной терапии моноклональными анти-IgE АТ в достижении и поддержании долговременного контроля БА, а также ее положительное влияние на качество жизни больных. Полученный клинический опыт многолетнего наблюдения за больными, получающими анти-IgE терапию, свидетельствует о безопасности этого метода лечения, т.к. на протяжении всего периода наблюдения не было отмечено ни одного побочного явления, потребовавшего отмены терапии. У всех больных была хорошая переносимость препарата.
После 1,5 лет перерыва в лечении моноклональными анти-IgE АТ было отмечено статистически значимое ухудшение клинико-функциональных показателей и КЖ больных. Актуальным представлялся изучения длительности сохраняющейся эффективности анти-IgE терапии после ее отмены и разработки схемы ее дискретного применения.
III этап. Сравнительное проспективное исследование эффективности и безопасности терапии моноклональными анти-IgE антителами и разработка дискретной схемы их применения
На III этапе исследования в первой группе больных исходно показатель общего сывороточного IgE составил 215,98±127,3 МЕ/мл, в группе сравнения - 253,08±141,7 МЕ/мл. Статистических различий между группами выявлено не было (таблица 6). У всех больных I и II групп отмечалось неконтролируемое течение заболевания. После начала терапии на 16 неделе лечения моноклональными анти-IgE АТ нами отмечено статистически значимое снижение количества дневных симптомов в неделю, что составляло 3,26±2,41; 2(2-7) (р<0,001). В этой же группе больных отмечено снижение количества ночных симптомов до 0,21±0,42 в неделю (р<0,001) на 16 неделе лечения. В группе сравнения на 32 неделе наблюдения отмечалось снижение количества дневных симптомов до 5,73±1,76; 7(5-7) в неделю (р=0,034), однако этот показатель был значимо выше по сравнению с группой больных, получавших моноклональные анти-IgE АТ.
Также статистически значимым у больных, получавших моноклональные анти-IgE АТ, было снижение потребности в ингаляциях ß2-агонистов – до 2,56±2,08; 2(1-2) в сутки на 16 неделе (р<0,001) и до 1,33±1,96; 0,5(0-2) в сутки (р=0,01) на 32 неделе лечения. В группе сравнения статистически значимых изменений выявлено не было (рис. 3).
