Методические указания к выполнению курсовой работы по курсу «Анализ и улучшение качества природных вод» для студентов IV курса, обучающихся по направлению 280400 «Природообустройство» Составители
| Вид материала | Методические указания |
| В разделе введение следует ПДКр () – для морских водоёмов; К |
- Методические указания к выполнению курсовой работы по курсу «Основы климатологии, 417.3kb.
- Методические указания по выполнению курсовой работы по курсу «Математические методы, 220.31kb.
- Методические указания по выполнению курсовой работы для студентов фф зфо, обучающихся, 175.52kb.
- Методические указания к выполнению курсовой работы по дисциплине «Оценка качества продовольственного, 856.1kb.
- Методические указания по выполнению курсовой работы Ижевск, 289.74kb.
- Методические указания к выполнению курсовой работы по дисциплине «Теория финансов», 279.99kb.
- Методические указания по выполнению курсовой работы для студентов 2 курса всех специальностей, 1477.96kb.
- Методические рекомендации к выполнению курсовой работы по основам менеджмента для студентов, 236.14kb.
- Методические указания к выполнению курсовых работ по дисциплине «финансы и кредит», 489.86kb.
- Методические указания к выполнению курсовой работы по дисциплине «Основы научных исследований», 403.99kb.
Характеристика места отбора пробы природной воды, дата отбора. Использование (назначение) природной воды.
В разделе введение следует:
- раскрыть актуальность вопросов темы;
- охарактеризовать проблему, к которой относится тема, изложить историю вопроса, дать оценку современного состояния теории и практики, привести характеристику отрасли (подотрасли) промышленности, предприятия;
- изложить задачи в области разработки проблемы, т.е. сформулировать задачи темы работы;
- перечислить методы и средства, с помощью которых будут решаться поставленные задачи;
- кратко изложить ожидаемые результаты, в том числе технико-экономическую эффективность.
§ 2. Теоретическая часть по методам анализа природной воды
Краткая характеристика использованных методов анализа воды, приборы [1].
§ 3. Экспериментальная часть по анализу природной воды
3.1. Выполнить анализ воды и рассчитать содержание в ней компонентов (СО2, своб., СО32-, НСО3-, О.Ж., Ca, Mg, Fe, NO2-, NH4+, Cl-, SO42-, Na, K или (Na + K), а так же pH, электропроводность (χ), минерализацию (М), мутность, цветность, прозрачность, запах воды по методическим указаниям [1].
3.2. К результатам анализа приписать погрешности анализа, рассчитанные по ГОСТ 24902-81 (табл. 2) [2] и по паспорту ПНИЛ гидрогеохимии УНПЦ «Вода» ИГНД ТПУ.
3.3. Доказать достоверность результатов анализа, оценив общую фактическую погрешность (Пфакт) результатов анализа по указаниям Научного Совета по Аналитическим Методам (НСАМ), секция гидрогеохимическая, используя формулу, и сравнив её с величиной допустимой погрешности (Пдопуст), % (табл. 3) [3]:
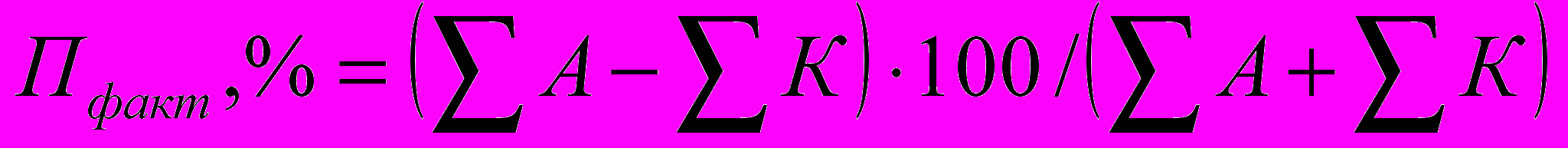 , где (1)
, где (1)А – сумма анионов воды в мг-экв/л, К – сумма катионов воды в мг-экв/л.
Таблица 2 – Допустимая погрешность анализа природных вод полевыми методами
| Компонент, размерность | Диапазон концентраций | Допустимая погрешность, % |
| pH, ед рН | | ± 0,2 |
| НСО3-, мг/л | до 180 > 180 | 30 10 |
| СО3 2-, мг/л | до 180 > 180 | 30 10 |
| Cl-, мг/л | до 150 > 150 | 30 10 |
| SO42-, мг/л | До 50 > 50 | >30 30 |
| NO3-, мг/л | До 10 > 10 | 30 20 |
| О.Ж., мг-экв/л | до 3 > 3 | 30 10 |
| Сa2+, мг/л | до 120 > 120 | 30 10 |
| Mg2+, мг/л | До 80 > 80 | 30 10 |
| Na+, мг/л | До 50 > 50 | >30 30 |
| Feобщ. , мг/л | до 0,2 > 0,2 | 30 20 |
| F-, мг/л | до 0,3 > 0,3 | 30 20 |
| NH4+, мг/л | до 0,5 > 0,5 | 30 20 |
| Сухой остаток, мг/л | до 50 > 50 | >30 30 |
Таблица 3 – Величины допустимой погрешности анализа воды
при различном содержании анионов в ней
| А, мг-экв/л | Более 15 | 15–5,0 | 4,9–3,0 | 2,0–2,0 | Менее 2 |
| П допуст, % | 2 | 3 | 7 | 10 | Не реглам |
3.4. Если Пфакт Пдопуст, переделать анализ воды.
3.5. Если Пфакт < Пдопуст, результаты анализа представить в виде табл. 4.
Таблица 4 – Результаты анализа воды в сравнении с нормативами вод питьевого назначения (ПДКпит), вод для рыборазведения (ПДКр) и кларковыми содержаниями компонентов в водах зоны гипергенеза (К г.г), в речных водах (К р.в.), в морских водах (Км.в.) [4, 5, 10]
| № п/п | Компонент, разменость | Сi | ПДКпит | ПДКр | К г.г | К р.в. | Км.в. | |||||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | |||||||
| 1 | рН, ед. рН | | 6–9 | 6,5–8,5 | 6,9 | – | 8,2 | |||||||
| 2 | НСО3 -,мг/л | | – | – | 187 | 58,4*;52** | 488 | |||||||
| 3 | СО2(св) , мг/л | | – | – | 26,6 | – | – | |||||||
| 4 | SO42-, мг/л | | 500 | 100; (3500**) | 76,7 | 11,2*; 8,25** | 2712 | |||||||
| 5 | Cl- , мг/л | | 350 | 300; (11900**) | 59,7 | 7,8*; 5,75** | 19400 | |||||||
| 6 | О.Ж., ммоль–э/л | | 7 | – | – | – | – | |||||||
| 7 | Са2+, мг/л | | – | 180; (610**) | 39,2 | 15*;13,4** | 411 | |||||||
| 8 | Mg 2+, мг/л | | – | 40; (940**) | 18,2 | 4,1*;3,35** | 1290 | |||||||
| 9 | П.ок.,мгO/л | | 5 | – | – | – | – | |||||||
| 10 | NО3-, мг/л | | 45 | 40 | 2,40 | 1*; 0,44** | – | |||||||
| 11 | NO2-, мг/л | | 3 | 0,08 | 0,19 | 0,03** | – | |||||||
| 12 | NН4+, мг/л | | 2 по N | 0,5; (2,9**) | 0,59 | 0,02** | – | |||||||
| 13 | РО43- по Р, мг/л | | 3,5 | 2 реки 0,05 олиг. в; 0,15 оз. м. 0,2 болота э. | – | – | – | |||||||
| 14 | Pэл., мкг/л | | 0,1 | – | 58 | 20*; 10** | 88 | |||||||
| 15 | В-ионы, мг/л | | | 0,5; (10**) | | | | |||||||
| 16 | В сумм., мкг/л | | 50 | | 77,9 | 10* | 4450 | |||||||
| 17 | SiО2, мг/л | | 10 по Si | – | 17,9 | 13,1*; 10,4** | 6,2 | |||||||
| 18 | Fe общ, мкг/л | | 300 | 100; (50**) | 481 | 670*; 40** | 3,4 | |||||||
| 19 | I –ионы, мкг/л | | – | 80; (200**) в доп. к ест. Cодерж. | 8,02 | 7* | 64 | |||||||
| | | | | | | | | |||||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | |||||||
| 20 | Br –ионы, мкг/л | | 200 | 1350; (12000**) в доп. к ест. содержанию | 85,2 | 20* | 67300 | |||||||
| 21 | F-, мг/л | | 1,5 (I-II); 1,2 (III) | 0,05 в доп. к ест. одерж., но не выше 0,75 | 0,48 | 0,1* 0,1** | 1,3 | |||||||
| 22 | Li, мкг/л | | 30 | 0,7 | 13 | 3* | 170 | |||||||
| 23 | Na, мг/л | | 200 | 120; (7100**) | 67,6 | 6,3*;5,15** | 10800 | |||||||
| 24 | К, мг/л | | - | 50;10 при М=100 мг/л; (390**) | 5,15 | 2,3*;1,3** | 392 | |||||||
| 25 | Rb, мкг/л | | 100 | 100 | 1,86 | 1* | 120 | |||||||
| 26 | Sr, мкг/л | | 7000 | Исследов-я, (10∙103**) | 183 | 50*; 60** | 8100 | |||||||
| 27 | Al, мкг/л | | 500 | 40 | 226 | 400*; 50** | 1,0 | |||||||
| 28 | Hg, мкг/л | | 0,5 | отсутствие (0,01) | 0,041 | 0,07* | 0,15 | |||||||
| 29 | Zn, мкг/л | | 5000 | 10; (50**) | 41,4 | 20* | 5,0 | |||||||
| 30 | Cd, мкг/л | | 1 | 5; (10**) | 0,24 | - | 0,11 | |||||||
| 31 | Pb, мкг/л | | 30 | 100; (10**) | 2,97 | 3* | 0,03 | |||||||
| 32 | Cu, мкг/л | | 1000 | 1; (5**) | 5,58 | 7* | 0,9 | |||||||
| 33 | As, мкг/л | | 50 | 50 (10**) | 1,46 | 2* | 2,6 | |||||||
| 34 | Bi, мкг/л | | 100 | - | - | - | - | |||||||
| 35 | Ag, мкг/л | | 50 | - | 0,26 | 0,3* | 0,28 | |||||||
| 36 | Ni, мкг/л | | 100 | 10 | 3,58 | 0,3* | 6,6 | |||||||
| 37 | Со, мкг/л | | 100 | 10; (5**) | 0,39 | 0,2* | 0,39 | |||||||
| 38 | Ti, мкг/л | | - | - | 17,4 | 3*; 10** | 1,0 | |||||||
| 39 | Cr общ., мкг/л | | | | 3,03 | 1* | 0,2 | |||||||
| 40 | Cr (6), мкг/л | | 50 | 20 | - | - | - | |||||||
| 41 | Cr(3), мкг/л | | 500 | 70 | - | - | - | |||||||
| 42 | V, мкг/л | | 100 | 1 | 1,34 | 0,9* | 1,9 | |||||||
| 43 | Sn, мкг/л | | - | - | 3,9 | 0,5* | 0,81 | |||||||
| 44 | Мо, мкг/л | | 250 | 1,2 | 1,75 | 1* | 10 | |||||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | |||||||
| 45 | Ве, мкг/л | | 0,2 | 0,3 | 0,19 | - | 6∙10-4 | |||||||
| 46 | Ва, мкг/л | | 100 | 740; (2∙103**) | 18,3 | 10* | 21 | |||||||
| 47 | Zr, мкг/л | | - | 70 | 1,2 | - | 2,6∙10-2 | |||||||
| 48 | Мn, мкг/л | | 100 | 10; (50**) | 54,5 | 8,2 | 0,4 | |||||||
| 49 | W, мкг/л | | 50 | 0,8 | - | - | - | |||||||
| 50 | Sb, мкг/л | | 50 | - | 0,68 | 1* | 0,33 | |||||||
| 51 | Au, мкг/л | | - | - | 5,3·10-3 | 2·10-3 * | 11·10-3 | |||||||
| 52 | Se, мкг/л | | 10 | 1,6 | 0,72 | 0,2* | 0,09 | |||||||
| 53 | Sc, мкг/л | | - | - | 0,07 | 0,004* | <0,004 | |||||||
| 54 | Cs, мкг/л | | - | 1000 | 0,26 | 0,02* | 0,3 | |||||||
| 55 | Lа, мкг/л | | - | - | 0,67 | 0,2* | 0,0034 | |||||||
| 56 | Sm,мкг/л | | 24 | - | - | - | - | |||||||
| 57 | Th, мкг/л | | - | - | 0,24 | 0,1* | 4∙10-4 | |||||||
| 58 | U, мкг/л | | - | - | 1,31 | 0,04* | 3,3 | |||||||
| 59 | Tl, мкг/л | | 0,1 | - | - | - | - | |||||||
| 60 | Те, мкг/л | | 10 | 2,8 | - | - | - | |||||||
| 61 | Nb, мкг/л | | 10 | - | 0,45 | - | 0,015 | |||||||
| 62 | Ga, мкг/л | | | | 0,37 | 0,09* | 0,03 | |||||||
| 63 | с.о., мг/л | | 1000 | - | - | - | - | |||||||
| 64 | S2-, м/л | | 0,003 | 0,005; 0,0005 для олиготроф. водоёмов | - | - | - | |||||||
| 65 | Фенол, мг/л | | 0,25 | 0,001 | - | - | - | |||||||
| 66 | Нефтепро-дукты, мг/л | | 0,1 | 0,05; (0,05**) | - | - | - | |||||||
| 67 | С6Н6, мг/л | | | 0,5 | | | | |||||||
Примечания: ПДКр (**) – для морских водоёмов; К р.в.* – по данным Livingston (1963), Turekian (1969); К р.в. ** – по данным Martin (1979), Meybeck (1982)
3.6. Используя величины эквивалентов компонентов (Э) (табл. 6), рассчитать содержание компонентов в природной воде в мг-экв/л по формуле

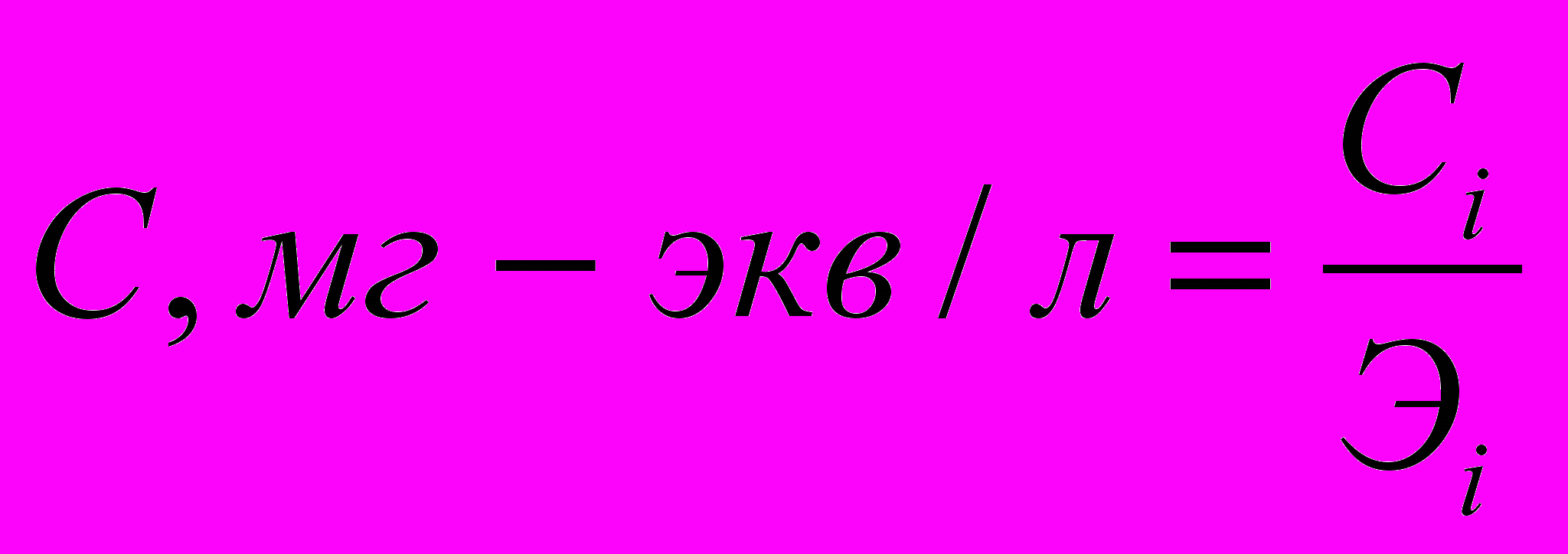 (2)
(2)заполнить колонки 1, 2, 3 табл. 6.
Таблица 5 – Величины эквивалентов компонентов вод
| Компонент | HCO3- | CO32- | Cl- | SO42- | NO3- | Ca2+ | Mg2+ | Na+ | K+ | Fe3+ |
| Э, мг | 61 | 60 *) | 35,5 | 48 | 62 | 20 | 12,2 | 23 | 39 | 18,6 |
*) в реакции перевода СО32- в НСО3-.
Таблица 6– Результаты анализа воды в мг-экв/л, в % -экв/л
| Компонент | Сi , мг/л | Сi , мг-экв/л | Сi , %-экв/л |
| 1 | 2 | 3 | 4 |
| | | | |
3.7. Рассчитать содержание компонентов в природной воде в %-экв/л, используя пропорции, например, для расчета содержания [НСО3-], %-экв/л
ΣА, мг-экв/л – 100 %-экв/л
[НСО3-], мг-экв/л – [НСО3-], %-экв/л
[НСО3-], %-экв/л = [НСО3-]∙100 / ΣА (3)
Например, для расчета [Са2+], %-экв/л
ΣК, мг-экв/л – 100 %-экв/л
[Са2+], мг-экв/л – [Са2+], %-экв/л
[Са2+], %-экв/л = [Са2+]∙100 / ΣК (4)
3.8. Заполнить колонку 4 табл. 6.
3.9. Описать исследуемую природную воду формулой Курлова и словами.
