Синтез, свойства, биологическая активность n-гетериламидов α-оксокислот и продуктов их химических превращений 15. 00. 02 фармацевтическая химия, фармакогнозия
| Вид материала | Автореферат диссертации |
Содержание6.4 Влияние соединений на свертывающую систему крови. 6.5 Противомикробная активность (ПМА). Основное содержание диссертации представлено в работах |
- Синтез соединений на основе химических превращений производных α- оксокарбоновых кислот, 643.93kb.
- Синтез, свойства и биологическая активность енаминоамидов ацилпировиноградных кислот, 439.81kb.
- Синтез, свойства и биологическая активность продуктов взаимодействия 1,2,4-триазолов, 669.98kb.
- Синтез, химические свойства и биологическая активность 1,4-дизамещенных 5-арил-3-гидрокси-3-пирролин-2-онов, 667.95kb.
- Синтез и биологическая активность карбо- и гетероциклов на основе тетрацианоэтилена, 673.64kb.
- Синтез, свойства и биологическая активность производных 2-хлорникотинонитрилов, 264.36kb.
- Синтез и свойства новых производных 2 (1,2,4 триазолил 5 тио)уксусных кислот 15. 00., 240.9kb.
- Примерная программа рекомендуется для направления подготовки (специальности) 111801, 717.4kb.
- Программа курса «Аналитическая химия» специальность «Фармация», 92.69kb.
- Тематический план лекций по дисциплине «Фармацевтическая химия», 32.57kb.
6.4 Влияние соединений на свертывающую систему крови.
Исследования проводили с помощью коагулометра «Минилаб 701» с использованием цитратной (3.8 %) крови собаки (9:1). Соединения вводили в концентрации 1 мг/мл. В качестве эталона сравнения гемостатической активности использовали этамзилат в концентрации 1мг/мл, а в качестве эталона антикоагулянтной активности – раствор гепарина в концентрации 1 ЕД/мл крови
Показано, что только бутеноат 8а, не имеющий заместителей в ароильном радикале и в 5 положении 1,3,4-тиадиазолильного фрагмента, обладает слабой гемостатической активностью. Соединения 8г,ж оказывают слабое, а бутеноат 8з - выраженное антикоагулянтное действие. Соли 9б-д и феноляты натрия 14а-г показывают различное по характеру действие, но не превышающее препараты сравнения.
6.5 Противомикробная активность (ПМА).
ПМА по отношению к штаммам St. aureus АТСС 6538-Р и E. coli АТСС 25922 определяли методом двукратных серийных разведений в жидкой питательной среде. Для всех исследуемых соединений определяли минимальные ингибирующие концентрации (МИК) в мкг/мл. Препаратами сравнения служили этакридин и гидроксиметилхиноксилиндиоксид (диоксидин). Результаты испытаний наиболее активных соединений представлены в таблице 3.
При изучении ПМА N-гетериламидов АрПК 2 и о-ГФГК 6 установлено, что они оказывают слабое действие. МИК для соединений 2 составляет: 62-500 / 125-1000 мкг/мл, а для соединений 6: 500-1000 / 125-1000 мкг/мл.
При изучении биологической активности бутеноатов 8а-о нами установлено, что они обладают ПМА на уровне, чуть превышающем этакридин, но уступающем диоксидину по отношению к эталонным штаммам микроорганизмов. Таким образом, при переходе «гетериламид-ароилпируват» существенного увеличения антимикробной активности не происходит.
Химическая модификация N-гетериламидов АрПК 2 и о-ГФГК 6 до комплексных соединений 10-13 и 15,16 приводит к значительному увеличению ПМА. Установлено, что антимикробный эффект зависит, в первую очередь, от природы металла и характера гетероцикла. Так, среди медных хелатов 10 не выявлено веществ с высокой антимикробной активностью. Обнаружено, что соединения 11а, 12а,д,е, 13б,в, превышают по противомикробной активности этакридин по отношению к золотистому стафилококку в 16-2000 раз и к кишечной палочке – в 512-1000 раз. Отношение МИК (мкг/мл) к токсичности ЛД50 (мг/кг) у соединений 11а, 12а,д,е, 13б,в, составляет для стафилококка 0,0003-0,01 и для кишечной палочки 0,0025-0,008, в то время как у этакридина эти показатели значительно уступают.
При изучении металлорганических комплексов 15,16 установлено, что в данном ряду наибольшую активность проявили кадмивые хелаты 16б-г. При этом кадмиевые производные показывают активность, не зависящую от строения гетероцикла и значительно превышающие диоксидин.
Введение во второе положение исходных N-гетериламидов 2 дифенилметиленгидразинового и флуоренилметиленгидразинового фрагментов не привело к значительному увеличению ПМА. Так, при сравнении влияния гидразонового заместителя на данный вид активности наибольший эффект проявили флуоренилиденгидразинопроизводные 18, по сравнению с соединениями 17. Выявлено, что их активность находится на уровне этакридина.
Установлено, что при переходе от N-гетериламидов АрПК 2 к производным пиразол-5-карбоновых кислот 19 не происходит существенного увеличения ПМА и их активность соответствует действию этакридина, но не превышает эффект диоксидина.
Таблица 3
Данные по ПМА наиболее активных соединений
| Соединение | МИК, мкг/мл | Соединение | МИК, мкг/мл |
| St. aureus / Е.coli | St. aureus / Е.coli | ||
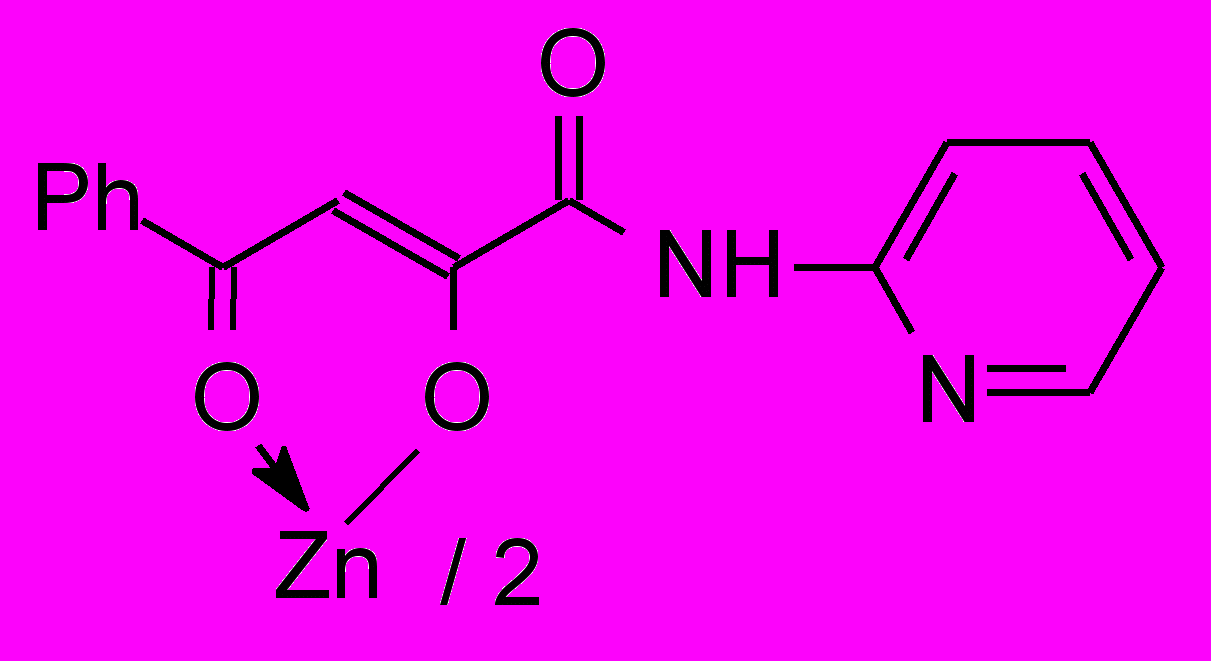 11а 11а3000 мг/кг | 31.0/3.9 | 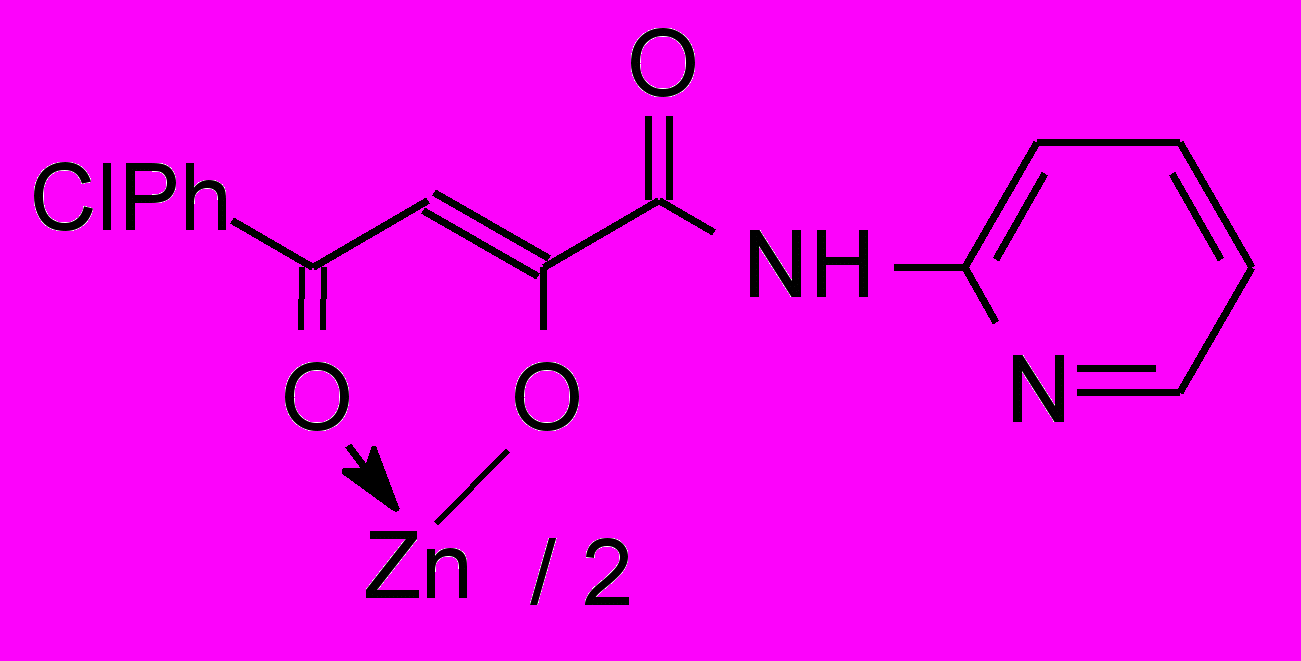 11б 11б | 31.0/62.0 |
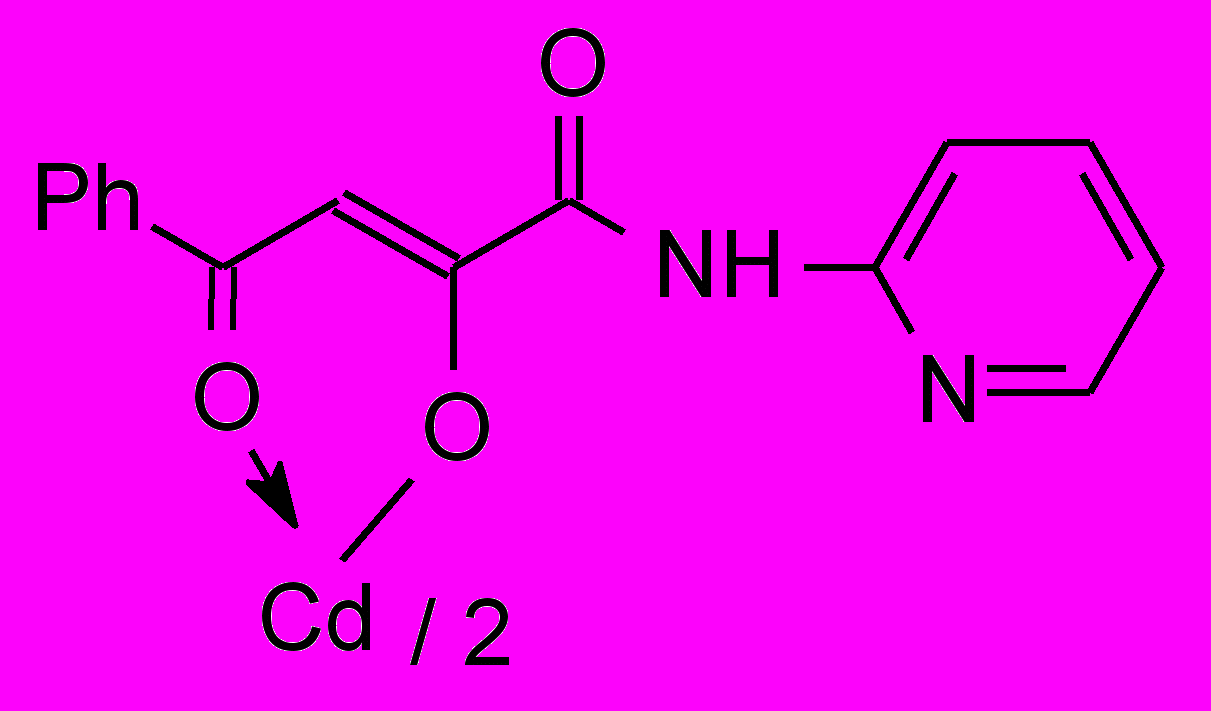 12а 12а1500 мг/кг | 2.0/2.0 | 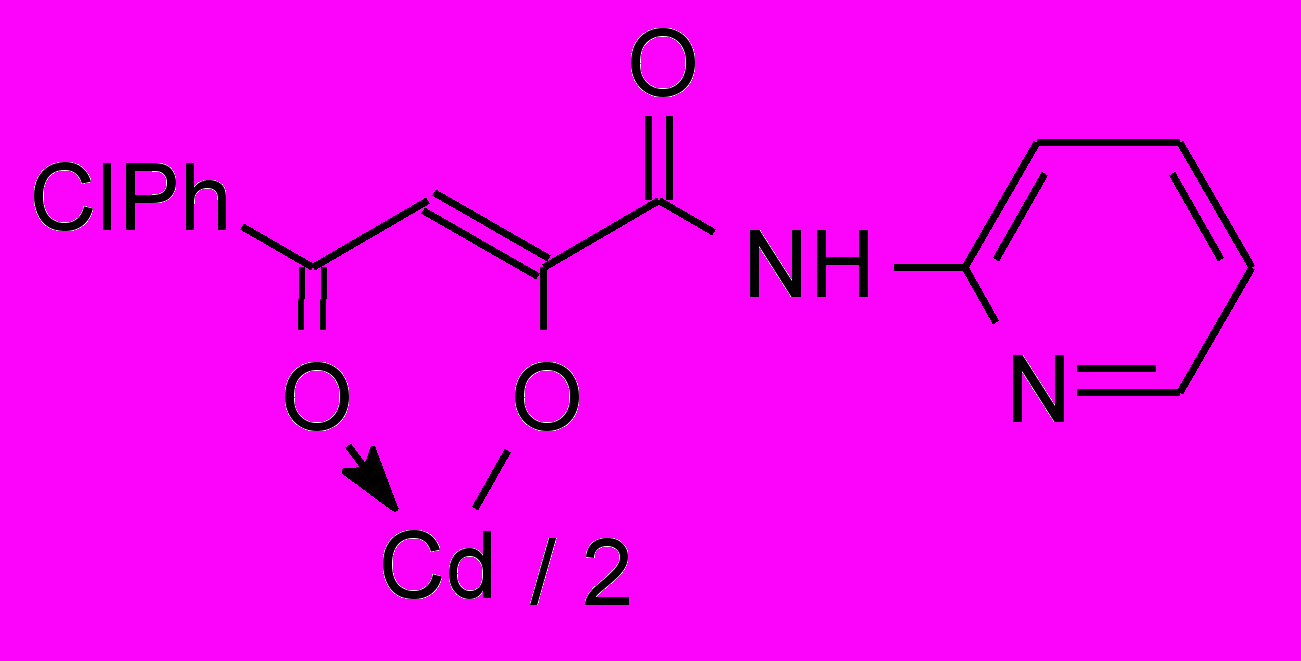 12б 12б | 250/31.0 |
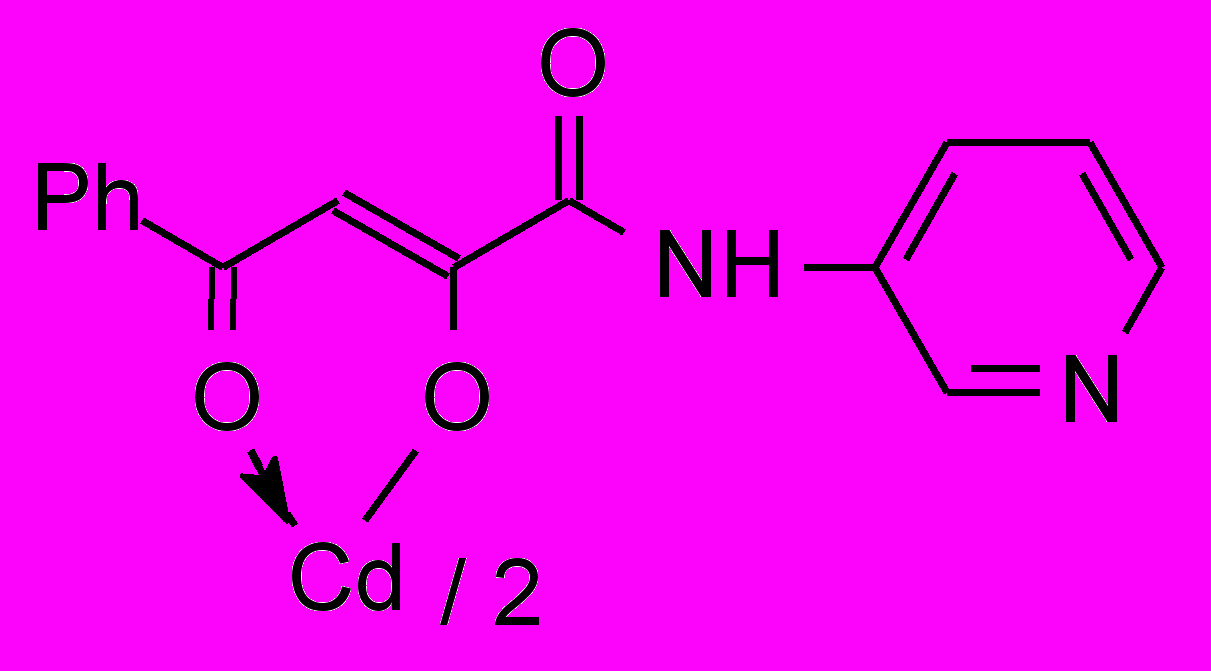 12в 12в | 15.6/62.0 | 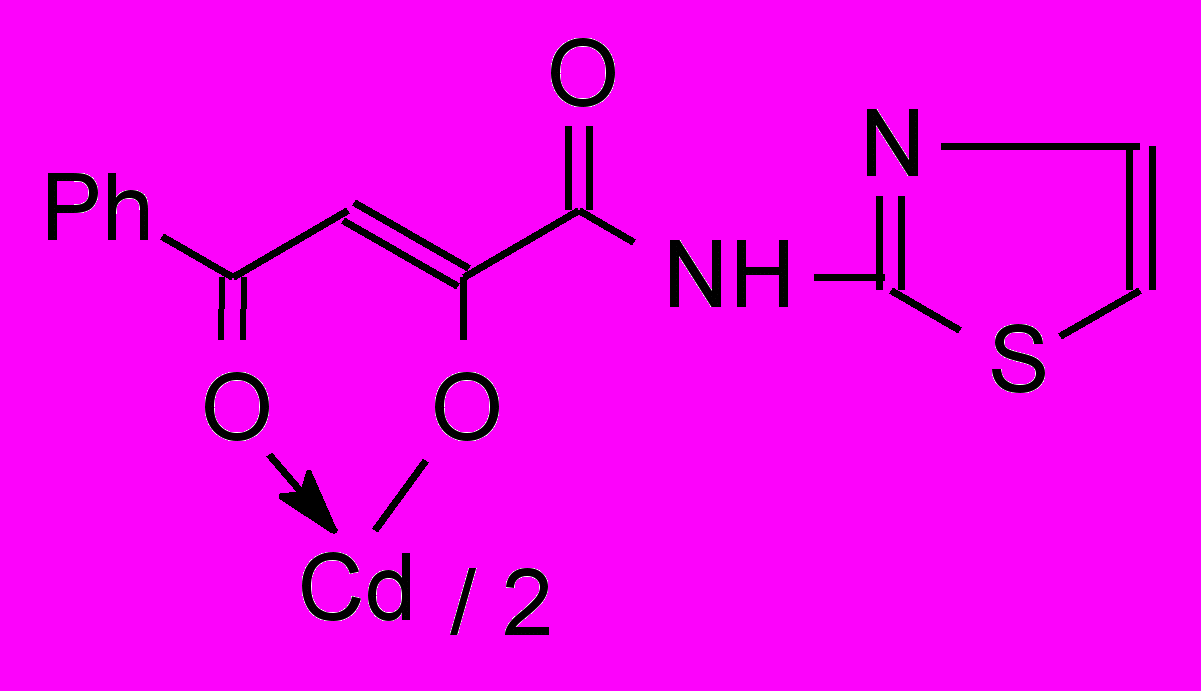 12д 12д500 мг/кг | 2.0/3.9 |
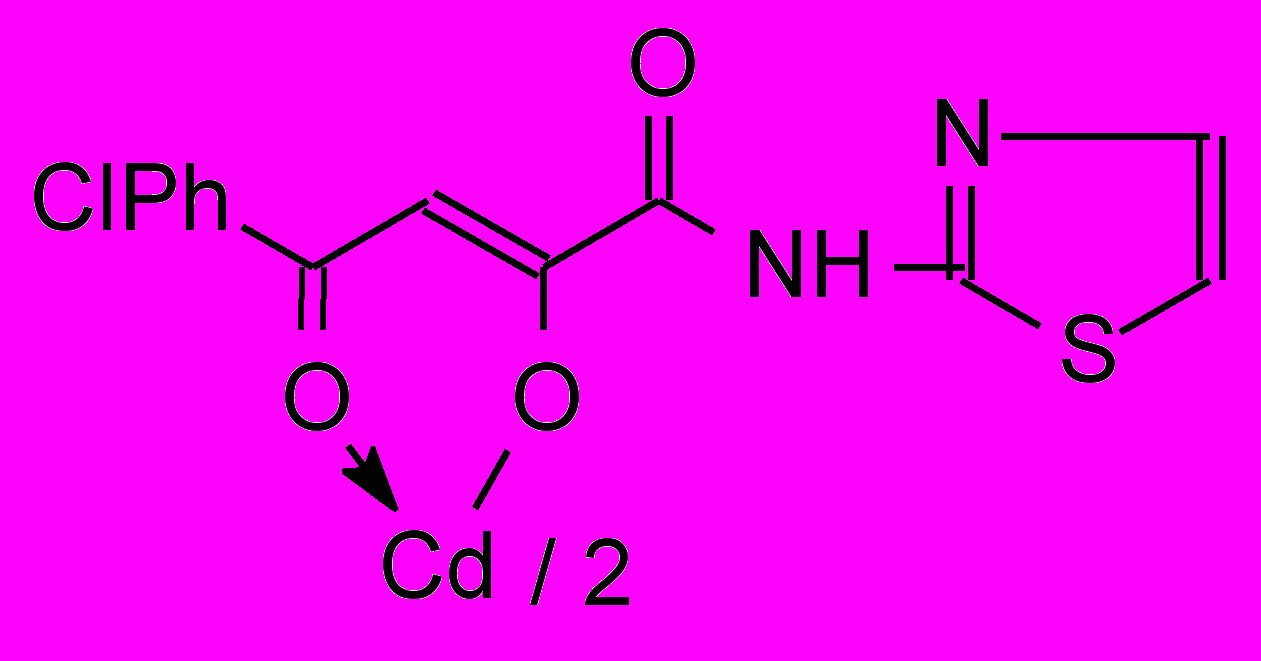 12е 12е | 1.0/1.0 | 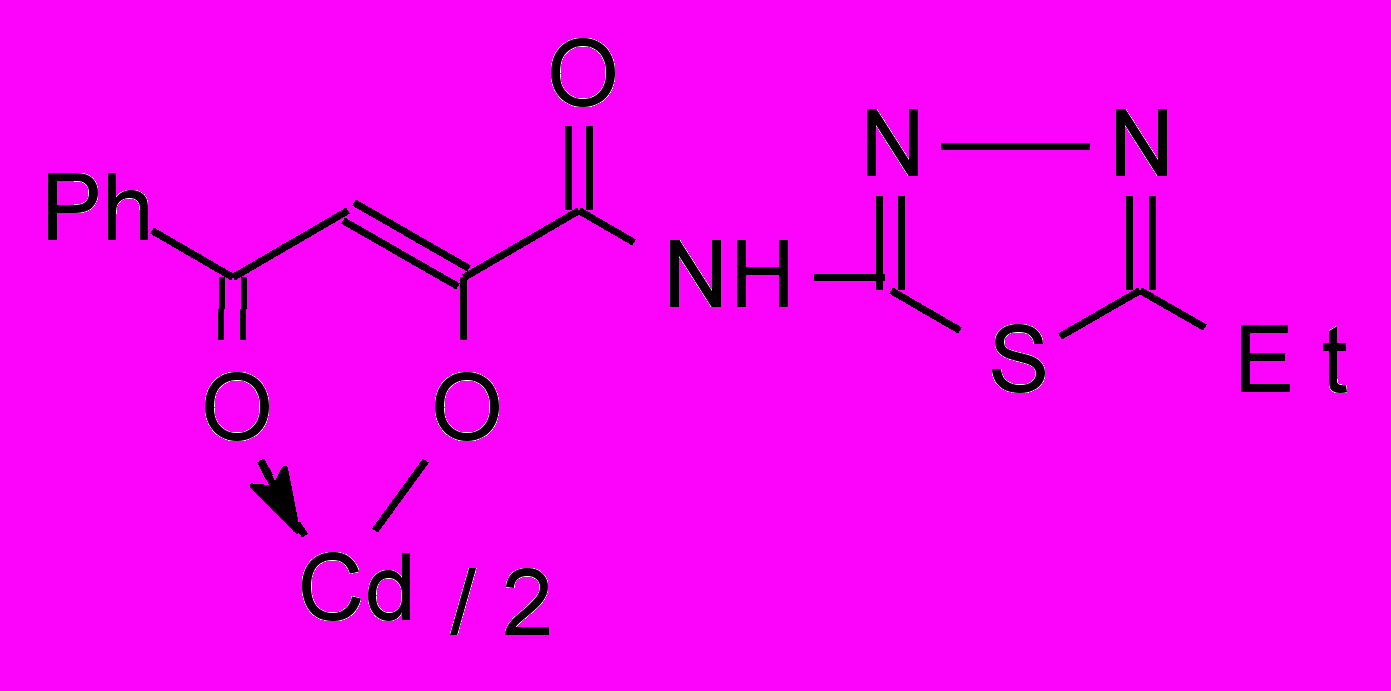 12з 12з | 250/62.0 |
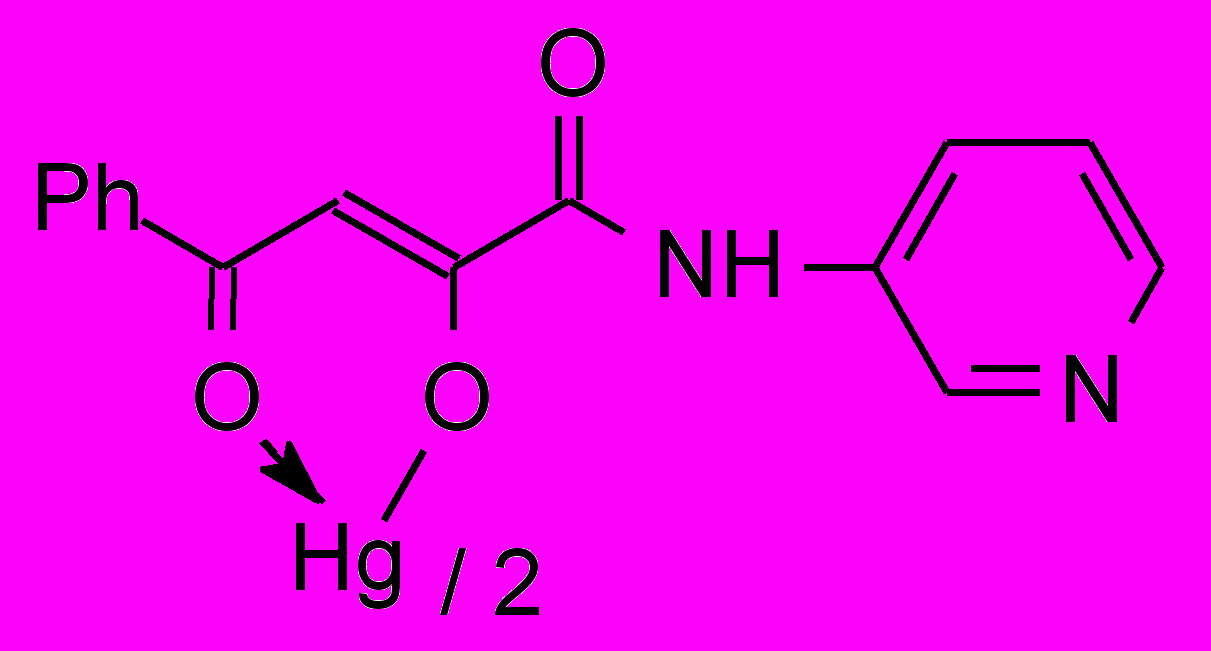 13б 13б800 мг/кг | 3.9/7.8 | 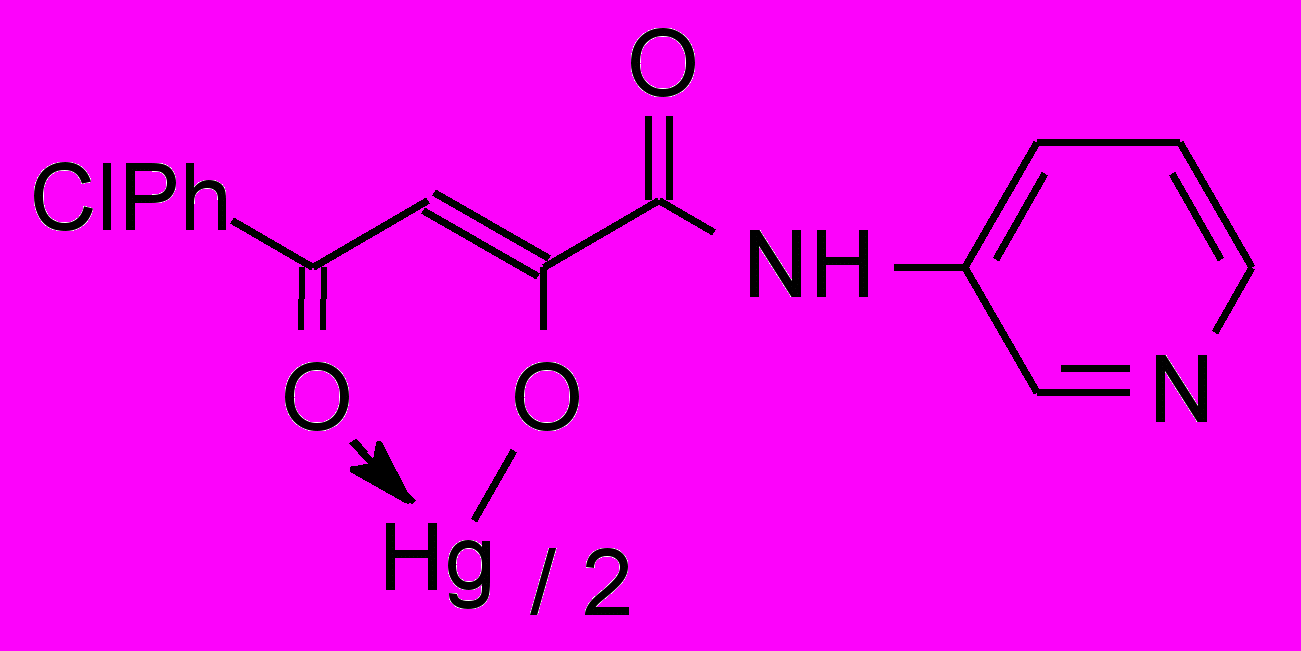 13в 13в800 мг/кг | 0.25/2.0 |
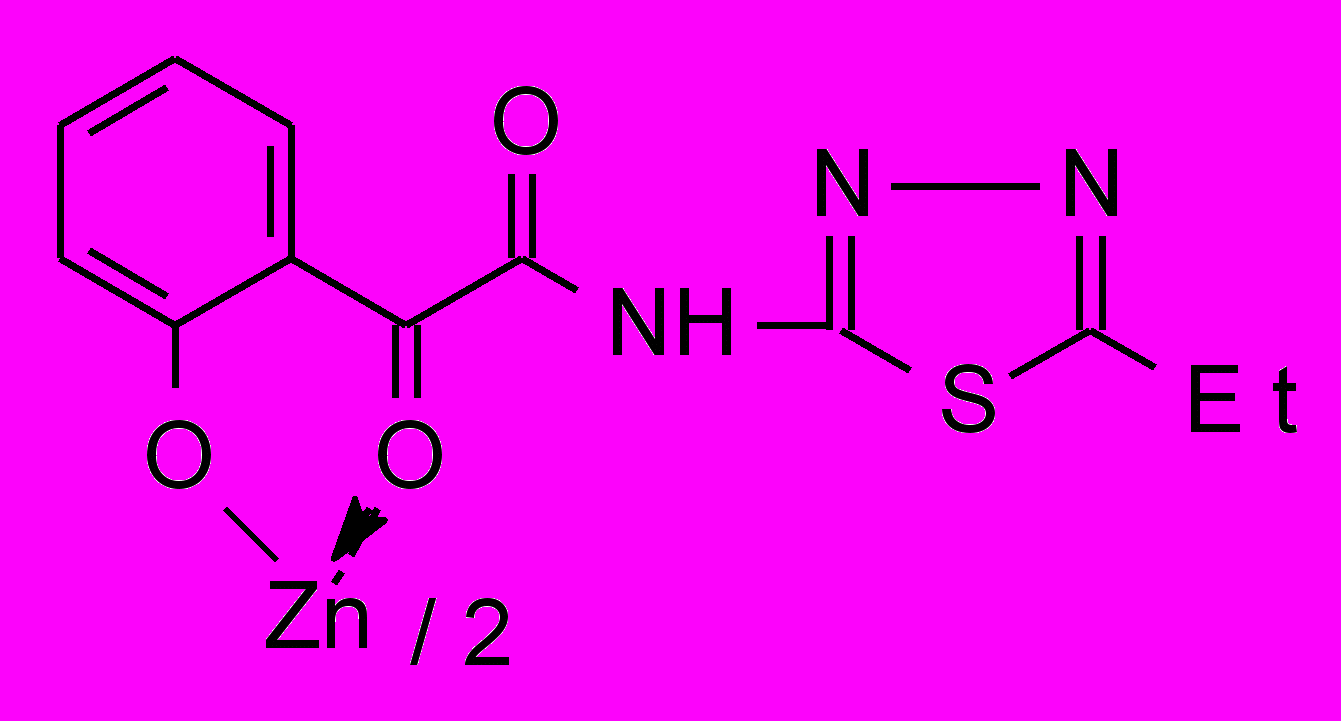 15 15 | 125/62.0 | 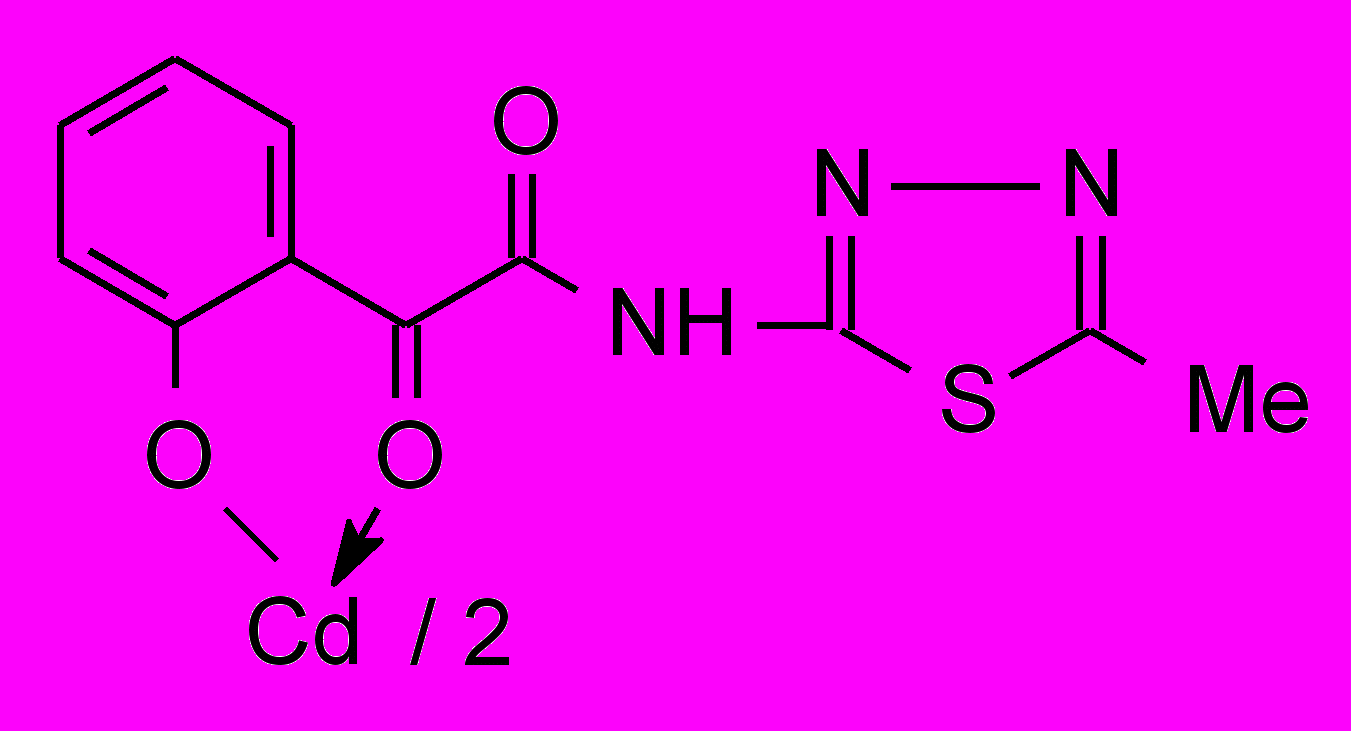 16б 16б | 2.0/3.9 |
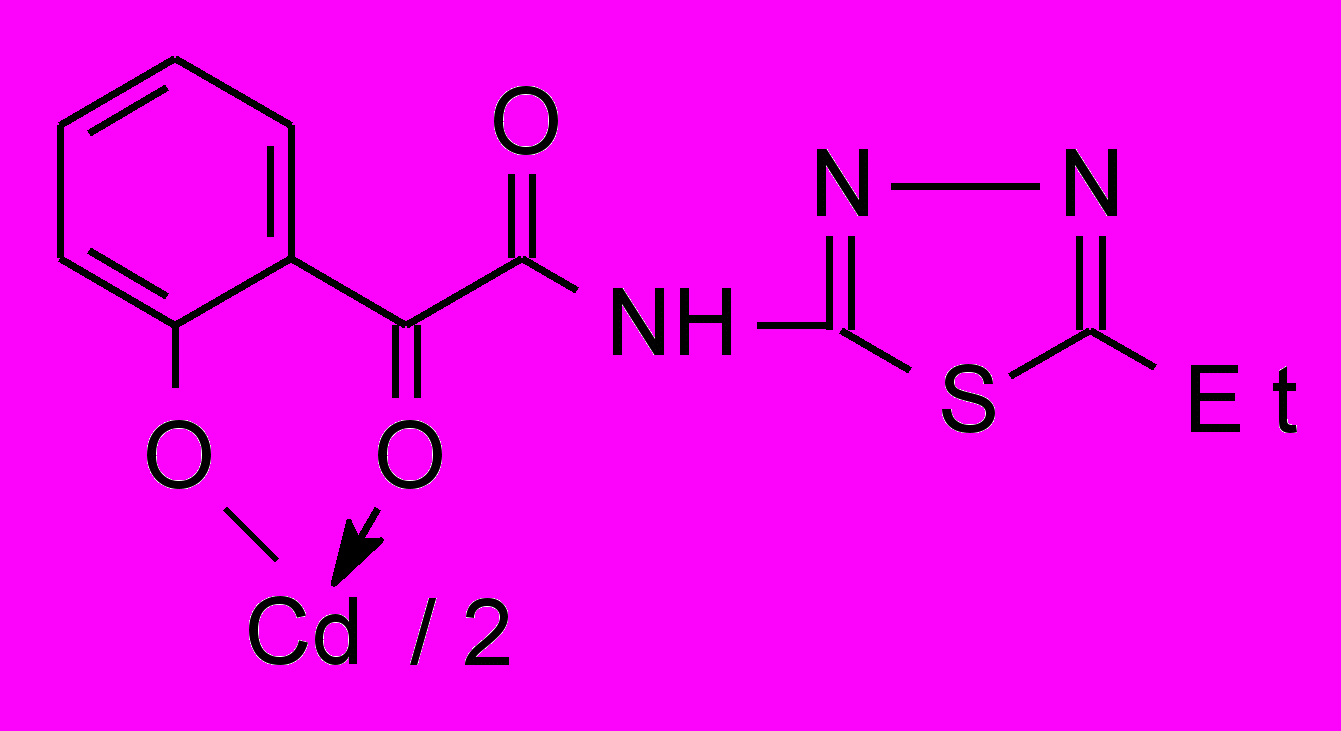 16в 16в | 2.0/3.9 | 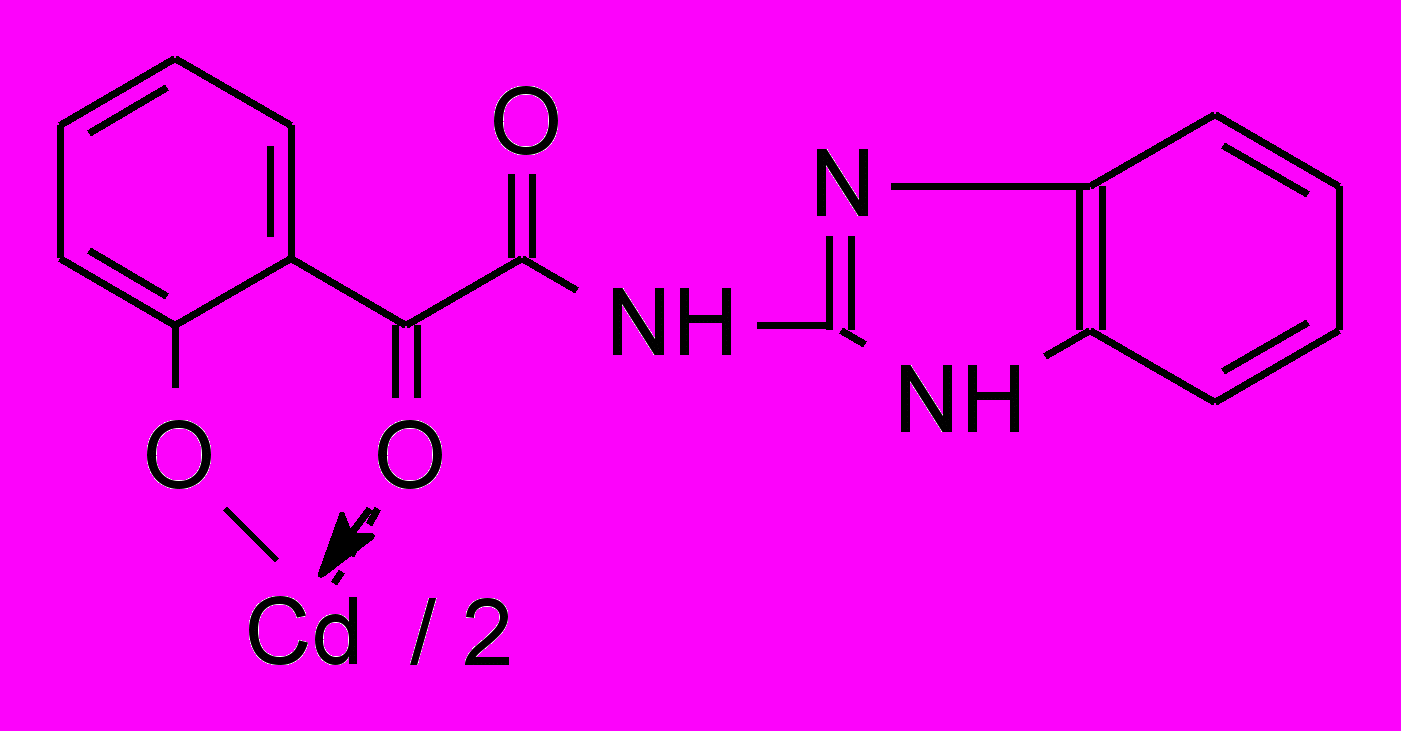 16г 16г | 2.0/3.9 |
| Этакридин | 500/2000 | Диоксидин | 62,5-1000/ 3,9-62,5 |
ВЫВОДЫ
- Реакцией дециклизации 5-арил-2,3-дигидрофуран-2,3-дионов и 2,3-дигидробензо[b]фуран-2,3-диона под действием N-гетериламинов получены N-гетериламиды α-оксокислот, имеющие в структуре потенциально биологически активные циклы 2-,3-,4-пиридина, 5-бром-2-пиридина, 2-тиазола, 5-R-1,3,4-тиадиазола и 2-бензимидазола.
- Впервые разработан способ синтеза комплексных соединений Cu2+, Zn2+, Cd2+, Hg2+ на основе N-гетериламидов 4-арил-2-гидрокси-4-оксо-2-бутеновых и 2-(2-гидроксифенил)-2-оксоэтановой кислот и установлено, что исходные реагенты координируются металлами как бидентатные О-О лиганды.
- Получены водорастворимые соединения на основе реакции α-оксокислот с гетероциклическими аминами, а также взаимодействием N-гетериламидов 2-(2-гидроксифенил)-2-оксоэтановой кислоты с натрия карбонатом.
- Изучено взаимодействие N-гетериламидов АрПК с гидразоном бензофенона и 9-флуоренона и установлено наличие таутомерного равновесия Z-КЕГ, Е-КЕГ и β-КГ форм в растворах полученных соединений, количественное содержание которых определяется природой растворителя, строением гетероциклического и гидразинного фрагментов.
- Установлено, что взаимодействие N-гетериламидов АрПК с этиловым эфиром гидразинэтановой кислоты приводит к образованию соответствующих производных 3-арил-2-этоксикарбонилметил-2,3-дигидропиразол-5-карбоновой кислоты. При этом выявлено, что в случае N-[2-(5-R-1,3,4-тиадиазолил)]амидов, целевые продукты существуют в растворах в виде двух таутомерных форм за счет миграции протона амидного фрагмента к атому азота гетероцикла.
- На основе разработанных или усовершенствованных методов синтеза получено 119 новых соединений, структура которых подтверждена данными спектров ЯМР1Н, ИК- и масс-спектроскопии, индивидуальность – данными ТСХ.
- Установлены некоторые закономерности биологической активности от химического строения соединений, которые могут быть использованы в дальнейшем поиске биологически активных веществ в ряду производных N-гетериламидов α-оксокислот.
- Выявлены наиболее перспективные соединения для дальнейших исследований:
- N-[2-(5-этил-1,3,4-тиадиазолил)]амид 2-(2-гидроксифенил)-2-оксоэтановой кислоты (6ж), обладающий противовоспалительной и анальгетической активностью
- бис{3-фенил-1-[N-(3-пиридил)карбоксамидо]-1,3-пропандионато} кадмий, ртуть (12в, 13б), обладающие противовоспалительной и противомикробной активностью.
- N-[2-(5-этил-1,3,4-тиадиазолил)]амид 2-(2-гидроксифенил)-2-оксоэтановой кислоты (6ж), обладающий противовоспалительной и анальгетической активностью
Основное содержание диссертации представлено в работах
- Синтез металлорганических соединений на основе производных ароилпировиноградных кислот и изучение их антимикробной активности / П.А. Мокин, Л.Н. Шелепенькина, Е.С. Еловикова [и др.] // Вопросы теоретической и практической медицины: Тез. докл. 70-й юбилейн. итог. Республ. науч. конф. молодых ученых.- Уфа, 2005.- С. 52-53.
- Синтез биологически активных соединений на основе взаимодействия о-гидроксифенилглиоксалевой кислоты с гетериламинами / Н.А. Пулина, П.А. Мокин, А.Е. Рубцов [и др.] // Фармация и здоровье: Мат. Междунар. науч.- практ. конф.- Пермь, 2005.- С.81-82.
- Синтез биологически активных производных пиразол-5-карбоновой кислоты на основе эфиров и амидов ароилпировиноградных кислот / Н.А. Пулина, В.В. Залесов, П.А. Мокин [и др.] // Здоровье и образование в XXI веке: Материалы VI междунар. науч.-практ. конф.- М: РУДН, 2005.- С. 415.
- Мокин, П.А. Изучение противоспалительной активности среди производных гетериламидов 4-арил-2-гидрокси-4-оксо-2-бутеновых кислот / П.А. Мокин, К.В. Яценко // Науки о человеке: Тез. докл. VII конгр. мол. ученых и специалистов.- Томск, 2006.- С. 14-143.
- Биологическая активность гетериламидов ароилпировиноградных кислот и их солей / В.В. Юшков, Н.А. Пулина, П.А. Мокин [и др.] // Новая технологическая платформа биомедицинских исследований (биология, здравоохранение, фармация): Материалы науч.- практ. конф.- Ростов-н/Д, 2006.- С.60-61.
- Пулина, Н.А. Биологически активные соединения на основе взаимодействия о-гидроксифенилглиоксалевой кислоты с гетериламинами / Н.А. Пулина, П.А. Мокин // Новая технологическая платформа биомедицинских исследований (биология, здравоохранение, фармация): Материалы научн.- практ. конф.- Ростов-н/Д, 2006.- С.39-40.
- Pulina, N.A. Synthesis, antiinflammatory and antibacterial activity of a series of novel metal-organic complexes / N.A. Pulina, Р.А. Мокin, К.V. Yасеnkо // 2-nd Russian-Chinese international scientific conferenсe оn pharmacologi: «Fundomental pharmacologi and pharmacy - сlinical practice».- Perm, 2006.- Р.134.
- Изучение синтеза и фармакологической активности, производных гетериламидов о-гидроксифенилглиоксалевой кислоты / Н.А. Пулина, П.А. Мокин, В.В. Залесов [и др.] // Здоровье образование в XXI веке: материалы VII междунар. науч.-практ. конф.- М: РУДН.- 2006.- С.408-409.
- Синтез биологически активных металлоорганических соединений на основе производных ароилпировиноградных кислот / Н.А. Пулина, В.В. Залесов, П.А. Мокин [и др.] // Разработка, исследование и маркетинг новой фармацевтической продукции: сб. науч. тр. / ПятГФА.– Пятигорск, 2006.– Вып. 61.– С.282-284.
- Синтез биологически активных соединений на основе взаимодействия гетериламидов ароилпировиноградных кислот с гидразонами бензофенона и 9-флуоренона / Н.А. Пулина, П.А. Мокин, В.В. Залесов [и др.] // Приоритеты фармацевтической науки и практики: материалы заоч. Междунар. конф.- М.: РУДН, 2006.- С.268-270.
- Синтез и поиск биологически активных водорастворимых веществ в ряду производных гетериламидов α-оксокислот / Н.А. Пулина, П.А. Мокин, Ф.В. Собин [и др.] // Медицинский вестник Башкортостана.- 2006.- Т.4, №1.- С.200-202.
- Гетериламиды 4-арил-2,4-диоксобутановых кислот в синтезе новых биологически активных веществ / Н.А. Пулина, П.А. Мокин, В.В. Залесов [и др.] // Пути и формы совершенствования фармацевтического образования. Создание новых физиологически активных соединений: материалы 3-й Всерос. науч.- метод. конф.- Воронеж, 2007.- С.294-296.
- Гетериламиды α-оксокислот в синтезе биологически активных соединений / Н.А. Пулина, В.В. Залесов, В.В. Юшков, П.А. Мокин… // Вестник Перм. гос. фарм. акад.- Пермь, 2007.- №2.- С.89-92.
- Изучение антимикробной активности комплексных соединений на основе гетериламидов 4-арил-2,4-диоксобутановых кислот / Н.А. Пулина, В.В. Залесов, П.А. Мокин [и др.] // Человек и лекарство: Сб. материалов. XIV Росс. национ. конгр.: М., 2007.- С.868.
- Поиск биологически активных солей гетероциклических аминов и гетериламидов на основе 4-арил-2,4-диоксобутановых кислот / Н.А. Пулина, П.А. Мокин, В.В. Залесов [и др.] // Разработка, исследование и маркетинг новой фарм. продукции: сб. научн. тр.- Пятигорск: ПятГФА, 2007.- Вып. 62.- С.533-534.
- Поиск биологически активных соединений среди производных о-гидроксифенилглиоксалевой кислоты / Н.А. Пулина, В.В. Юшков, В.В. Залесов, П.А. Мокин… // Фармация.- 2007.- №5.- С.35-38.
- Пулина, Н.А. Взаимодействие гетериламидов 4-арил-2-гидрокси-4-оксо-2-бутеновых кислот с хлоридами двухвалентных металлов / Н.А. Пулина, В.В. Залесов, П.А. Мокин // Баш. хим. журн.- 2007.- Т.14, №3.- С. 52-56.
Автор выражает благодарность зав. кафедрой физики и математики, доц. М.И. Вахрину за запись спектров ЯМР1Н, научному сотруднику РИЦ «Фарматест» Е.Б. Бабушкиной за запись ИК-спектров, старшему преподавателю кафедры токсикологической химии Л.Н. Карповой за запись масс-спектров, зав. кафедрой фармакологии с курсом иммунологии, проф. В.В. Юшкову и аспиранту данной кафедры К.В. Яценко, зав. кафедрой физиологии с основами анатомии, проф. Б.Я. Сыропятову, зав. кафедрой микробиологии, проф. Т.Ф. Одеговой и ассистенту данной кафедры М.В. Томилову за проведение биологических испытаний синтезированных соединений.
Подписано в печать 04.12.2007
Формат 60*90/16. Набор компьютерный. Бумага ВХИ.
Тираж 100 экз. Усл. печ. л. 1,75. Заказ № 119/2007
Отпечатано на ризографе в типографии ГОУ ВПО ПГФА
614070, г. Пермь, ул. Крупской, 46
тел./факс. 8-901-266-59-37
