Синтез, оптические спектры и стереоатомный анализ структуры сложных халькогенидов, активированных фторидов и оксидов 01. 04. 07 физика конденсированного состояния
| Вид материала | Автореферат |
- Взаимосвязь электрических и магнитных свойств в сильно коррелированных электронных, 1439.13kb.
- Учебно-методический комплекс по дисциплине Физика Конденсированного Состояния Для специальности, 322.8kb.
- Паспорт специальности 01. 04. 07 – физика конденсированного состояния, 1004.81kb.
- Ён Викторович Методы визуализации кинетики зарождения и роста углеродных наноструктур, 219.01kb.
- Рабочая программа учебной дисциплины «Физика конденсированного состояния, термодинамика,, 223.9kb.
- Министерство образования Российской Федерации международный университет природы, общества, 1374.95kb.
- Рентгенографические исследования и построение моделей структуры ряда углеродных материалов, 315.25kb.
- Дефекты структуры, механические, электрические и магнитные свойства монокристаллических, 445.28kb.
- Аннотация рабочей программы дисциплины «Дифракционный структурный анализ» Направление, 26.86kb.
- Кинетика старения медно-бериллиевых сплавов в постоянном магнитном поле 01. 04., 427.06kb.
Далее приведены основные положения метода пересекающихся сфер, в рамках которого атому в кристалле приписывается два радиуса: фиксированный rS (слейтеровский радиус), значение которого однозначно обусловлено химической природой этого атома, т.е. характеризует условно изолированные, т.е. химически не связанные, атомы; переменный RСД, значение которого определяется химическим составом, структурой соединения, т.е. природой атомов окружения и их взаимным пространственным размещением.
С учетом постулированной двухсферной модели квазиизолированных атомов А и X возможны 18 вариантов парного межатомного взаимодействия (а именно: А-А, Х-Х и А-Х), с которыми в общем случае можно столкнуться в структурe любых кристаллов. Два атома, находящиеся на расстояниях, превышающих суммы радиусов их внешних сфер, считаются химически не связанными, так как в этом случае итоговое перекрывание их сфер (тип П0) равно нулю. Химическое взаимодействие двух атомов начинаемся с момента пересечения внешних сфер этих атомов. Такое взаимодействие называется одинарным перекрыванием П1. И так до тех пор, пока попарно перекрываются каждая из двух сфер одного атома с каждой из двух сфер соседнею атома (четверное перекрывание, тип П4).
Анализируется применение методов стереоатомного анализа, которые можно разделить на анализ структурных особенностей кристаллических материалов и на исследование взаимосвязи этих особенностей с физическими свойствами кристаллов.
Во второй части третьей главы с помощью комплекса программ TOPOS [3] на основании сведений о параметрах элементарных ячеек, пространственных группах симметрии и координатах атомов [4] для всех соединений, содержащих в структуре атомы кадмия в окружении серы, были рассчитаны характеристики полиэдров Вороного-Дирихле (ВД) базисных атомов.
Как показывают полученные результаты, атомы Cd по отношению к атомам серы могут проявлять КЧ 3, 4, 5 или 6. Наиболее характерна для атомов Cd тетраэдрическая координация, соответствующая КЧ 4. Значительно реже атомы Cd проявляют КЧ 5 и 6. При КЧ 5 во всех случаях образуются координационные полиэдры в виде искаженной тригональной бипирамиды, в которой расстояние Cd-S до одного апикального атома серы значительно длиннее (3.0(2)Å), чем до четырех остальных атомов серы (в среднем 2.58(5)Å). При КЧ 6 координационные полиэдры имеют форму октаэдра или тригональной призмы.
Длина связей Cd-S в 318 координационных полиэдрах CdSn изменяется в диапазоне от 2.39 до 3.29Å, а соответствующие им телесные углы () составляют от 9 до 24% полного телесного угла, равного 4 стерадиан. Несмотря на разнообразие формы полиэдров ВД атомов Cd, по данным регрессионного анализа, как валентные, так и невалентные взаимодействия независимо от КЧ атомов кадмия описываются единой линейной зависимостью
(Cd-S) = 42.1(2) - 9.30(5)r(Cd-S) (22)
с коэффициентом корреляции r = -0.970 для всех 2118 граней типа Cd-S или Cd/S. Именно наличие линейной зависимости типа (1) с r > 0.9 является в общем случае критерием существования ближнего порядка, обусловленного сильными химическими взаимодействиями в структуре кристаллов.
Согласно полученным данным, в зависимости от КЧ и формы координационных полиэдров атомов Cd объем (VПВД) их полиэдров ВД изменяется в пределах от 19 до 23 Å3 (табл. 4.2), а радиусы сферических доменов (RСД), объем которых равен VПВД, лежат в области 1.66-1.77Å.
Интегральным параметром, количественно характеризующим нецентросимметричность окружения атома комплексообразователя в структуре кристалла, является величина смещения атома из центра тяжести собственного полиэдра ВД (DA). По имеющимся данным, в большинстве случаев в пределах 2(DA) для атомов кадмия DA=0.
В структуре обсуждаемых соединений безразмерный параметр G3, характеризующий степень сферичности полиэдров ВД атомов Cd (для сферы G3=0.077), изменяется от 0.080 до 0.094. Наименьшее среднее значение G3 имеют атомы Cd с октаэдрической координацией, для которых оно совпадает с теоретическим значением 0.083 для правильного октаэдра. Максимальные значения G3 (в среднем 0.088(3)) соответствуют атомам Cd с тетраэдрической координацией. При этом для всех атомов Cd c КЧ 4 реальная величина G3 меньше теоретического значения 0.104 для идеального тетраэдра, что можно считать следствием влияния невалентных взаимодействий Cd/Z.
Аналогичные расчеты для полиэдров ZnSn показывают, что в зависимости от КЧ и формы координационных полиэдров атомов Zn объем их полиэдров ВД изменяется в пределах от 16 до 18.5Å3, а радиусы сферических доменов лежат в области 1.57-1.64Å. Безразмерный параметр G3, характеризующий степень сферичности полиэдров ВД атомов Zn, изменяется от 0.081 до 0.099. Наименьшее среднее значение G3 имеют атомы Zn с октаэдрической координацией, для которых оно совпадает с теоретическим значением 0.083 для идеального октаэдра. Максимальные значения G3 (в среднем 0.089) соответствуют атомам Zn с треугольной, тетраэдрической или тригонально-призматической координацией.
Согласно полученным результатам (для координационных полиэдров GaSn в структуре кристаллов) в зависимости от КЧ и степени окисления атомов Ga объем их полиэдров ВД (VПВД) изменяется в широких пределах от 14.7 до 21.1Å3, а радиусы сферических доменов (RСД), объем которых равен VПВД, лежат в области 1.52-1.72Å. Отметим, что для атомов Ga(III) с КЧ 6 и 3 значения RСД практически совпадают (соответственно 1.522 и 1.529Å), тогда как для Ga(III) с КЧ 4 RСД увеличено в среднем до 1.64Å. Этот факт связан со сравнительно сильным искажением в структуре кристаллов как линейных, так и угловых параметров тетраэдров GaS4.
В заключение заметим, что параметры полиэдров ВД являются важными интегральными характеристиками атомов в структуре кристаллов. Поэтому их существенное отклонение от среднего значения для атомов некоторого элемента с фиксированной природой атомов первой координационной сферы позволяет легко выявлять ошибки в кристаллоструктурной информации, содержащейся в базах данных [4]. Например, в процессе данного исследования было обнаружено, что в структуре MgGa2S4 {15350} [5], содержащей три разных атома Ga c КЧ 4, характеристики полиэдров ВД Ga(1) и Ga(3) аномально отличаются от
Табл. 1. Влияние ошибки в координате атома S(6) на некоторые параметры
полиэдров ВД атомов галлия в структуре MgGa2S4 {15350}.
| Параметр полиэдра ВД | Ga(1) | Ga(2) | Ga(3) | Среднее значение для Ga(III) с КЧ 4 | |||
| с ошибкой | без ошибки | с ошибкой | без ошибки | с ошибкой | без ошибки | ||
| RСД, Å | 1.617 | 1.652 | 1.643 | 1.643 | 1.732 | 1.648 | 1.638(29) |
| DA, Å | 0.15 | 0.10 | 0.06 | 0.06 | 0.23 | 0.06 | 0.06(5) |
| G3 (104) | 934 | 927 | 921 | 921 | 909 | 928 | 928(29) |
таковых для Ga(2), так и от средних значений для остальных атомов Ga(III) с КЧ 4 (табл. 3). Проведенный с помощью комплекса TOPOS анализ позволил установить, что в статье [5] имеется опечатка для координаты z атома S(6) (вместо правильного значения 0.01223 опубликовано 0.1223), которая была повторена и в базе данных [4]. Как видно из данных табл. 1, после устранения указанной ошибки характеристики атомов Ga(1) и Ga(3) в пределах погрешности совпали со среднестатистическими значениями, тогда как для Ga(2) полиэдр ВД не изменился. Это и не удивительно, так как полиэдр ВД атома Ga(2), в отличие от Ga(1) или Ga(3), не имеет ни одной общей грани с полиэдром ВД атома S(6).
В четвертой главе на основе анализа литературных данных показано, что физической причиной взаимодействия мод является гиротропия кристаллов, причем под гиротропией понимают наблюдаемые в кристаллооптике оптические явления, связанные с проявлением эффектов пространственной дисперсии первого порядка. Помимо явления оптической активности, связанного со способностью вещества вращать плоскость поляризации света, к ним относятся: циркулярный дихроизм, эллиптическое двулучепреломление, возникновение продольной составляющей электрического поля, появление добавочных световых волн. Кристаллы, для которых псевдотензор гирации gik отличен от нуля, называют оптически активными. Оптической активностью могут обладать кристаллы всех сингоний. Необходимым условием является наличие в структуре кристалла винтовых осей симметрии. Исключив из 32 видов симметрии 11 центросимметричных и 10, имеющих инверсионные оси и плоскости симметрии, получим 11 видов симметрии, кристаллы которых обладают способностью вращать плоскость поляризации. Показано, что носителем гиротропии в халькопиритных кристаллах является фрагмент структуры – искаженный тетраэдр СА2В2. Однако соображения, основанные на анализе симметрии, лишь разрешают гиротропию, но не доказывают ее существование.
Поскольку изотропная точка в кристаллах со структурой дефектного халькопирита обнаружена только в тиогаллате кадмия, был проведен стереоатомный анализ его структуры с помощью программного комплекса TOPOS. Используя программы AutoCN и Dirichlet программного комплекса TOPOS, мы установили типы связи атома халькогена, входящего в структуру CdGa2S4 и других изоструктурных ему соединений. Показано, что сокращение межъядерных расстояний r(A-X) в общем случае неизбежно сопровождается увеличением объема соответствующих парных пересечений типа
rSRСД (23)
и/или
RСДrS. (24)
Ненулевые по величине пересечения типа (23) или (24) можно интерпретировать как наличие переноса электронной плотности с валентной оболочки атома радиуса rS на вакантные валентные орбитали соседнего атома с радиусом RСД. С указанной точки зрения пересечения типа П2, при которых одно из двух произведений вида (23) или (24) непременно равно нулю, можно трактовать как донорно-акцепторные или ионные связи. Поэтому при образовании связи донором электронов (в рамках ковалентной модели химической связи) или образующимся катионом (с позиций ионной модели) будет являться тот атом, значение rS которого входит в ненулевое по абсолютной величине произведение (23) или (24). Например, если для некоторой связи А-Х rS(А)RСД(Х) = 0, а RСД(А)rS(Х) > 0, то атом Х является донором электронов (катионом), а атом А - акцептором электронов (анионом).
В тех случаях, когда оба произведения (23) или (24) одновременно не равны нулю (пересечения типа П4 или П3), реально возможны две ситуации. Так, если взаимодействующие атомы идентичны как химически (при этом их значения rS = const), так и кристаллографически (при этом их значения RСД = const), то пересечения rSRСД RСДrS > 0 и возникающая связь будет ковалентной неполярной, так как перенос электронной плотности от левого атома к правому (определяется пересечением (23)) будет полностью компенсироваться идентичным по величине переносом от правого атома к левому (определяется пересечением (24)). Если же при перекрывании типа П3 или П4 вследствие химической и (или) кристаллографической неэквивалентности взаимодействующих атомов значения произведений (23) и (24) отличаются, то соответствующую связь можно назвать ионно-ковалентной (или полярной ковалентной). При этом в некоторой связи А-Х атомом, приобретающим заряд +, будет являться тот атом, значение rS которого входит в большее по абсолютной величине произведение (23) или (24). Например, если для связи А-Х rS(А)RСД(Х) > RСД(А)rS(Х) > 0, то итогом химического взаимодействия изначально нейтральных атомов А и Х явится увеличение электронной плотности (возникнет некоторый заряд -) в области действия атома Х, тогда как у атома А, являющегося более сильным донором (или более слабым акцептором) электронов, возникнет равный по абсолютной величине заряд +. Таким образом, согласно использованной модели при пересечениях типа П2, П3 или П4 перенос электронной плотности между атомами А и Х при возникновении связи А-Х, в общем случае должен быть пропорционален разности
П(А-Х)=rS(А)RСД(Х) - RСД(А)rS(Х). (25)
Так как объем ПВД атомов халькогенов также зависит от состава соединения, то для сравнения степени переноса электронной плотности используем безразмерную величину =
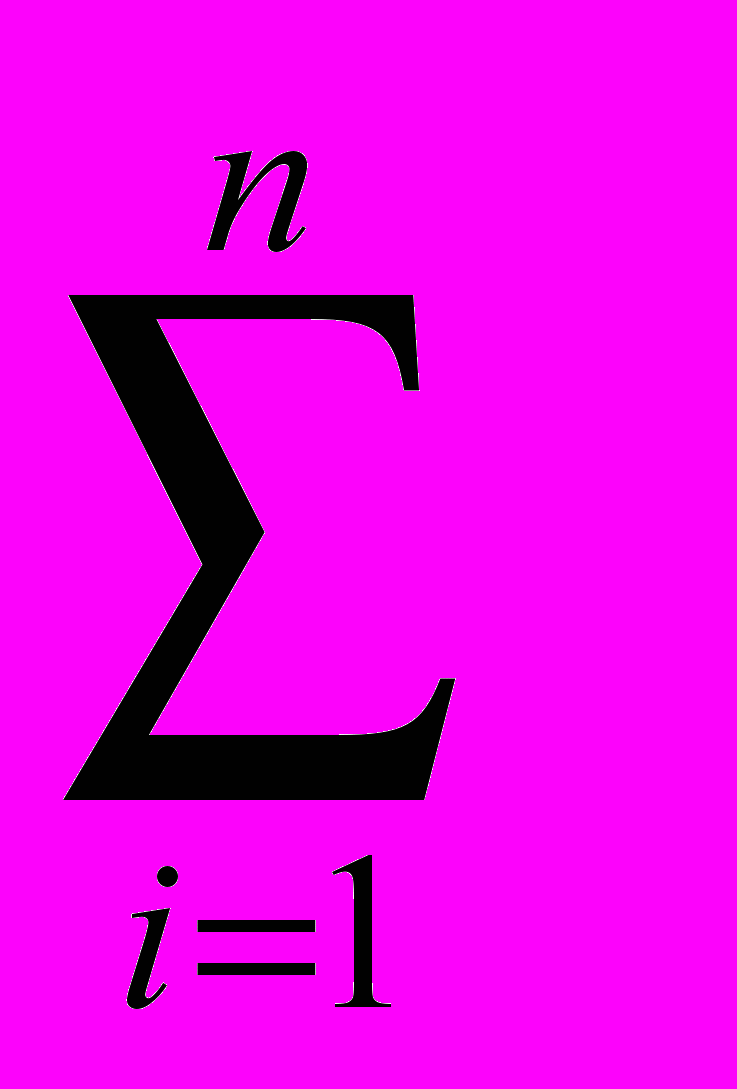 Пi/VПВД.
Пi/VПВД.Для соединений I-V (ZnGa2S4 (I), CdGa2S4 (II), HgGa2S4 (III), CdGa2Se4 (IV) и CdGa2Te4 (V)) равно соответственно 0.137, 0.157, 0.146, 0.100 и 0.025. Таким образом, в изоструктурных I-V соединениях максимальная величина μ и, как следствие, максимальный отрицательный заряд - на атомах халькогена отвечает кристаллам CdGa2S4 (II), обладающим точкой изотропии. Поэтому указанные данные позволяют предположить, что особенности оптических свойств изоструктурных соединений I-V зависят от степени ионности связей металл – халькоген. Имеющиеся экспериментальные данные для I-V дают основание считать, что точкой изотропии обладают вещества только с относительно высокой степенью ионности связей М-Х (>0.15). У веществ же со сравнительно небольшой степенью ионности связей М-Х (<0.15) точка изотропии отсутствует.
Твердые растворы замещения кристаллических полупроводников представляют собой особый класс неупорядоченных систем, в котором беспорядок обусловлен случайным характером расположения атомов, образующих твердый раствор, по узлам кристаллической решетки. Беспорядок, таким образом, является внутренним свойством твердого раствора и может иметь различные формы. Однако некоторые свойства твердых растворов могут быть достаточно хорошо описаны в модели виртуального кристалла, в рамках которой реальный твердый раствор аппроксимируется идеальным псевдокристаллом, в узлах которого находятся псевдоатомы, свойства которых определяются линейной комбинацией соответствующих свойств реальных атомов, из которых построен раствор. В этой модели, не учитывающей вообще наличие беспорядка, удается, тем не менее, описать в первом приближении многие важные свойства, в частности, концентрационные зависимости ширин запрещенных зон, а также постоянных решетки твердого раствора.
Используя предложенную модель, рассматриваем структурные особенности кристаллов твердых растворов на основе тиогаллата кадмия, для которых известно о существовании изотропной точки. В системе CdGa2S4 – ZnGa2S4 существует непрерывный ряд твердых растворов, причем для кристаллов CdGa2S4 изотропная точка существует и наблюдается при λ0 = 493 Å, тогда как для ZnGa2S4 она отсутствует. Однако для кристаллов твердых растворов состава Cd1-хZnxGa2S4, где х изменяется в пределах от 0 до 0,072, изотропная точка существует и изменяется от 493 до 661 Å. Полученные результаты показывают, что замещение атомов кадмия атомами цинка сопровождается закономерным понижением суммы П в твердых растворах Cd1-хZnхGa2S4. При этом с ростом концентрации цинка (х) безразмерный параметр = П / VПВД практически линейно уменьшается, составляя при x = 0, 0.2, 0.4, 0.6, 0.8 и 1 соответственно 0.157, 0.153, 0.149, 0.145, 0.141 и 0.137. Существенно, что для всех твердых растворов Cd1-хZnхGa2S4 при х 0.2 параметр 0.15, и поэтому такие твердые растворы, как и CdGa2S4, должны обладать точкой изотропии, что нами экспериментально подтверждено данными для образцов с х<0.072.
Аналогичные расчеты для систем твердых растворов CdGa2S4 – HgGa2S4, CdGa2S4 – CdGa2Se4, и CdGa2S4 – CdGa2Te4 показывают, что предельные соединения Cd0,68Hg0,32Ga2S4, CdGa2S3,76Se0,24, CdGa2S3,94Te0,06 должны обладать изотропной точкой. Первое и последнее соединения на наличие ИТ не исследовались, а для системы CdGa2S4 – CdGa2Se4 нами установлено, что для состава CdGa2S3,92Se0,08 длина волны изотропии λо равна 654 нм.
Таким образом, критерий >0.15, где величина определяет степень ионности связей М-Х, указывает на вещества со структурой дефектного халькопирита, которые обладают точкой изотропии.
Анализ полученных данных об основных характеристиках полиэдров ПВД показывает, что такие характеристики, как объем полиэдров Вороного – Дирихле, объем координационного полиэдра и площадь поверхности ПВД всех атомов, входящих в структуру, уменьшаются линейно с увеличением концентрации Ga2S3 (рис. 7).
Вместе с тем, как показано в четвертой главе, для кристаллов твердых растворов на основе тиогаллата кадмия в системе CdS – Ga2S3 наблюдается линейный рост положения изотропной точки с увеличением концентрации Ga2S3. Таким образом, можно сделать вывод о том, что уменьшение объема полиэдра Вороного-Дирихле атома серы закономерно ведет к увеличению значений длины волны изотропии в кристаллах со структурой дефектного халькопирита.
Действительно, построенные по рассчитанным данным графики зависимости объема полиэдров Вороного – Дирихле от состава в системе CdGa2S4–ZnGa2S4 показывают, что они уменьшаются нелинейно с увеличением концентрации ZnGa2S4. Что сопровождается нелинейным ростом положения изотропной точки.
Аналогичные зависимости наблюдаются и в системе CdGa2S4 - MgGa2S4 (рис. 9).
Таким образом, в системах твердых растворов на основе тиогаллата кадмия наблюдается закономерный рост значений длины волны изотропии с уменьшением объема полиэдра Вороного-Дирихле, а ее существование ограничено величиной степени ионности химической связи μ халькогена с элементами, входящими в полиэдр С□АВ2.
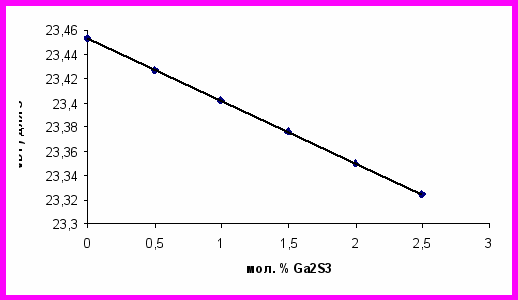
Рис. 7. Зависимость объема ПВД атома серы от концентрации Ga2S3 в системе CdS – Ga2S3.
С целью подтверждения возможности использования предложенного критерия существования изотропной точки и распространения области его применения во второй части
